Clear Sky Science · de
Von Impfstoffen abgeleitete T‑Zell‑Antworten reichen nicht aus, um Schutzimmunität gegen SARS‑CoV‑2 zu erzeugen
Warum diese Forschung wichtig ist
Als COVID‑19‑Impfstoffe eingeführt wurden, richtete sich viel Aufmerksamkeit auf Antikörper — die Proteine, die das Virus daran hindern können, unsere Zellen zu infizieren. Eine andere Komponente des Immunsystems, die T‑Zellen, wird jedoch häufig dafür verantwortlich gemacht, dass Menschen nicht ins Krankenhaus müssen und dass ein länger anhaltender Schutz besteht. Diese Studie stellt eine einfache, aber entscheidende Frage: Reicht ein Impfstoff, der starke T‑Zell‑Antworten auslöst, aber wenig oder keine neutralisierenden Antikörper produziert, aus, um vor schwerem COVID‑19 zu schützen?
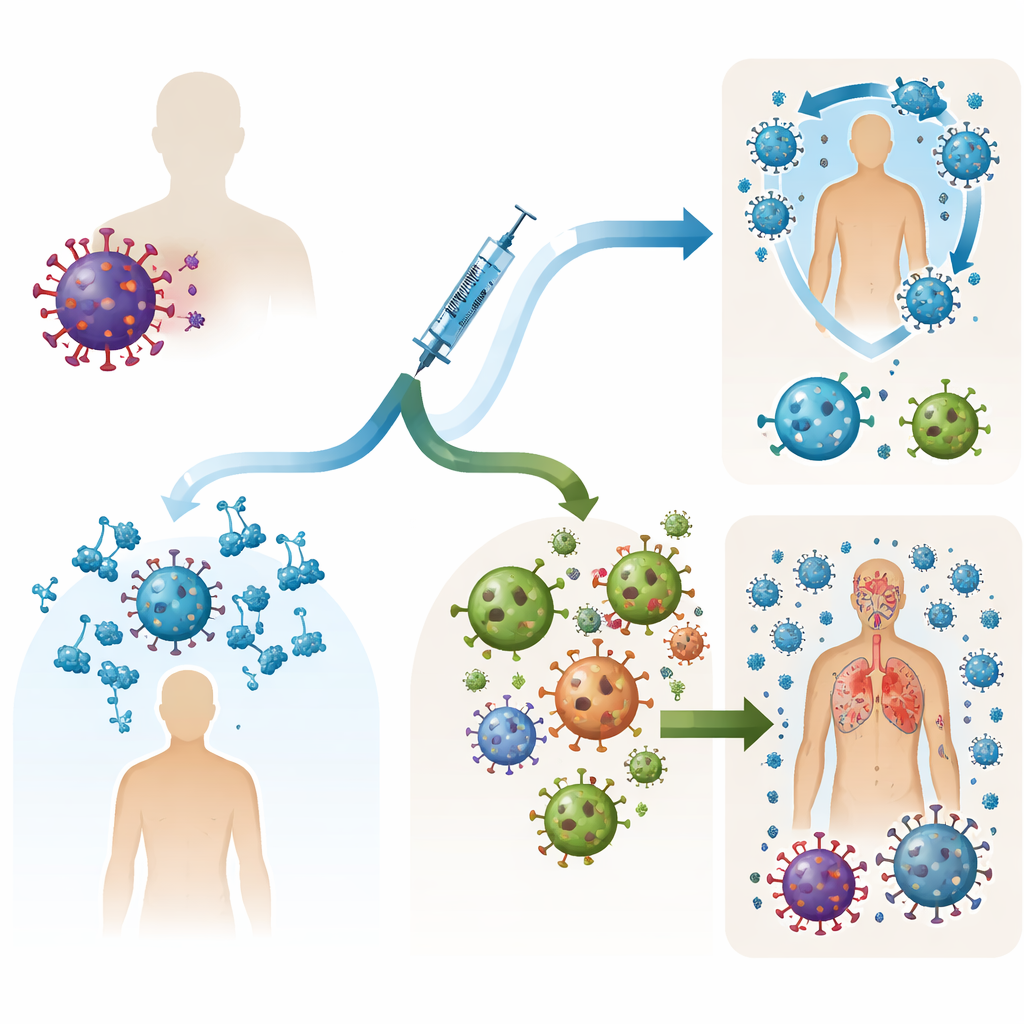
Die beiden Hauptverteidigungslinien
Unser Immunsystem bekämpft Viren auf zwei grundsätzliche Arten. Antikörper schwimmen im Blut und Schleim und heften sich an Viren, bevor diese in Zellen eindringen. Neutralisierende Antikörper sind besonders wirksam, weil sie Schlüsselstrukturen blockieren, die das Virus zur Invasion nutzt. T‑Zellen dagegen patrouillieren im Gewebe, suchen bereits infizierte Zellen und zerstören diese, wodurch die Ausbreitung einer Infektion begrenzt wird. Viele Patientinnen und Patienten, die keine guten Antikörper bilden können — zum Beispiel Personen mit bestimmten Blutkrebserkrankungen oder unter B‑Zell‑depletierenden Therapien — entwickeln nach einer Impfung dennoch T‑Zell‑Antworten. Das nährte die Hoffnung, dass ein „T‑Zell‑zentrierter“ Impfstoff Menschen mit schwacher Antikörperantwort schützen könnte.
Impfstoffe so entwerfen, dass sie T‑Zellen bevorzugen
Das Forschungsteam verwendete DNA‑Impfstoffe, eine Plattform, bei der kleine ringförmige DNA‑Stücke Zellen anweisen, virale Proteine herzustellen. Sie konstruierten mehrere Varianten des SARS‑CoV‑2‑Spike‑Proteins, darunter eine mit einem verkürzten Schwanz (ΔC) und eine andere mit entfernten Schlüsselspaltstellen und einem eingefügten flexiblen Linker (Linker‑ΔT). Einige Varianten wurden mit einer Chemokin‑Domäne namens MIP3α fusioniert, die das Spike‑Protein zu antigenpräsentierenden Zellen bringt — Immunwächter, die besonders gut darin sind, T‑Zellen zu aktivieren. Bei Mäusen lösten diese Konstrukte zuverlässig starke CD4‑ und CD8‑T‑Zell‑Antworten aus, die entzündliche Botenstoffe sezernierten, wie sie für eine antivirale, sogenannte „Typ‑1“‑Antwort typisch sind. Ein Konstrukt, Linker‑ΔT, wurde speziell so entworfen, die Form des Spike so weit zu verändern, dass Antikörper kaum stimuliert werden, während weiterhin viele T‑Zell‑Epitope präsentiert werden.
Was geschah, als das Virus angriff
Als die Impfstoffe in einem transgenen Mausmodell getestet wurden, das humanes ACE2 exprimiert — denselben Rezeptor, den SARS‑CoV‑2 beim Menschen nutzt —, wurde das Bild klarer. Die auf ΔC basierenden Impfstoffe erzeugten Antikörper, die an Spike und dessen rezeptorbindende Domäne aus mehreren Varianten binden konnten, diese Antikörper neutralisierten das Virus jedoch nicht in standardisierten Labortests. Die Linker‑ΔT‑Designs erzeugten, wie beabsichtigt, nahezu keine nachweisbaren Antikörper, trieben aber weiterhin robuste T‑Zell‑Aktivität an. Bei allen diesen Impfstofftypen zeigten die Mäuse starke T‑Zell‑Zytokinantworten gegen Spike. Doch als sie einer tödlichen Dosis von lebendem SARS‑CoV‑2 ausgesetzt wurden, schützte keiner der geimpften Gruppen vor Gewichtsverlust oder Tod im Vergleich zu Kontrolltieren.
Lehren für die Impfstoffgestaltung
Diese Ergebnisse fügen sich in eine wachsende Datenlage bei Menschen und nichtmenschlichen Primaten: Die Spiegel neutralisierender Antikörper korrelieren stark damit, wie gut Impfstoffe symptomatische Infektionen verhindern. T‑Zellen bleiben dennoch sehr wichtig. Sie scheinen dabei zu helfen, eine Infektion schneller zu beseitigen, die Schwere der Erkrankung zu reduzieren und gegenüber neuen Varianten aktiv zu bleiben, auch wenn Antikörper an Wirksamkeit verlieren. Aber in diesem strengen Mausmodell reichten kraftvolle T‑Zell‑Antworten, ausgelöst durch chemokin‑fusionierte DNA‑Impfstoffe, allein nicht aus. Die Autorinnen und Autoren argumentieren, dass die von ihnen eingeführten Spike‑Änderungen vermutlich Schlüsselmerkmale für die Neutralisation verzerrt haben und dass die erzeugten T‑Zellen möglicherweise nicht die optimalen Eigenschaften besaßen, etwa in Bezug auf Gewebeverteilung oder zytotoxische Kapazität.
Was das für die Zukunft bedeutet
Für ein Laienpublikum ist die Schlussfolgerung klar: Ein Impfstoff, der hauptsächlich T‑Zellen trainiert, ohne gleichzeitig neutralisierende Antikörper zu erzeugen, schützte Mäuse in dieser Studie nicht vor schwerem COVID‑19. Die Arbeit stützt die Idee, dass die besten Impfstoffe beides anstreben sollten — starke, korrekt geformte Antikörper, die das Eindringen von Viren blockieren, und robuste T‑Zell‑Antworten, die eventuelle Durchbruchsinfektionen beseitigen. Das ist besonders relevant für Personen mit eingeschränkter Antikörperantwort. Zukünftige Impfstoffe könnten intelligentes Antigen‑Design, das neutralisierende Zielstrukturen erhält, mit Liefertricks wie Chemokinfusion kombinieren, um einen ausgewogenen, zweigleisigen Schutz zu erreichen, statt sich allein auf T‑Zellen zu verlassen.
Zitation: Cha, SC., Szymura, S.J., Anderson, A. et al. Vaccine-derived T-cell responses are insufficient to generate protective immunity to SARS-CoV-2. Sci Rep 16, 14331 (2026). https://doi.org/10.1038/s41598-026-44391-x
Schlüsselwörter: SARS‑CoV‑2‑Impfstoffe, T‑Zell‑Immunität, neutralisierende Antikörper, DNA‑Impfstoffe, COVID‑19‑Schutz