Clear Sky Science · zh
一种诱导二尖瓣反流的新技术,作为容量负荷诱发心力衰竭的猪科实验模型
这项猪心研究为何重要
心力衰竭是全球主要的疾病与死亡原因之一,许多病例由瓣膜漏导致,迫使心脏反复额外泵血。在将新药、器械或外科方法安全地用于人体之前,科学家需要能贴切模拟人类心脏病理的动物模型。这项研究引入了一种简单但有效的方法,在猪体内建立稳定的瓣膜相关心力衰竭模型。猪的心脏功能与人为相似,这为更好地测试未来治疗方案提供了可能。
心脏主泵的一个漏门
在许多患者中,心力衰竭是由于二尖瓣——位于左心房与左心室之间——不再紧密关闭所致。每次心跳都会有部分血液逆流回去,造成长期的容量负荷,逐渐扩张并削弱心肌。现有的大型动物模型存在缺点:常通过损伤冠状动脉来引发瓣膜病变,这会引入类似心肌梗死的损伤,使结果不稳定且难以解释。作者旨在建立一个仅聚焦于瓣膜反流本身的模型,避免对心脏造成额外隐性损伤。
直接且可控的制造瓣膜反流方法
研究团队使用了25头健康的皮特兰(Piétrain)猪,这是一种常见的农场品种,其心脏结构和功能与人类相似。17头猪接受了制造明显二尖瓣反流的手术,8头则接受了相似的“假手术”但未损伤瓣膜。在全身麻醉及开胸方式下,研究人员轻柔地打开包绕心脏的囊,并从左心室尖端插入定制工具。在直接置于心脏表面的高质量超声引导下,他们勾住并切断了帮助瓣膜关闭的一根细索(腱索),通过调整切断的腱索选择,直到形成一个强而定向的逆流喷射。在假手术组中,工具虽被引入但腱索保持完整,瓣膜功能保持正常。
观察心脏在四周内的适应
术后,所有动物都给予细致的镇痛、抗生素治疗,反流组还使用利尿剂以缓解液体潴留。猪只随访四周,随后重复超声检查并在显微镜下检查心肌组织。所有被诱导反流的猪只,影像学均证实存在非常严重的瓣膜病变,伴有偏心的血液逆流射向上腔。与假手术组相比,这些猪的心房与心室明显扩大,体现在左心房与左心室在充盈末期与收缩末期体积显著增加。同时,射血分数与缩短分数等关键泵功能指标显著下降,表明心脏功能已经开始衰弱。
肌肉中的瘢痕与该模型的比较
组织学检查得出了相似结论。暴露于瓣膜反流的心脏,其主泵室(左心室)中的纤维瘢痕样组织量约为假手术心脏的两倍。这个模式——腔室扩大、泵功能减弱和纤维化增加——与人类因二尖瓣反流引起的早期心力衰竭相一致。重要的是,雄性与雌性猪表现出类似的改变,且几乎所有动物中反流都强而均一,这是许多早期模型难以实现的。由于该方法仅针对腱索并避免阻断冠状动脉,它能在不引入心肌梗死混杂损伤的情况下,单独孤立出容量负荷的效应。
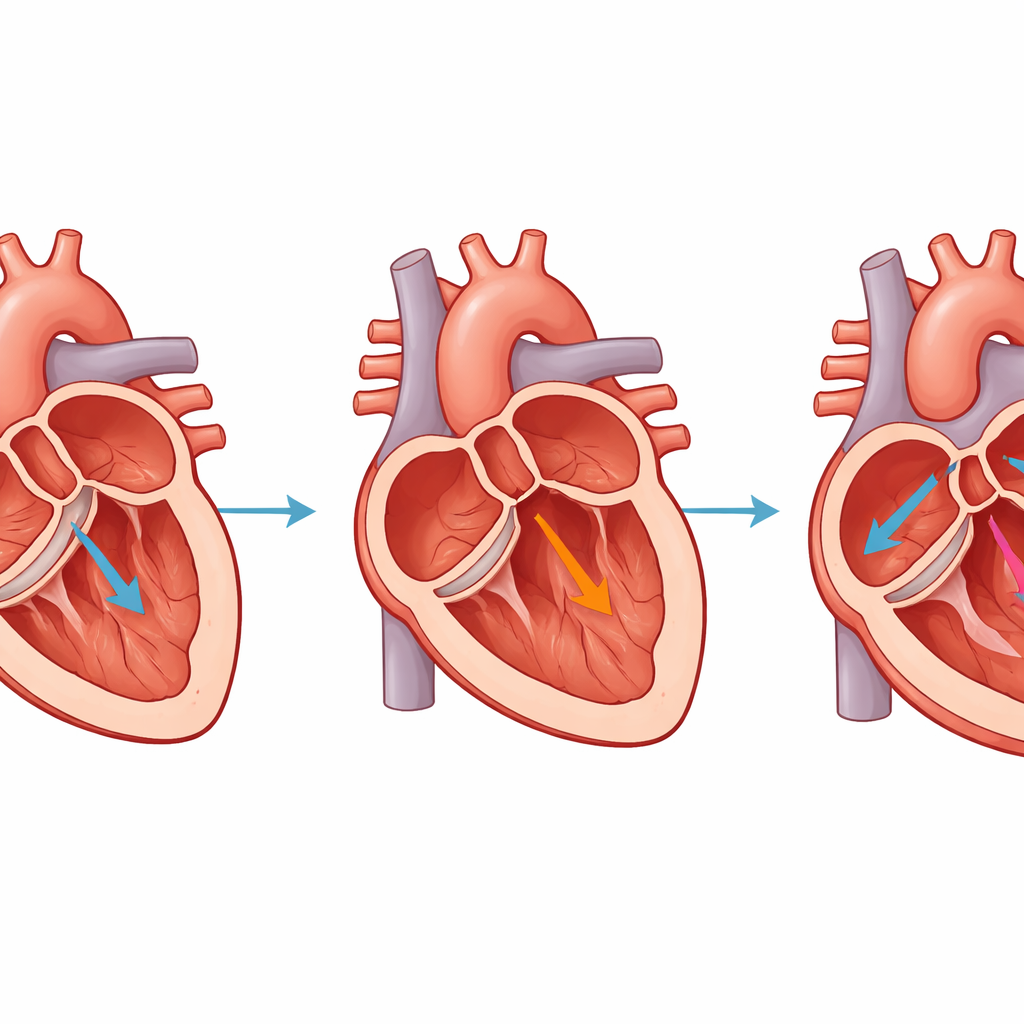
对未来治疗的意义
简而言之,研究者建立了一种可靠的方法,使猪心在短时间内出现与人类在严重瓣膜反流下相似的扩张、功能减退与瘢痕形成。在仅四周内,动物即可发展到由慢性容量负荷单独驱动的临床意义明确的心力衰竭阶段。该模型特别适合用于测试新的成像方法、药物和器械,目标可以是修复瓣膜或保护心肌免受长期损伤。通过提供更干净、更可控的实验条件,这一猪模型有望加速从实验室发现到改善瓣膜相关心力衰竭患者生活的治疗路径。
引用: Van Laer, S.L., Goovaerts, B., Laga, S. et al. A new technique inducing mitral valve regurgitation as an experimental porcine model of volume-overload induced heart failure. Sci Rep 16, 13500 (2026). https://doi.org/10.1038/s41598-026-43623-4
关键词: 心力衰竭, 二尖瓣关闭不全, 动物模型, 猪心脏病学, 容量负荷