Clear Sky Science · it
Una nuova tecnica per indurre insufficienza mitralica come modello sperimentale su suini di scompenso cardiaco da sovraccarico di volume
Perché questo studio sul cuore del maiale è importante
Lo scompenso cardiaco è una delle principali cause di malattia e morte a livello mondiale, e molti casi sono determinati da una valvola cardiaca che perde, costringendo il cuore a pompare sangue in eccesso ripetutamente. Prima che nuovi farmaci, dispositivi o approcci chirurgici possano essere testati in sicurezza sull’uomo, i ricercatori hanno bisogno di modelli animali che riproducano fedelmente ciò che avviene nei cuori umani. Questo studio presenta un metodo semplice ma efficace per creare una forma stabile di scompenso legato alla valvola nei suini, i cui cuori si comportano in modo molto simile ai nostri, aprendo la strada a test più accurati per i trattamenti futuri.
Una porta che perde nella pompa principale del cuore
In molti pazienti lo scompenso si sviluppa perché la valvola mitrale, che si trova tra il principale ventricolo di pompaggio e l’atrio che lo alimenta, non si chiude più ermeticamente. A ogni battito, una parte del sangue viene così spinta all’indietro invece che in avanti, creando un sovraccarico cronico di volume che progressivamente dilata e indebolisce il muscolo cardiaco. I modelli su animali di grandi dimensioni esistenti presentano limiti: spesso si basano sul danneggiamento delle arterie coronariche per indurre la perdita valvolare, il che introduce un danno simile a un infarto e rende i risultati meno prevedibili. Gli autori hanno quindi voluto sviluppare un modello focalizzato esclusivamente sulla perdita valvolare, senza danni aggiuntivi nascosti al cuore.
Un modo diretto ma controllato per provocare la perdita valvolare
Il gruppo ha lavorato con 25 suini Piétrain sani, una razza di allevamento comune il cui cuore ha struttura e funzionamento simili a quelli umani. Diciassette suini sono stati sottoposti a una procedura per creare una grave insufficienza mitralica, mentre otto hanno subito un intervento “finto” (sham) senza danneggiare la valvola. In anestesia generale e con approccio a torace aperto, i ricercatori hanno delicatamente aperto il sacco pericardico e inserito uno strumento artigianale attraverso l’apice del ventricolo sinistro. Guidati da immagini ecografiche di alta qualità posizionate direttamente sulla superficie cardiaca, hanno agganciato e reciso uno dei sottili filamenti (corde tendinee) che aiutano la valvola a chiudersi, regolando quale corda recidere fino a ottenere un getto retrogrado di sangue forte e ben diretto. Negli animali sham lo strumento è stato introdotto ma le corde sono state lasciate intatte, così le valvole hanno continuato a funzionare normalmente.
Osservare l’adattamento del cuore durante quattro settimane
Dopo l’intervento, tutti gli animali hanno ricevuto un attento controllo del dolore, antibiotici e, nel gruppo con la perdita, diuretici per ridurre l’accumulo di liquidi. I suini sono stati seguiti per quattro settimane, dopo le quali il gruppo ha ripetuto le ecografie e ha esaminato i tessuti cardiaci al microscopio. In ogni animale con insufficienza indotta, le immagini hanno confermato una perdita valvolare molto grave con un getto eccentrico di sangue che risale nell’atrio. Rispetto al gruppo sham, questi suini hanno sviluppato atri e ventricoli molto più grandi, come evidenziato da aumenti marcati dei volumi dell’atrio sinistro e del ventricolo sinistro sia alla fine della fase di riempimento sia alla fine della fase di contrazione cardiaca. Allo stesso tempo, parametri chiave della funzione di pompaggio, come la frazione di eiezione e il frazionamento della contrazione, sono diminuiti bruscamente, indicando che i cuori stavano già indebolendosi.
Cicatrici nel muscolo e come si colloca questo modello
Le analisi istologiche hanno raccontato una storia coerente. I cuori esposti alla perdita valvolare presentavano circa il doppio del tessuto fibrotico di tipo cicatriziale nel ventricolo principale rispetto ai cuori sham. Questo quadro—dilatazione delle camere, riduzione della forza di pompaggio e aumento della fibrosi—ricalca le fasi iniziali dello scompenso cardiaco umano causato dall’insufficienza mitralica. È significativo che sia i suini maschi sia le femmine abbiano mostrato cambiamenti simili, e che la perdita fosse intensa e uniforme nella quasi totalità degli animali, un risultato che molti modelli precedenti avevano faticato a ottenere. Poiché il metodo agisce solo sulle corde valvolari ed evita l’occlusione delle arterie coronariche, isola gli effetti del sovraccarico di volume senza il danno confondente di un infarto.
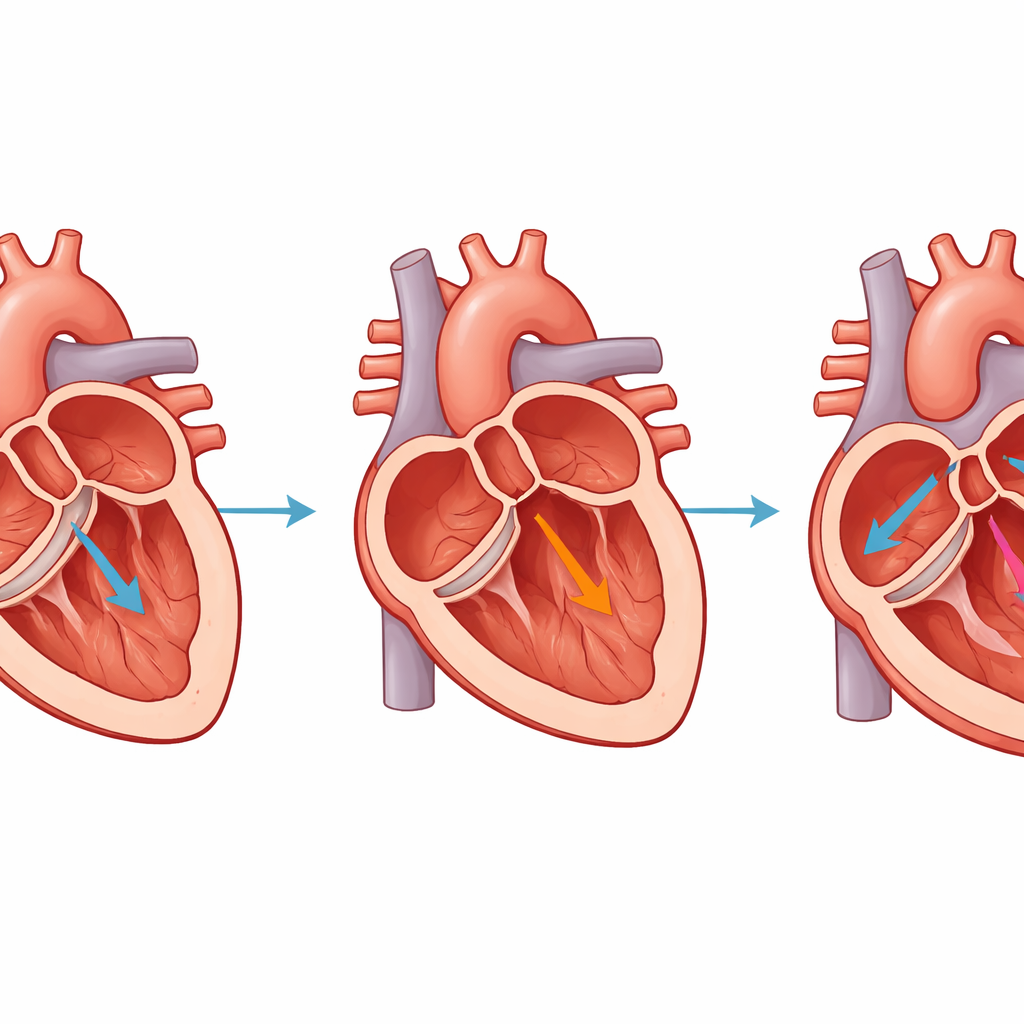
Cosa significa per i trattamenti futuri
In termini pratici, i ricercatori hanno creato un modo affidabile per indurre nei cuori dei suini lo stesso tipo di dilatazione, indebolimento e formazione di cicatrici che i cuori umani sperimentano quando una valvola principale perde gravemente. In appena quattro settimane, gli animali progrediscono verso una fase clinicamente significativa di scompenso guidato esclusivamente dal sovraccarico di volume cronico. Questo rende il modello particolarmente utile per testare nuove tecniche di imaging, farmaci e dispositivi mirati sia a riparare la valvola sia a proteggere il muscolo cardiaco dal danno a lungo termine. Fornendo un assetto sperimentale più pulito e controllato, questo modello suino può accelerare il percorso dalle scoperte di laboratorio a terapie che migliorano la vita dei pazienti con scompenso cardiaco legato a patologie valvolari.
Citazione: Van Laer, S.L., Goovaerts, B., Laga, S. et al. A new technique inducing mitral valve regurgitation as an experimental porcine model of volume-overload induced heart failure. Sci Rep 16, 13500 (2026). https://doi.org/10.1038/s41598-026-43623-4
Parole chiave: scompenso cardiaco, insufficienza mitralica, modelli animali, cardiologia suina, sovraccarico di volume