Clear Sky Science · nl
Een nieuwe techniek om mitralisklepinsufficiëntie te veroorzaken als experimenteel varkensmodel van door volume-overbelasting veroorzaakte hartfalen
Waarom deze studie met varkenshart belangrijk is
Hartfalen is een van de belangrijkste oorzaken van ziekte en sterfte wereldwijd, en veel gevallen worden veroorzaakt door een lekkende hartklep die het hart dwingt herhaaldelijk extra bloed te pompen. Voordat nieuwe medicijnen, apparaten of chirurgische methoden veilig bij mensen getest kunnen worden, hebben wetenschappers diermodellen nodig die nauwkeurig nabootsen wat er in menselijke harten gebeurt. Deze studie introduceert een eenvoudige maar krachtige manier om een stabiele vorm van klepgerelateerd hartfalen bij varkens te creëren; varkensharten gedragen zich sterk vergelijkbaar met die van mensen, wat de deur opent naar betere tests van toekomstige behandelingen.
Een lekkende klep in de belangrijkste hartpomp
Bij veel patiënten ontwikkelt hartfalen zich omdat de mitralisklep, die tussen de belangrijkste pompkamer van het hart en de kamer die daaraan toevoert ligt, niet meer goed sluit. Bij elke hartslag stroomt dan een deel van het bloed achteruit in plaats van vooruit, wat een chronische volume-overbelasting veroorzaakt die het hartspier langzaam uitrekt en verzwakt. Bestaande modellen bij grote dieren voor dit probleem hebben nadelen: ze berusten vaak op het beschadigen van kransslagaders om lekkage te veroorzaken, wat verwonding vergelijkbaar met een hartinfarct introduceert en de resultaten minder voorspelbaar maakt. De auteurs wilden een model bouwen dat zich puur richt op de lekkage zelf, zonder bijkomende verborgen schade aan het hart.
Een directe maar gecontroleerde manier om de klep te laten lekken
Het team werkte met 25 gezonde Piétrain-varkens, een veelvoorkomend fokras waarvan de hartstructuur en -functie lijken op die van mensen. Zeventien varkens ondergingen een procedure om een sterke lekkage over de mitralisklep te creëren, terwijl acht een vergelijkbare “sham”-operatie kregen zonder de klep te beschadigen. Onder algehele anesthesie en via een open-chest benadering openden de onderzoekers voorzichtig het hartzakje en brachten een op maat gemaakt instrument in door de punt van de linkerkamer. Met hulp van hoogwaardige echobeelden die rechtstreeks op het hart werden geplaatst, haakten ze één van de fijne peesdraden (chorda tendinea) die de klep helpen sluiten en sneden deze door, waarbij ze precies bepaalden welke draad ze moesten doorknippen totdat ze een sterke, gerichte terugstroom van bloed bereikten. Bij de sham-dieren werd het instrument ingebracht maar bleven de draden intact, zodat hun kleppen normaal bleven functioneren.
Het hart vier weken zien aanpassen
Na de operatie kregen alle dieren zorgvuldige pijnstilling, antibiotica en, in de lekkagegroep, plastabletten om vochtophoping te verminderen. De varkens werden vier weken gevolgd, waarna het team de echo’s herhaalde en hartweefsel onder de microscoop bestudeerde. Bij elk varken met geïnduceerde lekkage bevestigden de beelden een zeer ernstig klepprobleem met een excentrische straal bloed die terug de boezem in schoot. Vergeleken met de sham-groep ontwikkelden deze varkens veel grotere boezems en kamers, zoals bleek uit duidelijke toename van de volumes van het linkeratrium en de linkerkamer aan het einde van zowel de vullings- als de samentrekkingsfasen van de hartcyclus. Tegelijkertijd zakten belangrijke maatstaven van pompfunctie, zoals de ejectiefractie en fractionele verkorting, sterk, wat aangeeft dat de harten al verzwakten.
Littekens in de spier en hoe dit model zich verhoudt
Weefselmonsters vertelden een vergelijkbaar verhaal. Harten die aan de kleplekkage waren blootgesteld hadden ongeveer twee keer zoveel vezelig, littekenachtig weefsel in de hoofd pompkamer vergeleken met sham-harten. Dit patroon — kameruitzetting, verminderde pompkracht en verhoogde fibrose — weerspiegelt de vroege stadia van menselijk hartfalen veroorzaakt door mitralisklepinsufficiëntie. Belangrijk is dat zowel mannelijke als vrouwelijke varkens vergelijkbare veranderingen lieten zien, en dat de lekkage sterk en uniform was bij bijna alle dieren, iets waar veel eerdere modellen moeite mee hadden. Omdat de methode alleen op de klepdraden gericht is en het blokkeren van kransslagaders vermijdt, isoleert zij de effecten van volume-overbelasting zonder de verwarrende schade van een hartinfarct.
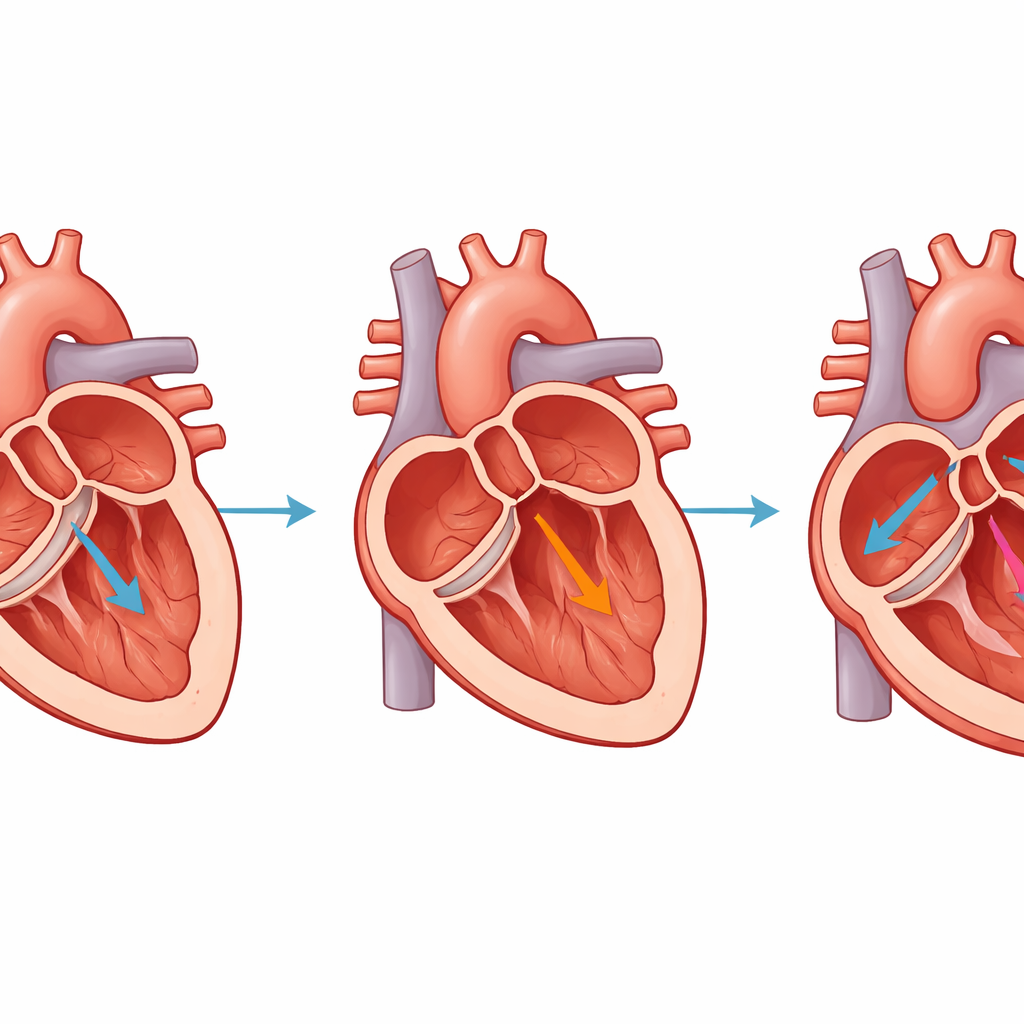
Wat dit betekent voor toekomstige behandelingen
Kort gezegd hebben de onderzoekers een betrouwbare manier ontwikkeld om varkensharten hetzelfde soort uitrekking, verzwakking en littekenvorming te laten doormaken dat menselijke harten ervaren wanneer een belangrijke klep ernstig lekt. Al binnen vier weken maken de dieren progressie naar een klinisch betekenisvolle fase van hartfalen die puur door chronische volume-overbelasting wordt aangedreven. Dit maakt het model bijzonder geschikt voor het testen van nieuwe beeldvormingstechnieken, medicijnen en apparaten die erop gericht zijn de klep te repareren of het hartspier te beschermen tegen langdurige schade. Door een schonere en beter gecontroleerde experimentele opzet te bieden, kan dit varkensmodel helpen het traject van laboratoriuminzichten naar therapieën die het leven van patiënten met klepgerelateerd hartfalen verbeteren, te versnellen.
Bronvermelding: Van Laer, S.L., Goovaerts, B., Laga, S. et al. A new technique inducing mitral valve regurgitation as an experimental porcine model of volume-overload induced heart failure. Sci Rep 16, 13500 (2026). https://doi.org/10.1038/s41598-026-43623-4
Trefwoorden: hartfalen, mitraliskleplek, diermodellen, varkenscardiologie, volume-overbelasting