Clear Sky Science · zh
负载miR-199a的金纳米颗粒对肝细胞癌的抗癌作用:体外研究
微小颗粒为何对肝癌重要
原发性肝癌,尤其是肝细胞癌,是全球最致命的癌症之一,常常在手术或常规治疗已难以取得良好效果时才被发现。本研究探讨了一个创新思路:使用超小的金颗粒作为“快递员”,将一种天然的抗癌分子运送进肝肿瘤细胞。对于读者来说,这提供了一个窗口,展示纳米技术与基因调控如何联手,开发更精确、毒性更低的癌症治疗方法。
让失落的保护因子重新发挥作用
许多肝肿瘤会沉默一种名为miR-199a的小型调控分子,在健康组织中它有助于控制细胞生长、迁移和存活。当miR-199a水平下降时,肿瘤细胞增殖加快、扩散更容易并且抗凋亡。恢复这一失落的保护因子可能将癌细胞推回更接近正常的行为,甚至诱导其自我毁灭。障碍在于miR-199a和其他脆弱的遗传信使一样,在体内易被降解,且难以自行进入细胞。
作为安全快递的金纳米颗粒
研究人员构建了一种由直径仅约15纳米的微小金球组成的递送载体——这比人类头发的宽度小数千倍。他们用一种柔性、生物相容的聚乙二醇(PEG)涂层对这些颗粒进行包覆,该涂层带有轻微的正电荷。这种涂层有助于颗粒在水性环境中保持稳定,并吸引带负电的miR-199a链,使其附着在颗粒表面。精细测量证实,加载后颗粒略微增大且表面电荷发生反转,这是miR-199a已牢固、稳定附着于金核的明确物理迹象。
进入癌细胞并将其关停
研究团队随后在培养的HepG2肝癌细胞上测试了这些miR-199a—金复合物。标准的细胞活力测试显示,裸金颗粒即使在相对较高剂量下也仅表现出轻度毒性,表明其基本安全性良好。相反,当相同的金颗粒负载miR-199a时,癌细胞存活率呈剂量和时间依赖性明显下降。在纳摩尔浓度下——远低于许多化疗药物的浓度——这些复合物在24至72小时内显著减少了存活细胞数量。流式细胞术(一种逐个计数并分类细胞的技术)显示,这种细胞丧失主要由凋亡驱动,即一种受控的细胞自杀,而非杂乱的毒性损伤。
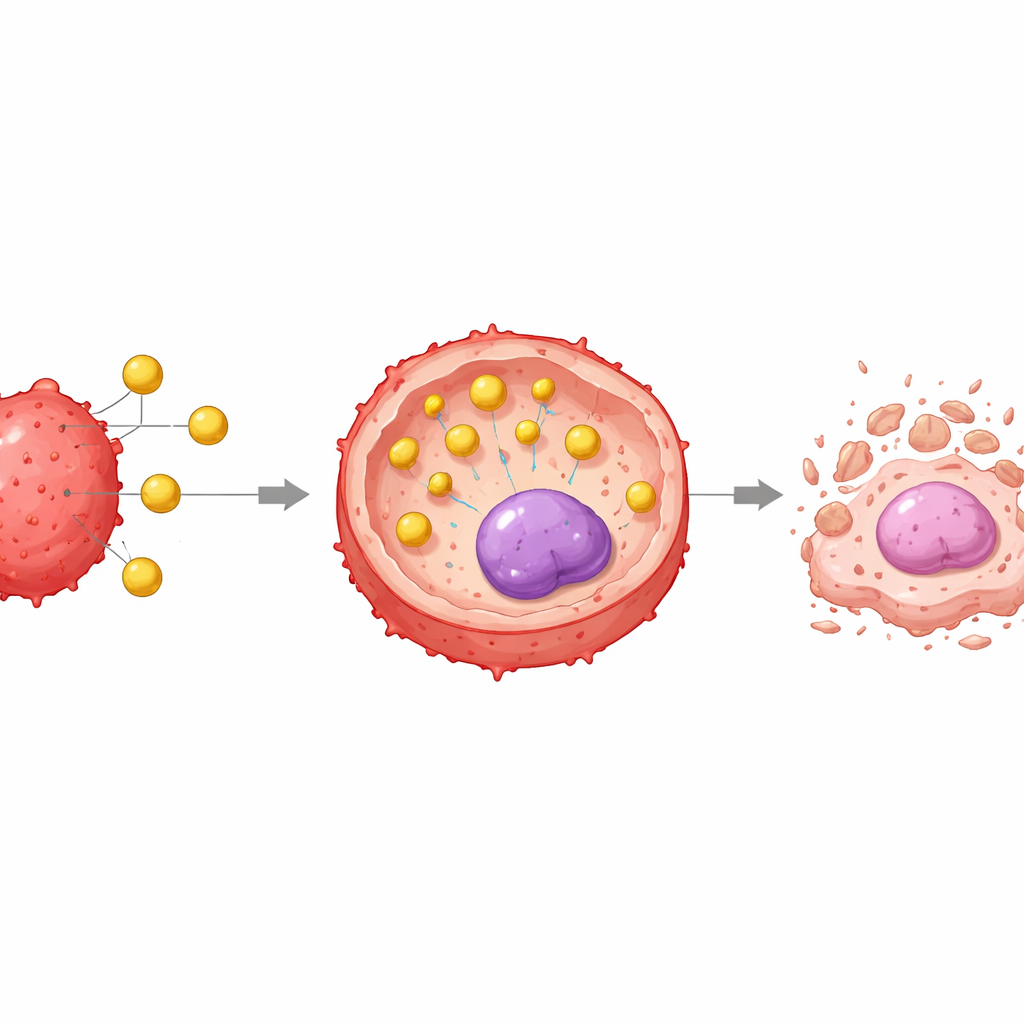
观察纳米颗粒的作用过程
为了确认其“快递系统”是否确实高效进入肿瘤细胞,科学家将miR-199a标记为红色荧光并用高分辨率显微镜跟踪。与仅有微弱细胞内信号的游离miR-199a不同,miR-199a—金复合物在细胞体内产生明亮且随时间增强的红色荧光,证实了强有力的摄取。电子显微镜更进一步,直观地捕捉到致密的金颗粒先聚集在细胞表面,随后出现在细胞质内被膜包裹的囊泡中,这与胞吞作用的摄取方式相符。与此同时,一个名为Ki-67的增殖标志物显著下降:在测试的最高剂量下,几乎所有细胞在24小时内停止分裂,表明该处理不仅能杀死细胞,还严重损害其增殖能力。
这对未来癌症治疗可能意味着什么
简言之,研究表明,经过工程化的微小金颗粒可以安全地将缺失的天然制动因子(miR-199a)送回肝癌细胞,在细胞内促使其走向自我毁灭并抑制生长——所需剂量非常小。虽然这些实验仅在细胞培养皿中进行,尚未在动物或人体中验证,但它们强调了一个有前景的方向:将稳定且可定制的纳米载体与特异性的基因调控因子结合,以更精确地攻击肿瘤,并有可能比传统药物产生更少的副作用。如果未来的动物和临床研究证实这些发现,这种金—miR-199a纳米复合物方法可能成为新一代高度靶向肝癌疗法的一部分。
引用: Achy, S.E., E. Moustafa, M., Fouad, M. et al. Anticarcinogenic effects of miR-199a-loaded gold nanoparticles on hepatocellular carcinoma: in vitro study. Sci Rep 16, 11357 (2026). https://doi.org/10.1038/s41598-026-42604-x
关键词: 肝癌, 金纳米颗粒, 微RNA疗法, 纳米医学, 靶向药物递送