Clear Sky Science · pl
Antykancerogenne działanie nanocząstek złota niosących miR-199a w raku wątrobowokomórkowym: badanie in vitro
Dlaczego drobne cząstki mają znaczenie w raku wątroby
Pierwotny rak wątroby, a w szczególności rak wątrobowokomórkowy, jest jednym z najgroźniejszych nowotworów na świecie i często wykrywany zbyt późno, by zabieg chirurgiczny lub standardowe terapie były skuteczne. W pracy tej badano pomysł użycia ultramałych cząstek złota jako „kurierów” do przemycenia naturalnej cząsteczki przeciwnowotworowej do komórek guza wątroby. Dla czytelników daje to wgląd w to, jak nanotechnologia i regulacja genetyczna mogą połączyć siły, by stworzyć precyzyjniejsze, mniej toksyczne terapie przeciwnowotworowe.
Przywrócenie utraconego strażnika
Wiele guzów wątroby wycisza małą molekułę regulatorową zwaną miR-199a, która w zdrowych tkankach pomaga kontrolować wzrost komórek, ich ruchliwość i przetrwanie. Gdy poziom miR-199a spada, komórki nowotworowe mnożą się szybciej, łatwiej się rozprzestrzeniają i stają się odporne na śmierć. Przywrócenie tego utraconego strażnika może skłonić komórki nowotworowe do powrotu w stronę normalnego zachowania lub nawet wywołać ich samozniszczenie. Problem polega na tym, że miR-199a, podobnie jak inne kruche przekaźniki genetyczne, jest szybko rozkładana w organizmie i ma trudności z samodzielnym przeniknięciem do wnętrza komórek.
Nanocząstki złota jako bezpieczni kurierzy
Naukowcy zbudowali nośnik z maleńkich złotych kulek o średnicy około 15 nanometrów — tysiące razy mniejszych niż grubość włosa. Pokryli te cząstki elastyczną, biokompatybilną warstwą polietylenu glikolu (PEG) niosącą lekko dodatni ładunek. Powłoka ta pomaga cząstkom zachować stabilność w środowisku wodnym i przyciąga ujemnie naładowane nici miR-199a, które mogą przylgnąć do powierzchni cząstek. Dokładne pomiary potwierdziły, że po załadowaniu cząstki stały się nieco większe, a ich ładunek powierzchniowy odwrócił się — jasne fizyczne oznaki, że miR-199a przyłączyła się pewnie i stabilnie do złotych rdzeni.
Wnikanie do komórek nowotworowych i ich wyłączanie
Zespół następnie przetestował te kompleksy miR-199a–złoto na hodowanych komórkach raka wątroby HepG2. Standardowe testy żywotności komórek wykazały, że gołe cząstki złota same w sobie były tylko słabo szkodliwe, nawet przy relatywnie wysokich dawkach, co wskazuje na dobrą podstawową tolerancję. Natomiast gdy te same cząstki złota były załadowane miR-199a, przeżywalność komórek nowotworowych gwałtownie spadała w sposób zależny od dawki i czasu. Przy stężeniach nanomolowych — znacznie niższych niż wiele chemioterapeutyków — kompleksy istotnie zmniejszały liczbę żywych komórek w ciągu 24 do 72 godzin. Cytometria przepływowa, technika zliczająca i klasyfikująca pojedyncze komórki, wykazała, że ten spadek wynikał głównie z apoptozy, kontrolowanej formy samobójczej śmierci komórkowej, a nie ze spektakularnego uszkodzenia toksycznego.
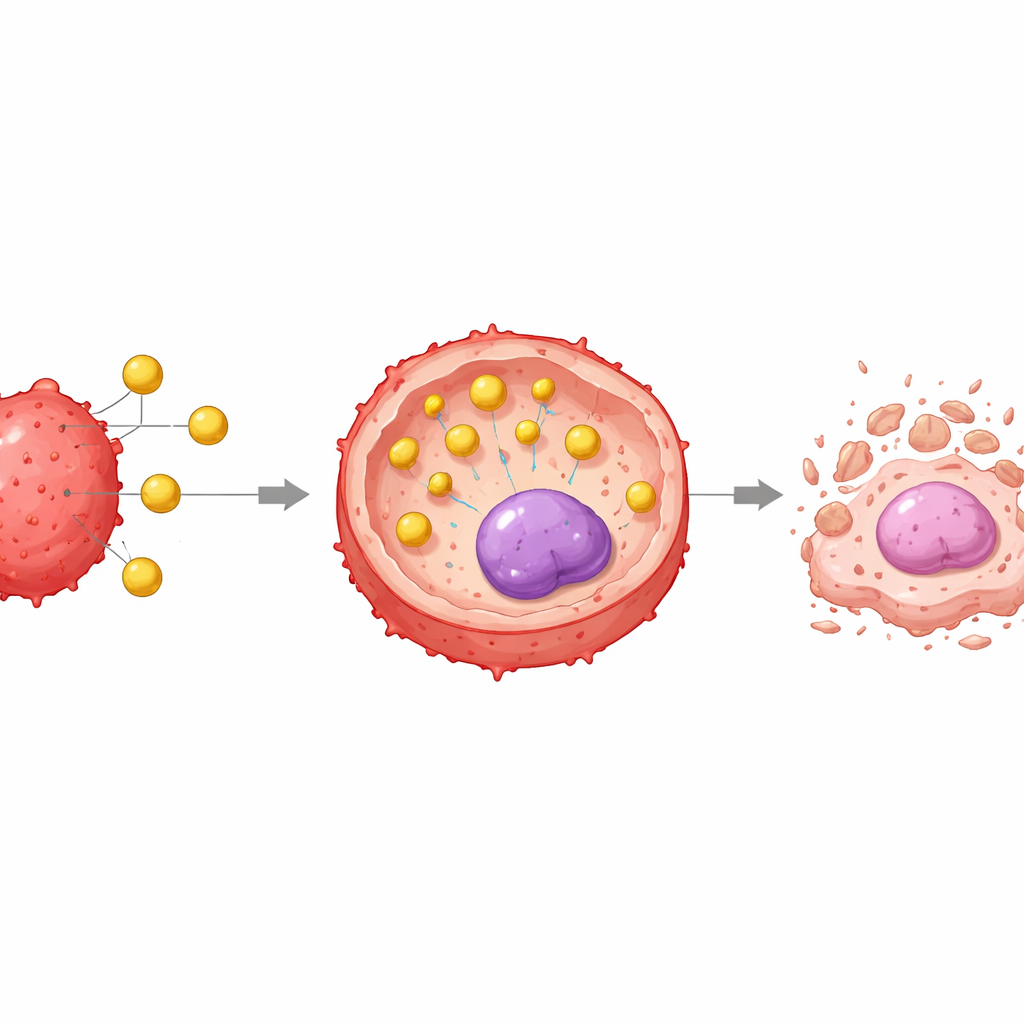
Obserwacja nanocząstek w działaniu
Aby sprawdzić, czy ich system kurierski faktycznie efektywnie wchodzi do komórek guza, naukowcy znakowali miR-199a czerwonym markerem fluorescencyjnym i śledzili go za pomocą mikroskopii o wysokiej rozdzielczości. Podczas gdy wolna miR-199a dawała jedynie słabe sygnały wewnątrz komórek, kompleksy miR-199a–złoto generowały jasne, narastające czerwone poświaty w obrębie ciała komórkowego w czasie, potwierdzając intensywne pobieranie. Mikroskopia elektronowa poszła krok dalej, wizualnie uchwyciła gęste cząstki złota skupione najpierw na powierzchni komórek, a później wewnątrz pęcherzyków ograniczonych błoną w cytoplazmie, co jest zgodne z pobieraniem przez endocytozę. Równocześnie znacznik proliferacji Ki-67 spadł dramatycznie: przy najwyższej testowanej dawce nanokompleksu niemal wszystkie komórki przestały dzielić się w ciągu 24 godzin, pokazując, że leczenie nie tylko zabijało komórki, lecz także unieruchamiało ich zdolność do mnożenia.
Co to może oznaczać dla przyszłej opieki onkologicznej
Mówiąc prosto, badanie pokazuje, że maleńkie, zaprojektowane cząstki złota mogą bezpiecznie dostarczyć brakującą naturalną blokadę (miR-199a) z powrotem do komórek raka wątroby, gdzie pomaga skłonić je do samozniszczenia i zatrzymuje ich wzrost — przy użyciu zaskakująco małych dawek. Chociaż eksperymenty przeprowadzono jedynie na hodowlach komórkowych, a nie jeszcze na zwierzętach czy ludziach, wskazują one obiecujący kierunek: łączenie stabilnych, modyfikowalnych nanonośników z konkretnymi regulatorami genetycznymi, aby atakować guzy precyzyjniej i potencjalnie z mniejszą liczbą skutków ubocznych niż tradycyjne leki. Jeśli przyszłe badania na zwierzętach i w badaniach klinicznych potwierdzą te wyniki, podejście z nanokompleksem złoto–miR-199a mogłoby stać się częścią nowej generacji wysoce ukierunkowanych terapii raka wątroby.
Cytowanie: Achy, S.E., E. Moustafa, M., Fouad, M. et al. Anticarcinogenic effects of miR-199a-loaded gold nanoparticles on hepatocellular carcinoma: in vitro study. Sci Rep 16, 11357 (2026). https://doi.org/10.1038/s41598-026-42604-x
Słowa kluczowe: rak wątroby, nanocząstki złota, terapia mikroRNA, nanomedycyna, celowane dostarczanie leków