Clear Sky Science · fr
Effets anticarcinogènes de nanoparticules d'or chargées en miR-199a sur le carcinome hépatocellulaire : étude in vitro
Pourquoi les particules minimes comptent pour le cancer du foie
Le cancer hépatique primaire, en particulier le carcinome hépatocellulaire, fait partie des cancers les plus mortels au monde et est souvent diagnostiqué trop tard pour que la chirurgie ou les traitements standards soient vraiment efficaces. Cette étude explore une idée inventive : utiliser de très petites particules d'or comme « coursiers » pour introduire une molécule naturelle anticancéreuse dans les cellules tumorales du foie. Pour le lecteur, elle offre un aperçu de la manière dont la nanotechnologie et la régulation génétique pourraient s'associer pour créer des thérapies contre le cancer plus précises et moins toxiques.
Réanimer un protecteur disparu
De nombreuses tumeurs hépatiques mettent hors circuit une petite molécule régulatrice appelée miR-199a, qui, dans un tissu sain, aide à contrôler la croissance, la migration et la survie cellulaires. Quand les niveaux de miR-199a chutent, les cellules tumorales prolifèrent plus rapidement, envahissent plus facilement et résistent à la mort. Restaurer ce protecteur perdu pourrait ramener les cellules cancéreuses vers un comportement plus normal ou même déclencher leur autodestruction. L'obstacle est que la miR-199a, comme d'autres messagers génétiques fragiles, est rapidement dégradée dans l'organisme et peine à pénétrer dans les cellules par elle-même.
Les nanoparticules d'or comme coursiers sûrs
Les chercheurs ont construit un vecteur de livraison à partir de minuscules sphères d'or d'environ 15 nanomètres de diamètre — des milliers de fois plus fines qu'un cheveu humain. Ils ont recouvert ces particules d'une couche flexible et biocompatible de polyéthylène glycol (PEG) portant une légère charge positive. Ce revêtement aide les particules à rester stables en milieu aqueux et attire les brins négativement chargés de miR-199a, qui peuvent alors se fixer à la surface des particules. Des mesures soigneuses ont confirmé qu'après chargement, les particules devenaient légèrement plus grosses et que leur charge de surface s'inversait, signes physiques clairs que la miR-199a s'était attachée de façon stable et sécurisée aux noyaux d'or.
Pénétrer les cellules cancéreuses et les neutraliser
L'équipe a ensuite testé ces complexes miR-199a–or sur des cellules cancéreuses hépatiques HepG2 en culture. Des tests standard de viabilité cellulaire ont montré que les particules d'or nues étaient seulement faiblement toxiques, même à des doses relativement élevées, ce qui indique une bonne sécurité de base. En revanche, lorsque ces mêmes particules étaient chargées en miR-199a, la survie des cellules cancéreuses chutait fortement, de façon dépendante de la dose et du temps. À des concentrations nanomolaires — bien inférieures à celles de nombreux chimiothérapies — les complexes réduisaient significativement le nombre de cellules vivantes sur 24 à 72 heures. La cytométrie en flux, technique qui compte et classe les cellules une par une, a révélé que cette perte était principalement due à l'apoptose, une forme contrôlée de suicide cellulaire, plutôt qu'à un dommage toxique désordonné.
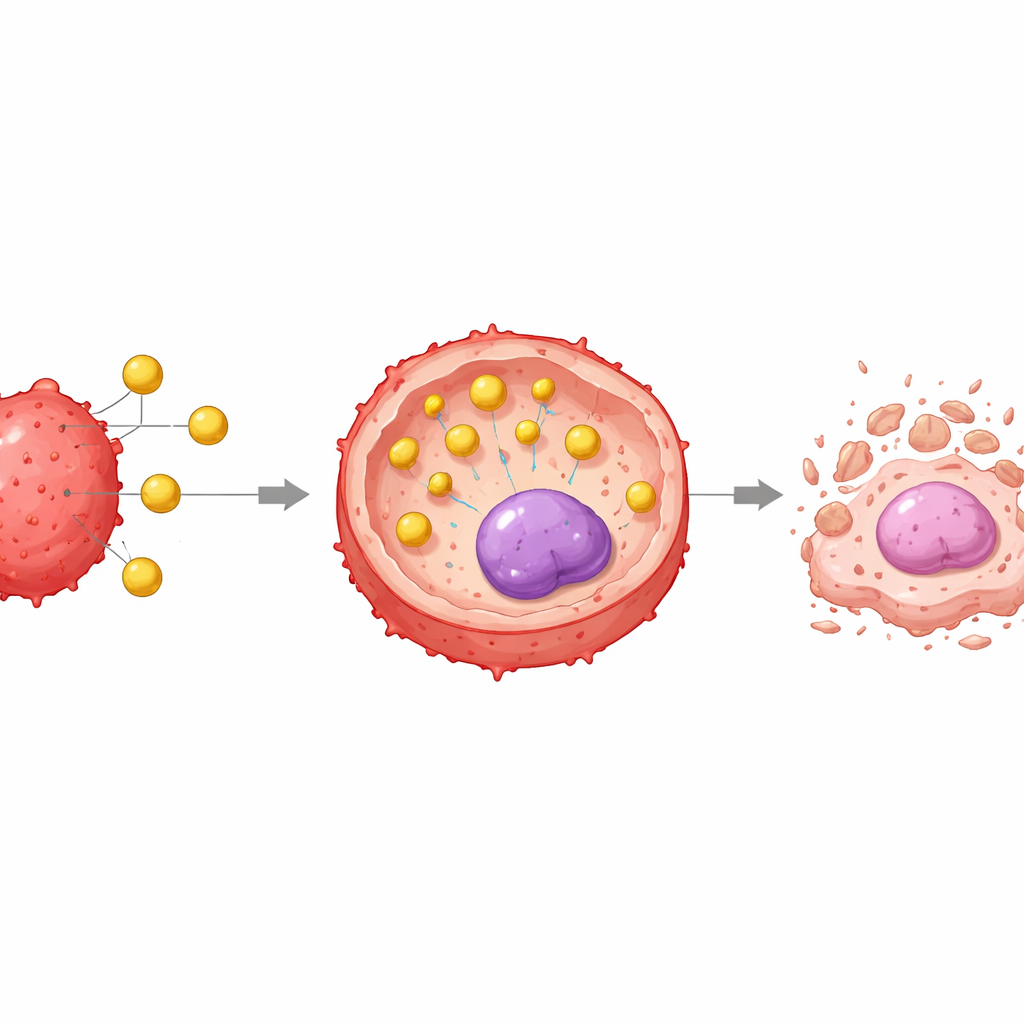
Observer les nanoparticules en action
Pour vérifier si leur système de livraison pénétrait vraiment efficacement dans les cellules tumorales, les scientifiques ont marqué la miR-199a par une sonde fluorescente rouge et l'ont suivie au microscope haute résolution. Alors que la miR-199a libre produisait des signaux faibles à l'intérieur des cellules, les complexes miR-199a–or généraient des lueurs rouges intenses et croissantes dans le corps cellulaire au fil du temps, confirmant une uptake robuste. La microscopie électronique est allée plus loin en capturant visuellement des particules denses d'or regroupées d'abord à la surface cellulaire, puis à l'intérieur de sacs entourés de membrane dans le cytoplasme, compatible avec une internalisation par endocytose. Dans le même temps, un marqueur de prolifération appelé Ki-67 chutait de façon spectaculaire : à la dose maximale testée du nanocomplexe, presque toutes les cellules avaient cessé de se diviser en 24 heures, montrant que le traitement tuait les cellules et paralysait aussi leur capacité à se multiplier.
Ce que cela pourrait signifier pour les soins oncologiques futurs
En termes simples, l'étude montre que de minuscules particules d'or conçues peuvent transporter sans danger un frein naturel manquant (miR-199a) dans les cellules du cancer du foie, où il aide à les pousser vers l'autodestruction et à arrêter leur croissance — et ce à des doses remarquablement faibles. Bien que ces expériences aient été réalisées uniquement sur des cultures cellulaires, pas encore sur des animaux ou des humains, elles mettent en lumière une piste prometteuse : combiner des nanovecteurs stables et personnalisables avec des régulateurs génétiques spécifiques pour attaquer les tumeurs de façon plus précise et potentiellement avec moins d'effets secondaires que les traitements traditionnels. Si des études animales et cliniques ultérieures confirment ces résultats, l'approche nanocomplexe or–miR-199a pourrait devenir partie intégrante d'une nouvelle génération de thérapies ciblées contre le cancer du foie.
Citation: Achy, S.E., E. Moustafa, M., Fouad, M. et al. Anticarcinogenic effects of miR-199a-loaded gold nanoparticles on hepatocellular carcinoma: in vitro study. Sci Rep 16, 11357 (2026). https://doi.org/10.1038/s41598-026-42604-x
Mots-clés: cancer du foie, nanoparticules d'or, thérapie par microARN, nanomédecine, libération ciblée de médicaments