Clear Sky Science · zh
核酸酶 EXO1 通过降解新生 DNA 在 BRCA 完整的细胞中促进基因组不稳定性
当 DNA 修复变得危险
我们的细胞不断复制并修复它们的 DNA,依靠一群通常被视为抗癌卫士的酶。本研究揭示,这些卫士之一——名为 EXO1 的酶——在过量存在时可能变成麻烦制造者。在许多肿瘤中,EXO1 被过度激活,而不是安静地协助修复,它会啃噬新合成的 DNA 链,留下危险的断裂,这些断裂既可能助长癌症发展,也可能使这类肿瘤对某些药物更为敏感。 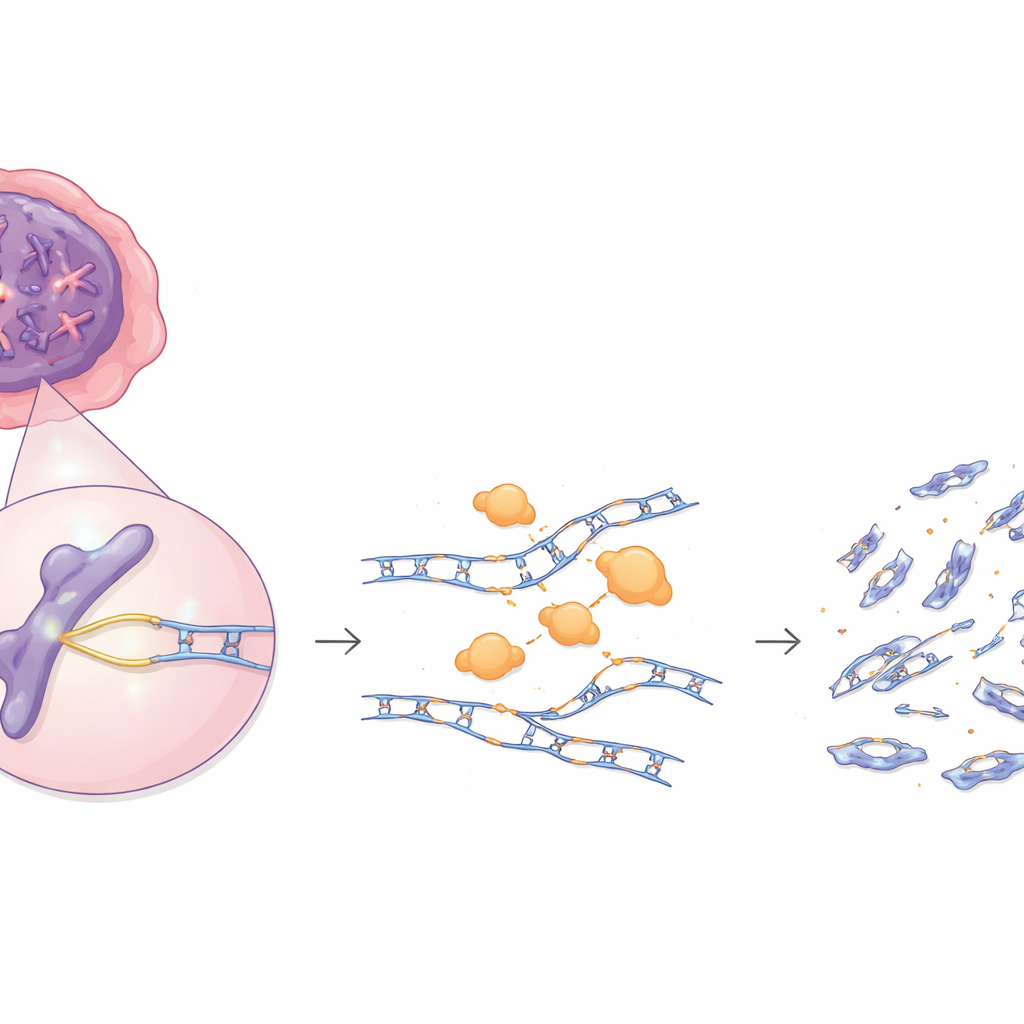
让 DNA 复制保持正轨
每当细胞分裂时,必须复制其 DNA。这个称为复制的过程由一个沿双螺旋移动的分子机器完成,产生两条新的子链。在癌细胞中,这一复制过程常常承受压力:DNA 的构建模块可能短缺,或复制机器可能遇到由损伤或化疗引起的化学阻碍。通常,细胞会使用后备策略来应对——暂停并重启复制机器,或跳过障碍并在稍后填补缺口——同时修复系统修补任何易受损的单链 DNA 区域,以防它们演变成完整断裂。
过度活跃的“有益”酶
EXO1 是参与修复时修整 DNA 的清理酶之一。在正常情况下,它会啃回 DNA 末端,以便其他蛋白能够准确地恢复断裂的链。作者首先分析了大型癌症数据库,发现包括乳腺癌、肝癌、皮肤癌、睾丸癌和宫颈癌在内的多种肿瘤中,EXO1 经常以异常高的水平存在。与许多作为肿瘤抑制的修复基因被丢失不同,EXO1 是被扩增或过度表达的。EXO1 增多的肿瘤倾向于表现出更多大尺度的 DNA 变化,如染色体的增减和重排,这一模式暗示基因组不稳定性的增加。
过量 EXO1 如何损伤新生 DNA
为了解 EXO1 过量在细胞内实际造成什么,研究人员让仍保有完整 BRCA 修复通路的癌细胞系额外表达 EXO1。当他们随后用减慢 DNA 复制或在 DNA 上产生化学加合物的药物对这些细胞施加复制压力时,发现在最近复制的区域出现了更多 DNA 损伤。详尽的单分子检测显示,过量的 EXO1 会在新合成的链上产生缺口,并在复制叉因停滞而折叠成四向“反向”结构时啃回 DNA。关键是,这种破坏性行为依赖于 EXO1 的切割活性;不能切割 DNA 的酶变体并不会产生这些效应。 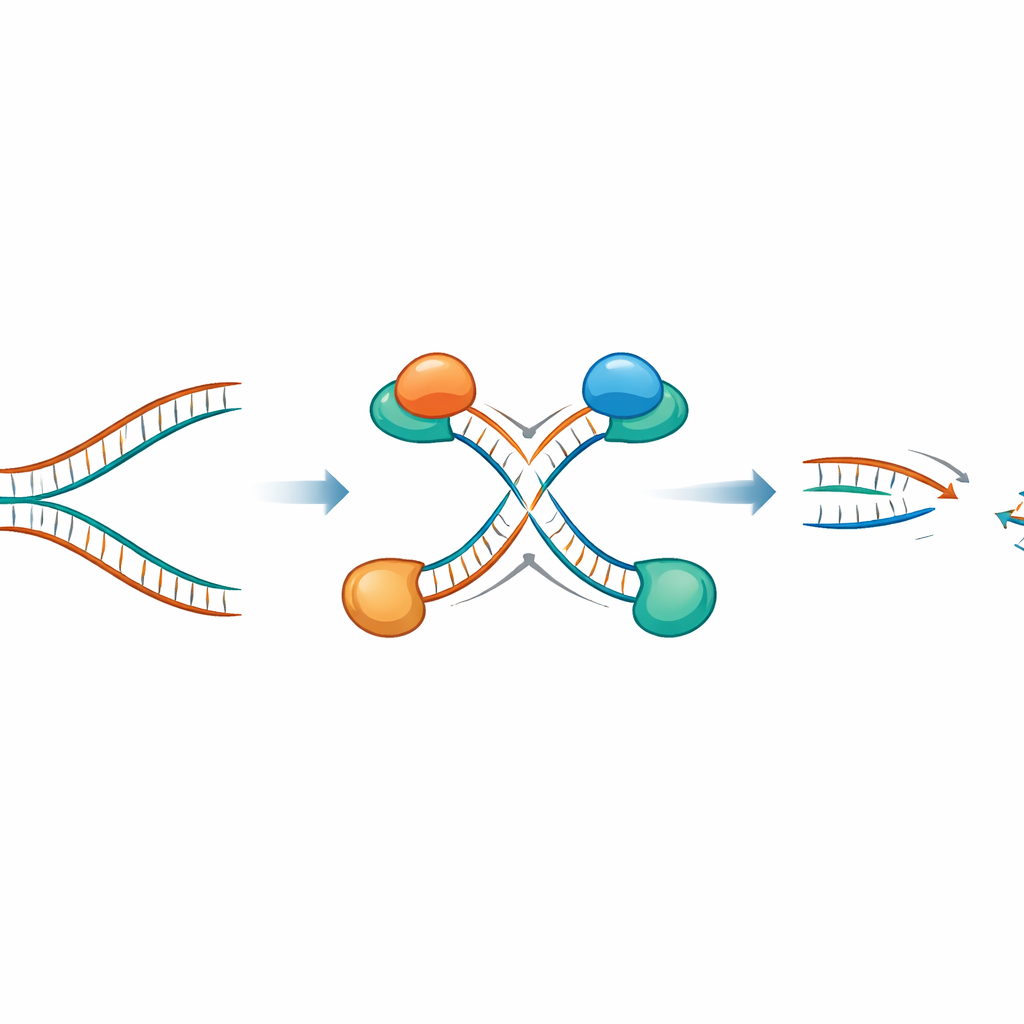
破坏性的协同与断裂的染色体
研究小组接着探查 EXO1 如何与另一种核酸酶 MRE11 协作。通过显微镜邻近性检测,他们发现过量的 EXO1 将 MRE11 招募到新合成的 DNA 上,存在于缺口和反向复制叉处,形成成对的切割装置,从相对方向攻击两条链。即便细胞仍具有正常工作的 BRCA 蛋白(通常保护停滞的复制叉),EXO1 与 MRE11 的联合作用也压倒了这种保护机制。结果是新生 DNA 被广泛降解,缺口和停滞的复制叉被转化为双链断裂,并且染色体结构损伤显著增加。
从基因组混乱到药物敏感性
尽管这些损伤促进了可推动癌症进化的基因组混乱,但它们也暴露出一个阿基里斯之踵。EXO1 过量的细胞对顺铂(一种在 DNA 上产生大块损伤的化疗药物)和 PARP 抑制剂(已在缺乏 BRCA 功能的肿瘤中表现良好的药物)表现出高度敏感。事实上,EXO1 富集细胞的药物反应类似于直接存在 BRCA 缺陷的细胞,这种状态常被称为“类 BRCA”。对非专业读者而言,这意味着即使没有著名 BRCA 基因的突变,过度表达 EXO1 的肿瘤也表现得像 BRCA 缺陷:其 DNA 更脆弱,更容易被加重复制压力的治疗推向崩溃,提示 EXO1 水平可能作为指导治疗选择的生物标志物。
引用: Nusawardhana, A., Nicolae, C.M. & Moldovan, GL. The nuclease EXO1 promotes genomic instability by degrading nascent DNA in BRCA-proficient cells. Nat Commun 17, 3169 (2026). https://doi.org/10.1038/s41467-026-69981-1
关键词: DNA 修复, 基因组不稳定性, BRCA 通路, 癌症化疗, EXO1 核酸酶