Clear Sky Science · de
Die Nuclease EXO1 fördert genomische Instabilität, indem sie naszierende DNA in BRCA-funktionstüchtigen Zellen abbaut
Wenn DNA-Reparatur riskant wird
Unsere Zellen kopieren und reparieren ständig ihre DNA und nutzen dafür eine Reihe von Enzymen, die normalerweise als Wächter gegen Krebs fungieren. Diese Studie zeigt, dass einer dieser Wächter, ein Enzym namens EXO1, zum Störenfried werden kann, wenn es im Übermaß vorhanden ist. In vielen Tumoren ist EXO1 übermäßig aktiviert und statt ruhig bei Reparaturen zu helfen, frisst es in neu synthetisierte DNA-Stränge hinein und hinterlässt gefährliche Brüche, die die Krebsentwicklung antreiben können – zugleich macht das solche Tumoren möglicherweise anfälliger für bestimmte Medikamente. 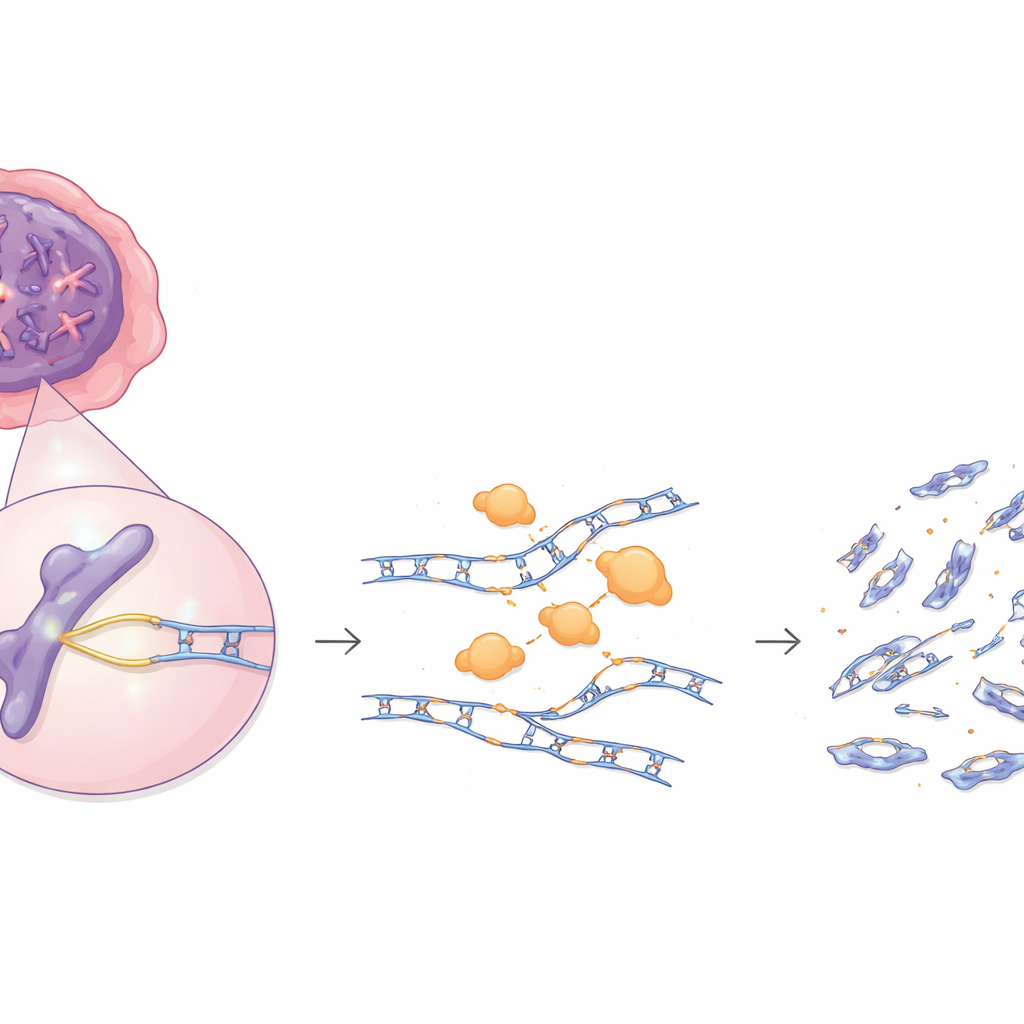
Die DNA-Replikation auf Kurs halten
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre DNA verdoppeln. Dieser Prozess, bekannt als Replikation, wird von einer beweglichen molekularen Maschine ausgeführt, die sich entlang der Doppelhelix bewegt und zwei neue Tochterstränge erzeugt. In Krebszellen ist dieser Kopiervorgang oft unter Stress: Bausteine für die DNA können knapp werden, oder die Maschinerie stößt auf chemische Hindernisse durch Schäden oder Chemotherapie. Normalerweise nutzen Zellen Backup-Strategien – sie pausieren und starten die Kopiermaschine neu oder überspringen Hindernisse und füllen Lücken später auf –, während Reparatursysteme anfällige Regionen mit einzelsträngiger DNA abdecken, damit diese nicht zu vollständigen Brüchen werden.
Ein hilfreiches Enzym auf Überdrehung
EXO1 ist eines der Aufräumenzyme, das DNA bei der Reparatur kürzt. Unter üblichen Bedingungen knabbert es DNA-Enden zurück, damit andere Proteine gebrochene Stränge präzise wiederherstellen können. Die Autorinnen und Autoren haben zunächst große Krebsdatensätze untersucht und festgestellt, dass EXO1 in mehreren Tumorarten – darunter Brust-, Leber-, Haut-, Hoden- und Gebärmutterhalskrebs – häufig in ungewöhnlich hohen Mengen vorkommt. Statt wie viele tumorunterdrückende Reparaturgene verloren zu gehen, ist EXO1 verstärkt vorhanden oder überexprimiert. Tumoren mit erhöhtem EXO1 zeigen tendenziell größere DNA-Veränderungen wie Gewinn, Verlust und Umlagerung von Chromosomen, ein Muster, das auf gesteigerte genomische Instabilität hinweist.
Wie überschüssiges EXO1 neue DNA schädigt
Um zu sehen, was eine Überfülle an EXO1 tatsächlich in Zellen bewirkt, veranlassten die Forschenden Krebszelllinien mit intaktem BRCA-Reparaturweg, zusätzliches EXO1 zu produzieren. Setzten sie diese Zellen dann Replikationsstress aus – durch Medikamente, die das DNA-Kopieren verlangsamen oder chemische Addukte auf der DNA erzeugen – beobachteten sie mehr DNA-Schäden speziell in kürzlich replizierten Bereichen. Detaillierte Einzelmolekül-Assays zeigten, dass überschüssiges EXO1 Lücken in frisch gebildeten Strängen verursacht und außerdem an Replikationsgabeln nagt, die während des Stillstands in eine vierarmige „reversierte“ Form gefaltet sind. Entscheidend war, dass dieses zerstörerische Verhalten die Schneideaktivität von EXO1 erforderte; eine Variante des Enzyms, die DNA nicht spalten kann, erzeugte diese Effekte nicht. 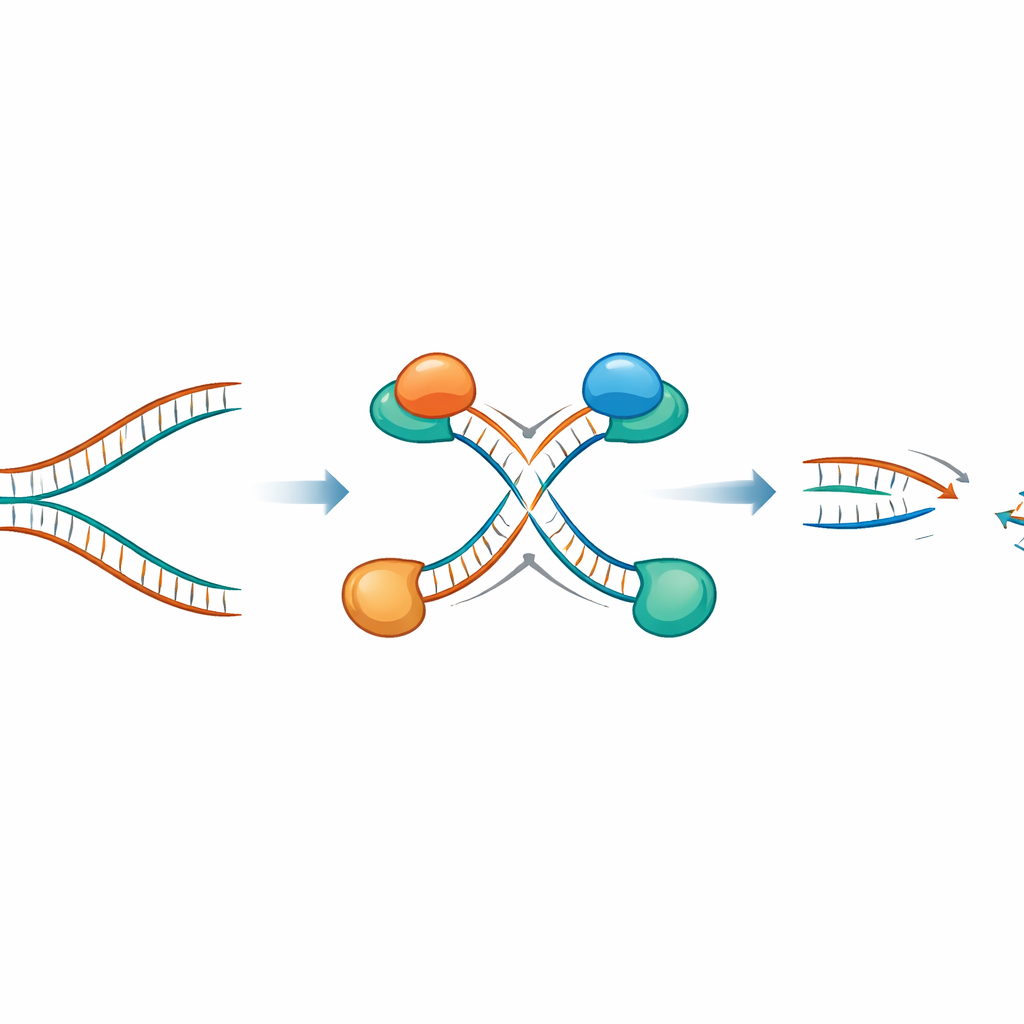
Eine destruktive Zusammenarbeit und gebrochene Chromosomen
Das Team untersuchte anschließend, wie EXO1 mit einer anderen Nuclease, MRE11, zusammenarbeitet. Mithilfe mikroskopischer Proximitätsassays fanden sie heraus, dass überschüssiges EXO1 MRE11 auf neu synthetisierte DNA an sowohl Lücken als auch reversierten Gabeln anzieht und gepaarte Schneidemaschinen bildet, die die beiden Stränge aus entgegengesetzten Richtungen angreifen. Obwohl die Zellen weiterhin funktionierende BRCA-Proteine besaßen, die normalerweise stillstehende Gabeln schützen, überwältigte die kombinierte Wirkung von EXO1 und MRE11 diesen Schutz. Das Ergebnis war eine weitverbreitete Degradation naszierender DNA, die Umwandlung von Lücken und gestoppten Gabeln in Doppelstrangbrüche und ein deutlicher Anstieg struktureller Chromosomenschäden.
Von genomischem Chaos zur Medikamentenempfindlichkeit
Obwohl diese Schäden die Art von genomischem Chaos fördern, die die Krebsentwicklung vorantreiben kann, schaffen sie gleichzeitig eine Achillesferse. Zellen mit zu viel EXO1 waren hypersensitiv gegenüber Cisplatin, einem Chemotherapeutikum, das sperrige Läsionen in die DNA einbaut, und gegenüber PARP-Inhibitoren, Medikamenten, die bereits bei Tumoren mit BRCA-Defekten wirksam sind. Tatsächlich ähnelten die Arzneimittelantworten von EXO1-reichen Zellen denen von Zellen mit direkten BRCA-Defekten, einem Zustand, der oft als „BRCAness“ bezeichnet wird. Für Laien bedeutet das: Selbst ohne Mutationen in den bekannten BRCA-Genen verhalten sich Tumoren, die EXO1 hochfahren, wie BRCA-defiziente Tumoren – ihre DNA ist fragil und lässt sich durch Therapien, die die Replikation belasten, leicht ins Verderben treiben. Das legt nahe, dass EXO1-Spiegel als Biomarker dienen könnten, um Therapieentscheidungen zu lenken.
Zitation: Nusawardhana, A., Nicolae, C.M. & Moldovan, GL. The nuclease EXO1 promotes genomic instability by degrading nascent DNA in BRCA-proficient cells. Nat Commun 17, 3169 (2026). https://doi.org/10.1038/s41467-026-69981-1
Schlüsselwörter: DNA-Reparatur, genomische Instabilität, BRCA-Weg, Krebschemotherapie, EXO1-Nuclease