Clear Sky Science · fr
La nucléase EXO1 favorise l’instabilité génomique en dégradant l’ADN naissant dans des cellules compétentes pour BRCA
Quand la réparation de l’ADN devient risquée
Nos cellules copient et réparent en permanence leur ADN à l’aide d’un ensemble d’enzymes qui agissent habituellement comme des gardiens contre le cancer. Cette étude montre que l’un de ces gardiens, une enzyme nommée EXO1, peut se transformer en perturbateur lorsqu’elle est présente en excès. Dans de nombreuses tumeurs, EXO1 est trop fortement activée et, au lieu d’aider discrètement à la réparation, elle ronge les brins d’ADN nouvellement synthétisés, laissant derrière elle des cassures dangereuses susceptibles de favoriser le développement tumoral — mais qui peuvent aussi rendre ces tumeurs plus sensibles à certains médicaments. 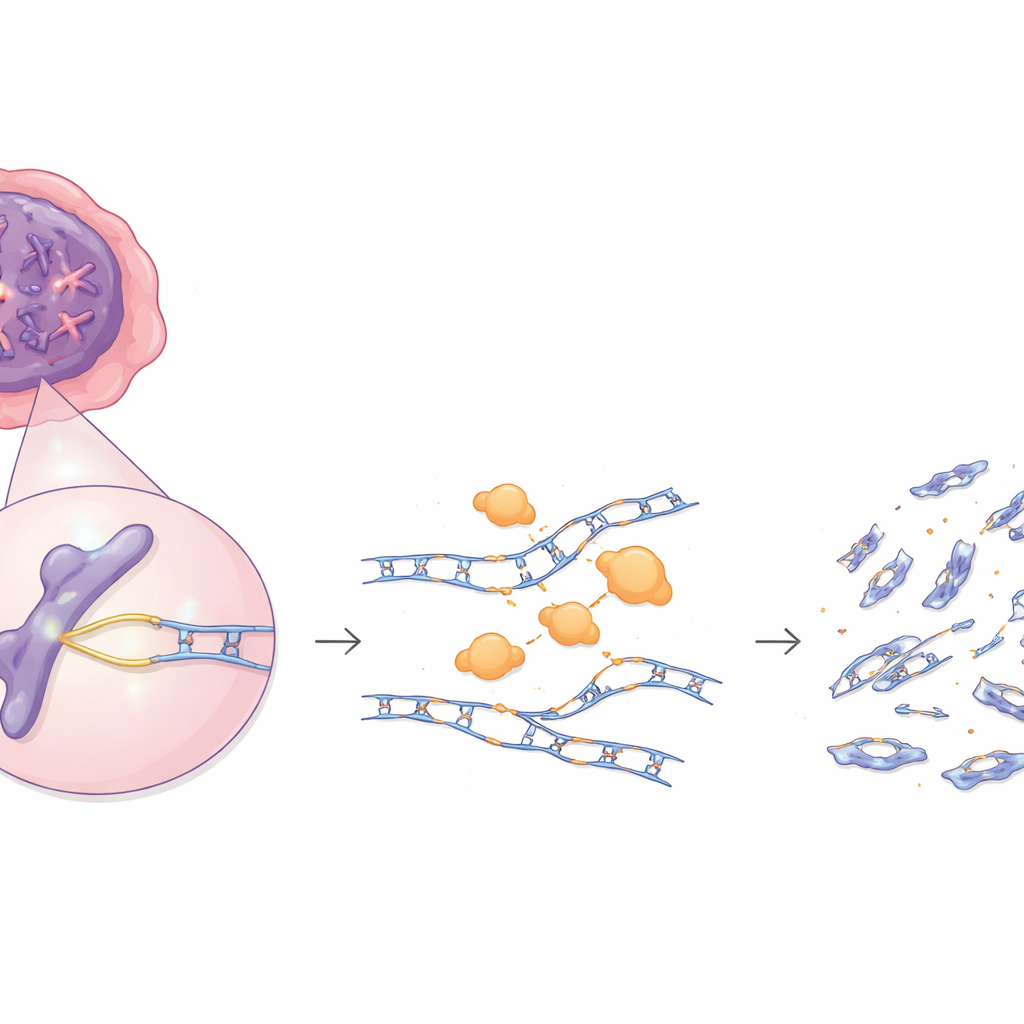
Maintenir la copie de l’ADN sur la bonne voie
À chaque division, une cellule doit dupliquer son ADN. Ce processus, appelé réplication, est assuré par une machine moléculaire en mouvement qui parcourt la double hélice et crée deux nouveaux brins filles. Dans les cellules cancéreuses, ce processus de copie est souvent mis à l’épreuve : les précurseurs de l’ADN peuvent se raréfier ou la machinerie peut rencontrer des obstacles chimiques dus à des lésions ou à la chimiothérapie. En temps normal, les cellules mobilisent des stratégies de secours — mettre la réplication en pause et la relancer, ou sauter des obstacles puis combler les lacunes — tandis que les systèmes de réparation protègent les segments monocaténaires vulnérables pour qu’ils ne se transforment pas en cassures complètes.
Une enzyme utile en surrégime
EXO1 fait partie des enzymes de nettoyage qui élaguent l’ADN lors de la réparation. Dans des conditions normales, elle rogne les extrémités d’ADN pour permettre à d’autres protéines de restaurer précisément les brins cassés. Les auteurs ont d’abord examiné de larges jeux de données tumorales et constaté que, dans plusieurs types de tumeurs — notamment du sein, du foie, de la peau, des testicules et du col de l’utérus — EXO1 est fréquemment présente à des niveaux anormalement élevés. Plutôt que d’être perdue, comme c’est le cas pour de nombreux gènes suppresseurs de tumeur impliqués dans la réparation, EXO1 est amplifiée ou surexprimée. Les tumeurs riches en EXO1 tendent à présenter davantage d’altérations d’envergure du génome, telles que des gains, pertes et réarrangements chromosomiques, un schéma qui suggère une instabilité génomique accrue.
Comment l’excès d’EXO1 endommage l’ADN nouvellement synthétisé
Pour savoir ce que entraîne réellement la surabondance d’EXO1 dans les cellules, les chercheurs ont forcé des lignées cancéreuses possédant encore une voie BRCA intacte à produire de l’EXO1 en excès. Lorsqu’ils ont soumis ces cellules à un stress de réplication à l’aide de médicaments ralentissant la copie de l’ADN ou provoquant des adduits chimiques sur l’ADN, ils ont observé davantage de lésions d’ADN spécifiquement dans les régions récemment répliquées. Des essais détaillés au niveau des molécules individuelles ont montré que l’excès d’EXO1 crée des lacunes dans les brins fraîchement synthétisés et ronge également l’ADN aux fourches de réplication qui se replient en une structure « inversée » à quatre branches lors du blocage. De façon cruciale, ce comportement destructeur dépendait de l’activité de clivage d’EXO1 ; une version de l’enzyme incapable de couper l’ADN n’engendrait pas ces effets. 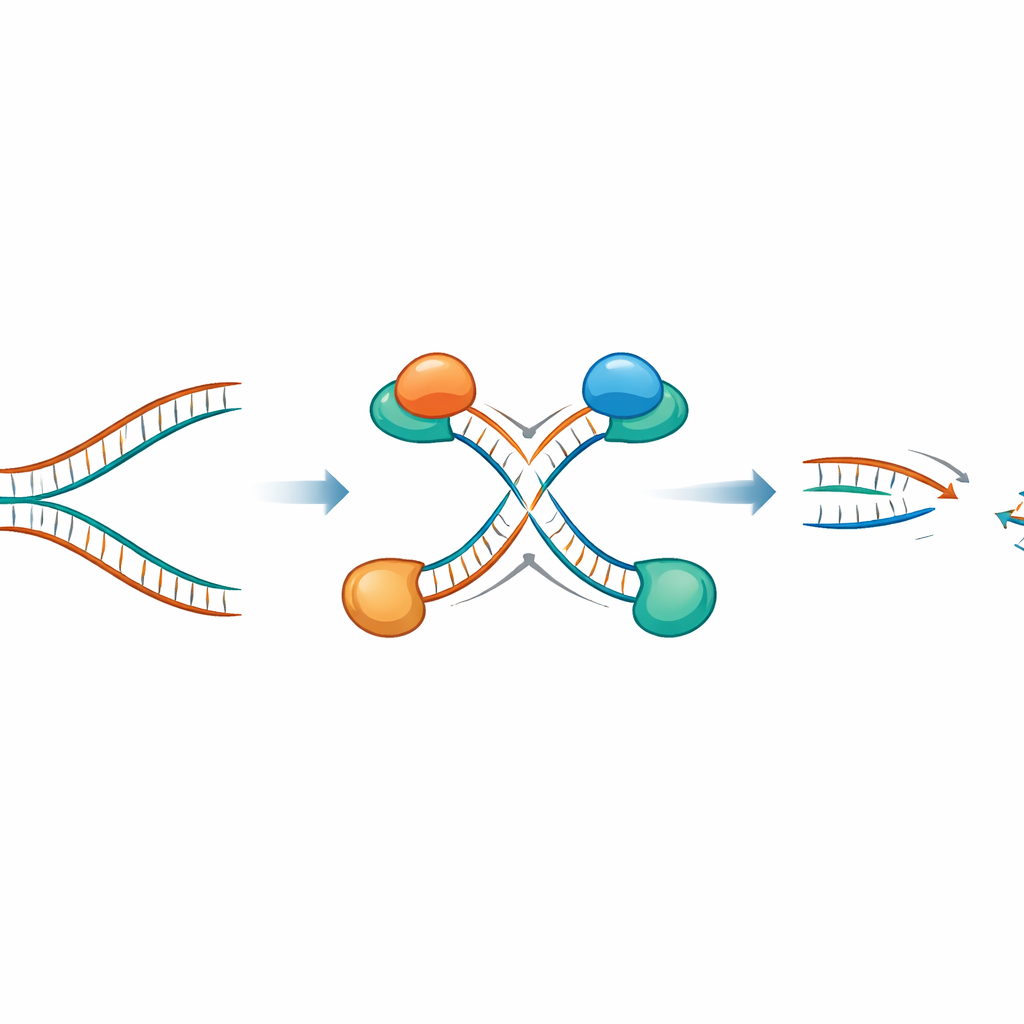
Un partenariat destructeur et des chromosomes brisés
L’équipe a ensuite étudié comment EXO1 coopère avec une autre nucléase, MRE11. À l’aide d’essais de proximité microscopiques, ils ont découvert qu’un excès d’EXO1 attire MRE11 sur l’ADN nouvellement synthétisé, tant aux endroits des lacunes qu’aux fourches inversées, formant des machines de découpe jumelées qui attaquent les deux brins en sens opposés. Même si les cellules possédaient toujours des protéines BRCA fonctionnelles, qui protègent normalement les fourches bloquées, l’action combinée d’EXO1 et de MRE11 a submergé cette protection. Le résultat a été une dégradation généralisée de l’ADN naissant, la conversion des lacunes et des fourches bloquées en cassures double-brin, et une augmentation marquée des dommages structurels aux chromosomes.
Du chaos génomique à la sensibilité aux médicaments
Bien que ces dommages favorisent le type de chaos génomique qui peut propulser l’évolution tumorale, ils créent aussi un talon d’Achille. Les cellules surchargées en EXO1 étaient hypersensibles au cisplatine, un médicament de chimiothérapie qui provoque des lésions volumineuses dans l’ADN, et aux inhibiteurs de PARP, des médicaments déjà efficaces contre les tumeurs dépourvues de fonction BRCA. En réalité, la réponse médicamenteuse des cellules riches en EXO1 ressemblait à celle des cellules présentant des défauts directs de BRCA, un état souvent qualifié de « BRCAness ». Pour un non-spécialiste, cela signifie que, même sans mutations dans les célèbres gènes BRCA, les tumeurs qui surexpriment EXO1 se comportent comme si elles étaient déficientes en BRCA : leur ADN est fragile et facilement renversé par des traitements qui stressent la réplication, ce qui suggère que le niveau d’EXO1 pourrait servir de biomarqueur pour orienter le choix thérapeutique.
Citation: Nusawardhana, A., Nicolae, C.M. & Moldovan, GL. The nuclease EXO1 promotes genomic instability by degrading nascent DNA in BRCA-proficient cells. Nat Commun 17, 3169 (2026). https://doi.org/10.1038/s41467-026-69981-1
Mots-clés: Réparation de l’ADN, instabilité génomique, voie BRCA, chimiothérapie anticancéreuse, nucléase EXO1