Clear Sky Science · zh
拓扑异构酶 VI 中对超螺旋 DNA 的识别与切割控制
解开生命的扭曲密码
在每个细胞内,DNA 并不是整齐的直梯,而是一根长而柔性的线,经常盘成螺旋和环。这样的扭曲对于将数米长的遗传物质装入显微级的空间至关重要,但它们也会产生结和缠绕,阻碍复制和转录等重要过程。本研究揭示了一种分子机器——拓扑异构酶 VI(Top6)——如何特异性识别并安全切割高度扭曲的 DNA,揭示细胞如何管理基因组中产生的机械应力。
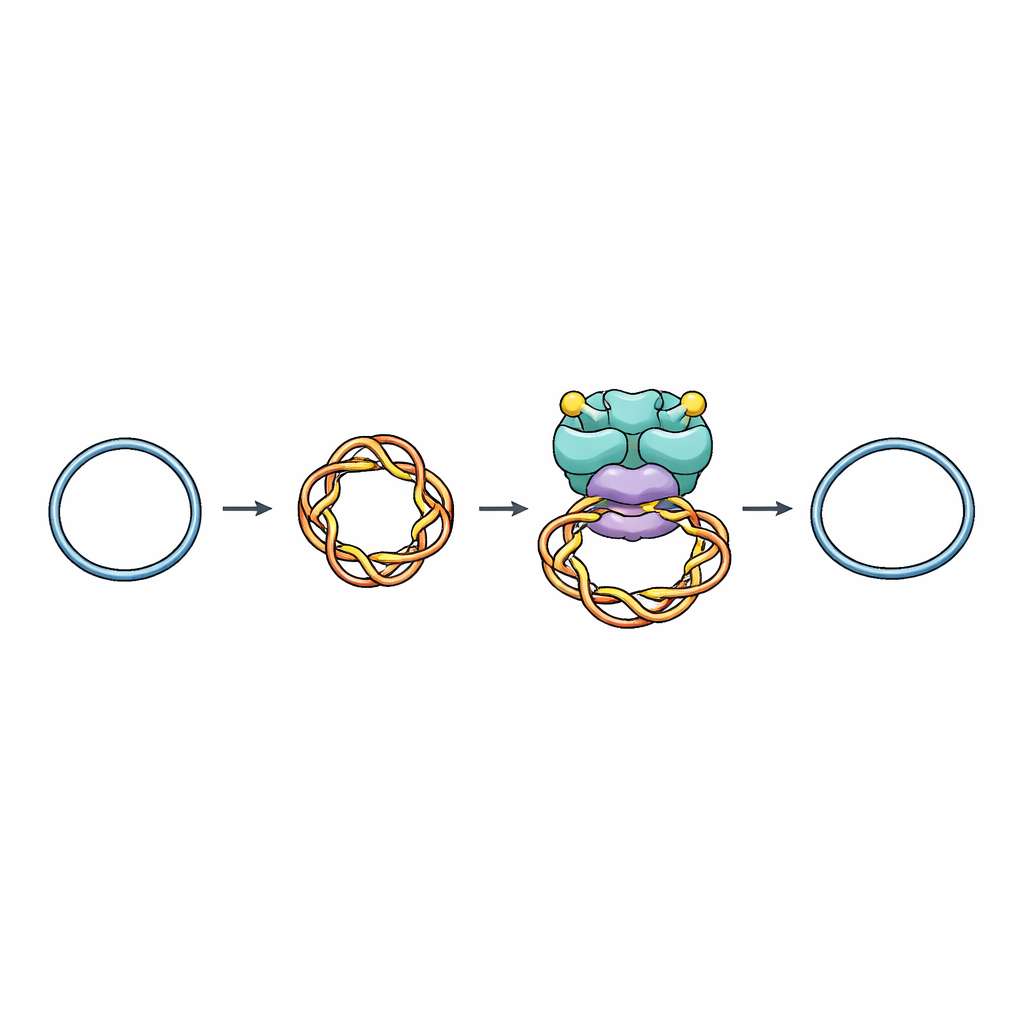
管理 DNA 纠结的分子工具
细胞依靠称为拓扑异构酶的酶来增加或去除 DNA 中的扭曲,以防在复制、转录和染色体分离过程中出现有害的缠结。拓扑异构酶 VI(Top6)存在于古菌和植物中,并与启动减数分裂和细菌抗病毒的某些蛋白相关,属于一类能切断 DNA 双链、将另一段 DNA 穿过断口再重新封合的酶。直到现在,科学家还缺乏关于 Top6 如何识别合适的切割位点以及如何避免意外有害断裂的详细图像。
捕捉 DNA 扭曲时的瞬间
研究者使用单粒子冷冻电子显微镜(single-particle cryo-EM),这是一种可在近原子分辨率下成像冷冻分子的技术,来观察 Top6 与人为制造的微小圆形超螺旋 DNA 的结合状态。他们解析了 Top6 在未切割和已切割两种状态下与这些螺旋结合的结构。无论哪种情况,Top6 都抱持着一段 74 碱基对的 DNA,使其弯成一个紧密的环,类似超螺旋体(plectoneme)顶端的弯曲——这种尖锐弯曲是过扭 DNA 中自然出现的。这解释了为何 Top6 偏好超螺旋 DNA 而非松弛的直段:其结合腔形状正好与强弯曲的片段相契合。
酶如何感知并选择合适的部位
更深入的观察表明,Top6 并非简单地抓住任何弯曲的 DNA。它偏好一种由特定序列构成、特别容易变形的区域。通过分析密度图谱,研究组推断出切割位点处的碱基对并计算了圆形 DNA 不同区段的柔韧性。切割位点位于一个相对刚性片段与非常柔软片段的边界处,并且切割发生的确切碱基阶跃本身异常易弯曲。该处的 DNA 被迫进入更压缩、略有非标准的构象。酶似乎利用局部柔性与尖锐弯曲的组合作为物理特征,借此定位安全的切割位点,而不是像传统意义上逐个“读取”碱基来决定。
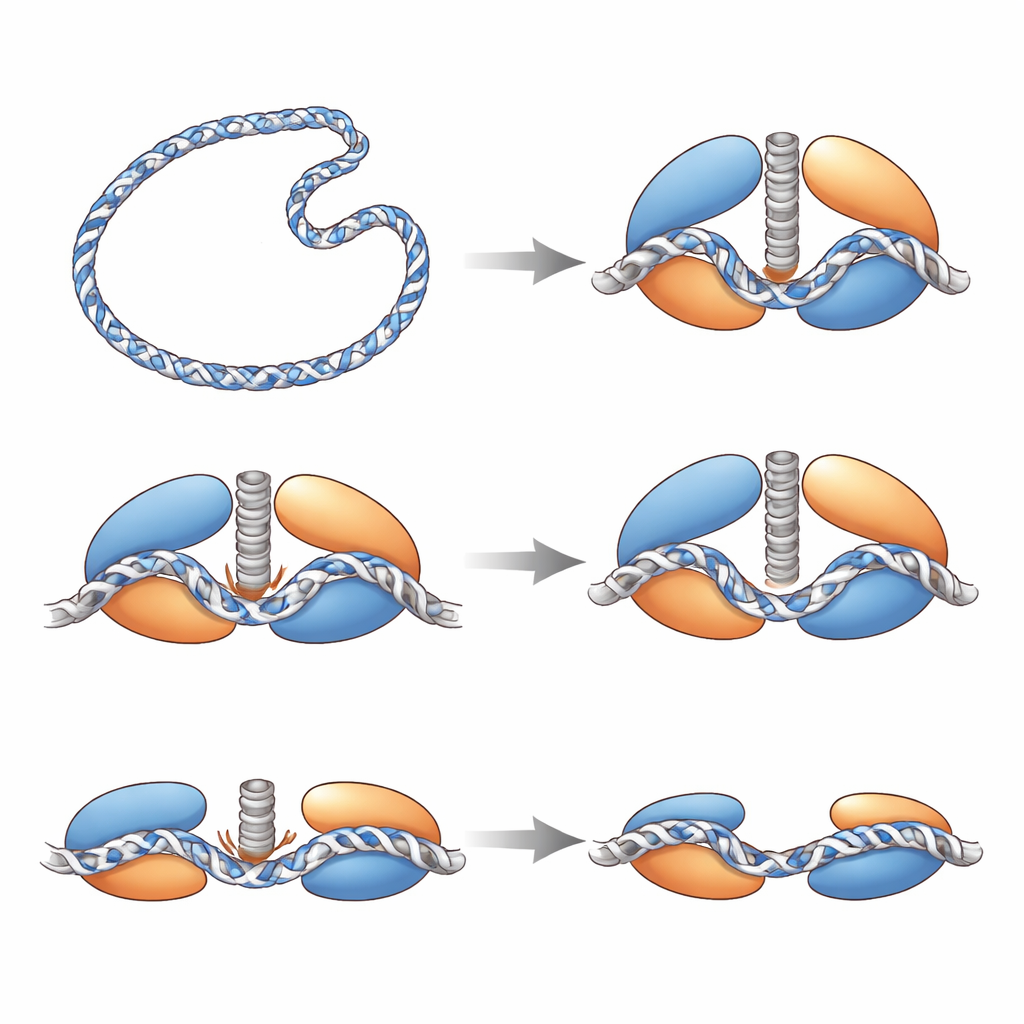
安全闩与张力传感器
这些结构还揭示了防止 Top6 过度切割 DNA 的内部安全机制。在处理 DNA 的酶半部中,一段可动的环只有在 DNA 被紧密弯曲到位时才变得有序;它类似闩锁,加固活性位点与 DNA 之间的配合。一对相反电荷的氨基酸形成了一个“静电夹”,物理上限制了催化酪氨酸到达 DNA 骨架。当研究者削弱该夹时,酶产生了更多断裂,表明该夹通常抑制切割。在 Top6 的 ATP 驱动半部,一根连接能量获取区与切割区的长螺旋柄像一个张力传感器:当其完整且笔直时,允许形成一个紧致、可切割的构象;当部分展开或因突变而不稳定时,酶难以放松超螺旋,表明该柄的受控柔性将能量利用与安全切割协调起来。
DNA 作为主动的机械伙伴
综合这些观察,研究将 Top6 与 DNA 描绘成一对机械舞伴。超螺旋在 DNA 中储存能量,推动某些序列产生尖锐弯曲。Top6 识别这些受力构象,将其夹住,且仅在其内部闩锁、夹和柄正确就位时,才实施受控的双链断裂并随后封合。这项工作显示了 DNA 的物理特性,而不仅仅是其字母序列,如何帮助决定切割的时机与位置。通过阐明 Top6 如何感知并响应超螺旋 DNA,研究加深了我们对染色体维护、减数分裂重组和某些细菌防御系统的理解,并凸显了生命如何利用扭曲分子的物理学来保持基因组既紧凑又完整。
引用: Richman, D.E., Wendorff, T.J., Rashid, F. et al. Supercoiled DNA recognition and cleavage control in topoisomerase VI. Nat Commun 17, 3092 (2026). https://doi.org/10.1038/s41467-026-69491-0
关键词: DNA 超螺旋, 拓扑异构酶 VI, DNA 力学, 冷冻电镜, 基因组稳定性