Clear Sky Science · de
Erkennung supergewickelter DNA und Kontrolle der Spaltung in Topoisomerase VI
Das verwobene Programm des Lebens entwirren
In jeder Zelle ist DNA keine gerade Leiter, sondern ein langer, flexibler Faden, der sich häufig zu Windungen und Schleifen dreht. Diese Drehungen sind entscheidend, um Meter an genetischem Material in mikroskopische Räume zu packen, gleichzeitig erzeugen sie aber auch Knoten und Verwicklungen, die essenzielle Vorgänge wie Kopieren und Ablesen der Gene zum Stillstand bringen können. Diese Studie zeigt, wie eine molekulare Maschine, die Topoisomerase VI, speziell hochgradig verdrillte DNA erkennt und sicher schneidet und gewährt damit Einblick, wie Zellen mechanische Belastungen im Erbgut handhaben.
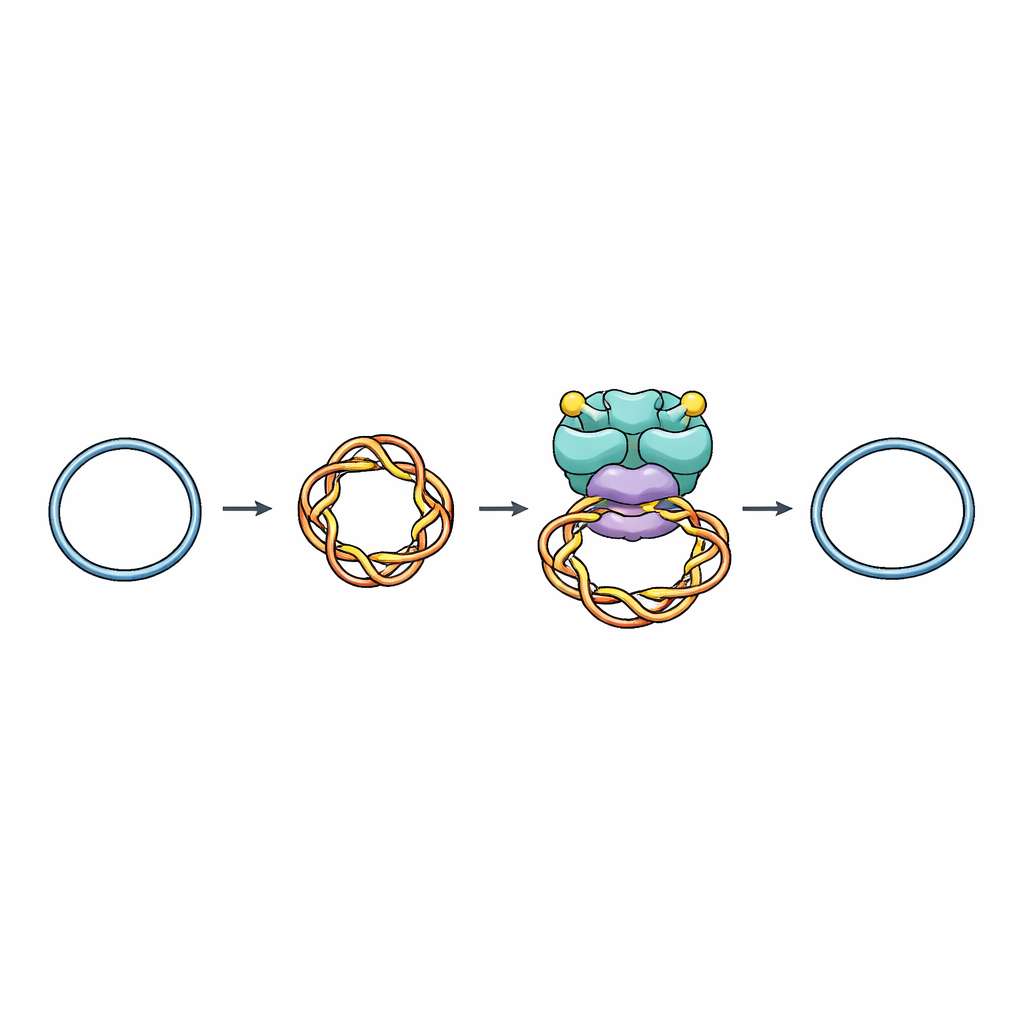
Ein molekulares Werkzeug zum Umgang mit DNA-Knoten
Zellen verlassen sich auf Enzyme, die Topoisomerasen genannt werden, um Drehungen in der DNA hinzuzufügen oder zu entfernen und so gefährliche Verknotungen während Replikation, Transkription und Chromosomentrennung zu verhindern. Topoisomerase VI (Top6), die in Archaeen und Pflanzen vorkommt und mit Proteinen verwandt ist, die die Meiose einleiten oder Bakterien gegen Viren verteidigen, gehört zu einer Familie, die beide Stränge der DNA-Helix durchtrennt, ein anderes DNA-Stück durch die Lücke hindurchführt und dann die Bruchstelle wieder verschließt. Bisher fehlte ein detailliertes Bild davon, wie Top6 das richtige DNA-Stück zum Schneiden erkennt und wie es vermeidet, versehentlich schädliche Brüche zu erzeugen.
DNA beim Verdrehen in flagranti erwischen
Die Forscher verwendeten Einzelpartikel-Kryo-Elektronenmikroskopie, eine Technik, die eingefrorene Moleküle in annähernd atomarer Auflösung abbildet, um Top6 gebunden an kleinen zirkulären DNA-Stücken zu visualisieren, die absichtlich supergewickelt wurden — ähnlich einem überdrehten Gummiband. Sie lösten Strukturen von Top6 sowohl im ungeschnittenen als auch im geschnittenen Zustand, während das Enzym diese Windungen hielt. In allen Fällen umfasste Top6 eine 74-Basenpaare lange DNA-Strecke, die zu einer engen Schleife gebogen war, die der Spitze eines plectonemisch supergewickelten Segments ähnelt — jener scharfen Biegung, die in überdrehten DNA-Strängen natürlich entsteht. Das erklärt, warum Top6 supergewickelte DNA gegenüber entspannten, geraden Stücken bevorzugt: seine Bindungstasche ist so geformt, dass sie ein stark gekrümmtes Segment aufnimmt.
Wie das Enzym fühlt und die richtige Stelle auswählt
Genauere Untersuchung zeigte, dass Top6 nicht einfach jede gebogene DNA ergreift. Es bevorzugt einen bestimmten Bereich, dessen zugrundeliegende Sequenz ihn besonders leicht verformbar macht. Durch Analyse der Dichtemaps schloss das Team darauf, welche Basenpaare an der Schnittstelle vorhanden sind, und berechnete, wie flexibel verschiedene Abschnitte der zirkulären DNA sein sollten. Die Schnittstelle liegt an einer Grenze, an der ein vergleichsweise starrer Abschnitt auf einen sehr flexiblen trifft, und die genauen Basenstufen, an denen die Schnitte erfolgen, sind selbst ungewöhnlich biegsam. Rund um diesen Punkt wird die DNA in eine stärker komprimierte, leicht nicht-standardmäßige Form gezwungen. Das Enzym scheint diese Kombination aus lokaler Flexibilität und scharfer Biegung als physikalisches Merkmal zu nutzen, das ihm erlaubt, sichere Schnittstellen zu identifizieren, ohne die genetische Information im üblichen buchstabenweisen Sinn abzulesen.
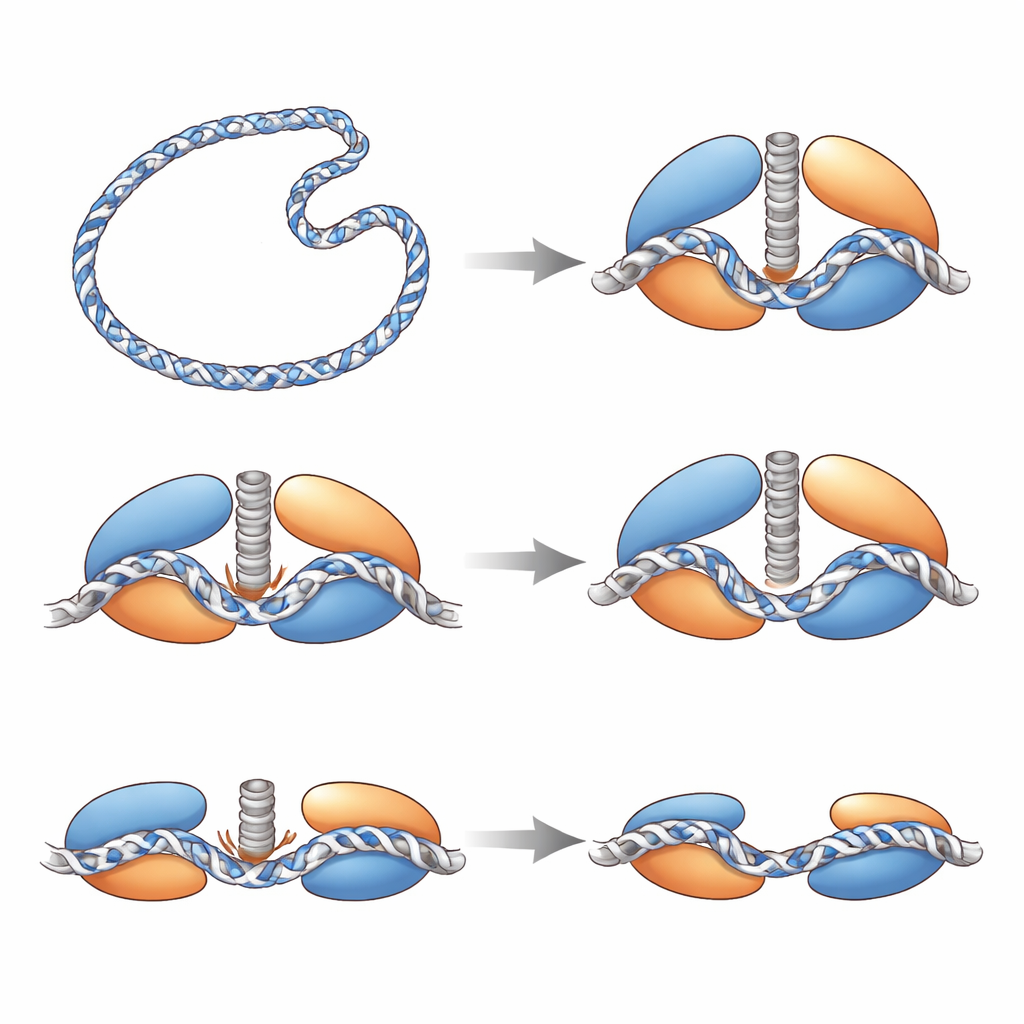
Eine Sicherung und ein Spannungssensor
Die Strukturen offenbaren außerdem interne Schutzmechanismen, die verhindern, dass Top6 die DNA zu leicht schneidet. Innerhalb der DNA-verarbeitenden Hälfte des Enzyms wird eine flexible Schleife nur dann geordnet, wenn die DNA fest gebogen anliegt; sie wirkt wie ein Riegel, der das aktive Zentrum gegen die DNA abstützt. Ein Paar entgegengesetzt geladener Aminosäuren bildet eine „elektrostatische Klammer“, die das katalytische Tyrosin physisch davon abhält, die DNA-Rückgrat zu erreichen. Wenn das Team diese Klammer abschwächte, erzeugte das Enzym deutlich mehr Brüche, was zeigt, dass die Klammer normalerweise die Spaltung unterdrückt. In der ATP-abhängigen Hälfte von Top6 verhält sich ein langer helikaler Stiel, der die Bewegungen im energieerzeugenden Bereich mit dem DNA-schneidenden Bereich verbindet, wie ein Spannungssensor: Ist er intakt und gestreckt, ermöglicht er eine enge, spaltungsbereite Konfiguration; ist er teilweise entfaltet oder durch Mutation destabilisiert, hat das Enzym Schwierigkeiten, Supercoils zu lösen, was darauf hindeutet, dass kontrollierte Flexibilität in diesem Stiel die Energienutzung mit sicherer Spaltung koordiniert.
DNA als aktiver mechanischer Partner
Setzt man diese Beobachtungen zusammen, zeichnet die Studie Top6 und DNA als Partner in einem mechanischen Tanz. Supercoiling speichert Energie in der DNA und treibt bestimmte Sequenzen dazu, scharf zu biegen. Top6 erkennt diese gestressten Formen, umklammert sie und führt — nur wenn Riegel, Klammer und Stiel intern korrekt positioniert sind — einen kontrollierten Doppelstrangbruch durch, bevor es ihn wieder verschließt. Diese Arbeit zeigt, dass die physikalischen Eigenschaften der DNA, nicht nur ihre Buchstabenfolge, mitbestimmen, wo und wann Schnitte stattfinden. Indem sie klärt, wie Top6 supergewickelte DNA wahrnimmt und darauf reagiert, vertieft die Studie unser Verständnis der Chromosomenpflege, der meiotischen Rekombination und bestimmter bakterieller Abwehrsysteme und hebt hervor, wie das Leben die Physik verdrehter Moleküle nutzt, um das Genom gleichzeitig kompakt und intakt zu halten.
Zitation: Richman, D.E., Wendorff, T.J., Rashid, F. et al. Supercoiled DNA recognition and cleavage control in topoisomerase VI. Nat Commun 17, 3092 (2026). https://doi.org/10.1038/s41467-026-69491-0
Schlüsselwörter: DNA-Supercoiling, Topoisomerase VI, DNA-Mechanik, Cryo-Elektronenmikroskopie, Genomstabilität