Clear Sky Science · zh
NSUN2通过MAPK/ERK信号通路介导肠道干细胞扩增与结直肠肿瘤起始
一种微小的RNA标记如何助燃结肠癌
结肠癌通常在出现任何症状之前就已悄然开始,当肠道深处的少数干细胞开始异常行为。该研究探讨了一种细微的RNA化学修饰——这些携带细胞制造蛋白质指令的信使上的标记——并展示了它如何将肠道干细胞推向不受控制的生长。理解这一隐蔽的调控层可能为结直肠癌的早期检测以及更温和、更有针对性的治疗打开新路径。
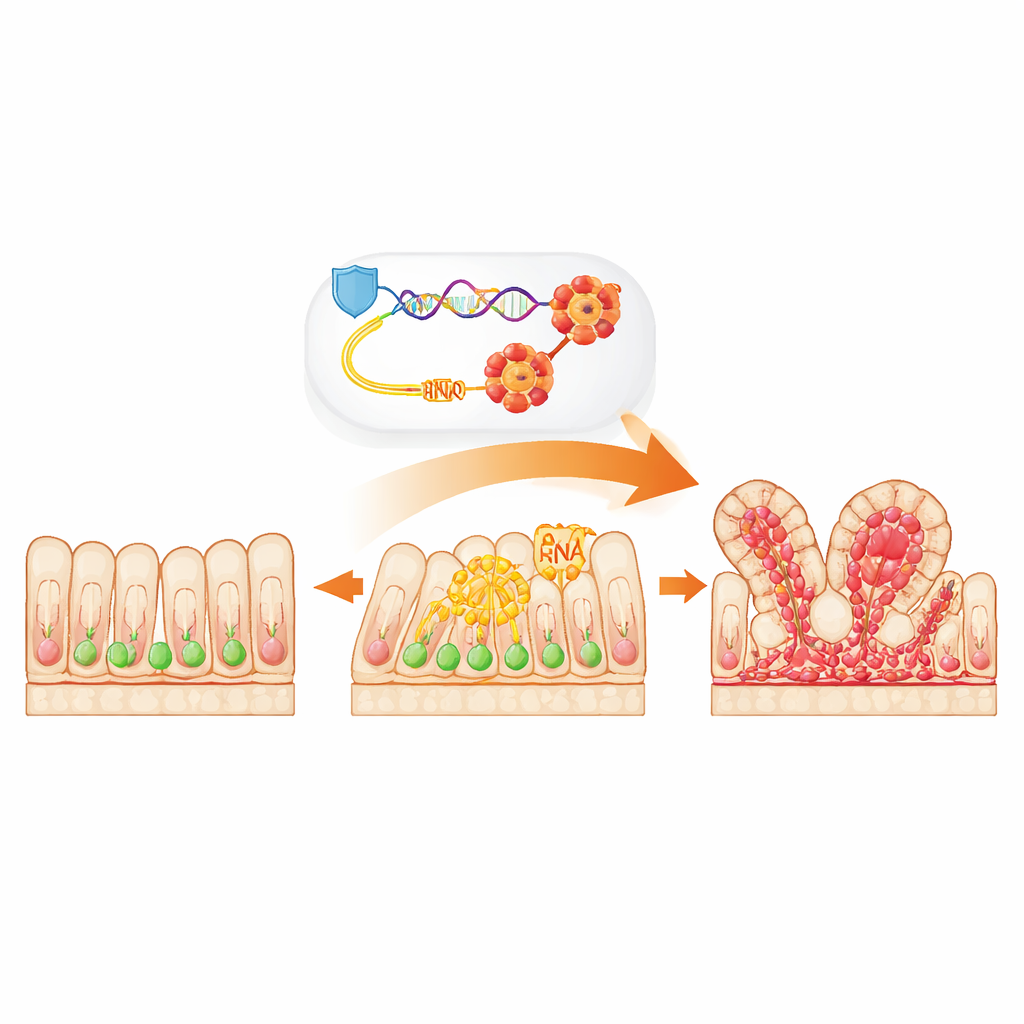
结肠肿瘤的根源:干细胞
我们肠道的上皮内衬由位于微小隐窝(隐窝)中的专门干细胞不断更新。在正常情况下,这些细胞分裂的频率恰到好处,以替换损耗的组织。然而在多数结直肠癌中,对守护基因APC的早期损伤打破了这种平衡,导致干细胞过度增殖并形成最初的异常增生。研究者聚焦于肿瘤起始的最早阶段,探究为何在APC丢失后,某些干细胞尤其容易驱动癌变。
一种将细胞生长“加速”的RNA“写入者”
研究组将注意力集中在NSUN2上,这是一种通过在特定胞嘧啶位点添加称为m5C的小标签来化学修饰RNA的蛋白质。通过挖掘已有数据并检查小鼠肠道和人类肿瘤样本,他们发现APC丧失和确诊的结直肠癌中NSUN2水平显著升高。肿瘤中NSUN2较多的患者预后往往更差。在由小鼠干细胞培养的三维小肠类器官中,降低NSUN2显著削弱了细胞形成新类器官的能力,减小了类器官体积,并降低了经典干细胞标志的活性——这些都是NSUN2有助于维持类癌性干细胞状态的重要证据。
对癌性生长必需,但对正常修复可有可无
为了观察NSUN2在活组织中的作用,科学家构建了可以在肠上皮中特异性删除NSUN2、APC或两者的小鼠模型。单独删除APC会引发预期的细胞分裂激增和干细胞基因活性上升。引人注目的是,当同时删除NSUN2时,这种过度生长在很大程度上被抑制:分裂的细胞更少,干细胞标志物显著减少。然而在没有APC丧失的健康肠道中,删除NSUN2对组织结构、细胞更替或干细胞基因表达影响甚微。这一对比表明NSUN2对患病的、APC缺失的干细胞尤为重要,而正常肠道的维持可以在没有它的情况下继续进行。
解码分子链式反应
为弄清NSUN2如何发挥作用,研究者在小鼠肠道和类器官的信使RNA上绘制了m5C标记图谱。NSUN2丢失导致特定RNA失去该标记,尤以参与RNA处理、干细胞调控以及一个主要生长途径MAPK/ERK相关的RNA为甚。这些低甲基化的RNA也往往表达量下降,暗示m5C标记有助于稳定它们或提高其利用效率。当NSUN2被删除时,在APC缺失模型中,MAPK/ERK通路中关键开关ERK的活性磷酸化形式下降,同时干细胞特征也随之减弱。但引入一种永久活化的信号蛋白KRAS变体能恢复ERK活性并挽救干细胞扩增,即便在没有NSUN2的情况下也是如此。这表明NSUN2位于驱动早期肿瘤生长的事件链中,位于MAPK/ERK通路上游。
对未来癌症预防的意义
综合来看,这项工作将NSUN2定位为将RNA化学修饰与将正常肠道干细胞转变为癌性干细胞的失控信号相连接的关键分子中介。由于健康肠组织能耐受NSUN2的丢失,而APC突变的细胞在没有它时难以启动肿瘤,NSUN2或其m5C标记可能成为旨在阻止结直肠癌完全形成的有吸引力的治疗靶点。简言之,RNA上的一处微小化学修饰似乎对维持健康与发生潜在致命疾病之间的界限具有重大影响。
引用: Bastem Akan, A., Billard, C.V., Chen, SY. et al. NSUN2 mediates intestinal stem cell expansion and colorectal tumour initiation via MAPK/ERK signalling. Cell Death Dis 17, 322 (2026). https://doi.org/10.1038/s41419-026-08560-0
关键词: 结直肠癌, 肠道干细胞, RNA甲基化, NSUN2, MAPK ERK信号