Clear Sky Science · fr
NSUN2 médie l'expansion des cellules souches intestinales et l'initiation des tumeurs colorectales via la signalisation MAPK/ERK
Comment une petite marque sur l'ARN peut contribuer au déclenchement du cancer du côlon
Le cancer du côlon commence souvent bien avant l'apparition de symptômes, lorsque quelques cellules souches profondément nichées dans l'intestin commencent discrètement à se comporter anormalement. Cette étude explore une marque chimique subtile sur l'ARN — les messages qui indiquent aux cellules quelles protéines produire — et montre comment elle peut pousser les cellules souches intestinales vers une croissance incontrôlée. Comprendre ce niveau caché de régulation pourrait ouvrir la voie à une détection plus précoce et à des traitements plus doux et ciblés du cancer colorectal.
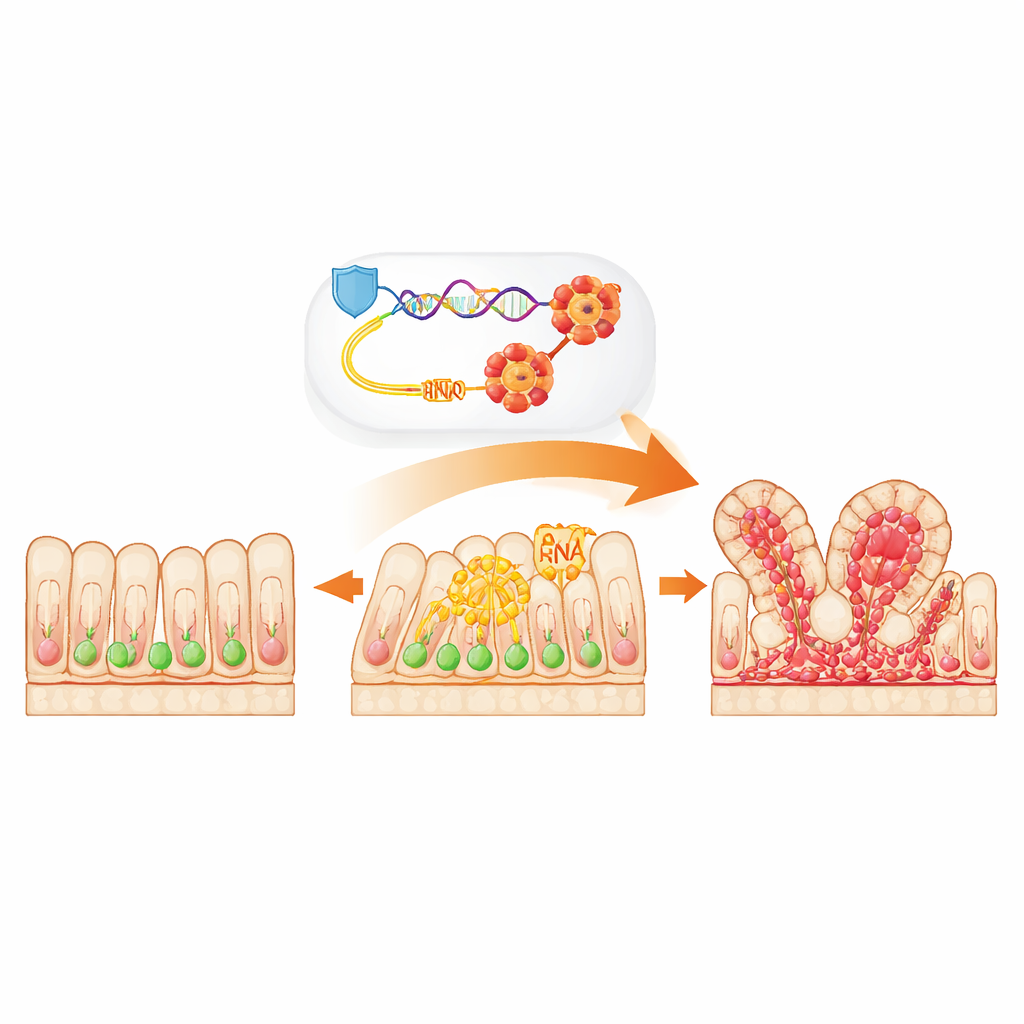
Des cellules souches à la racine des tumeurs du côlon
L'épithélium intestinal est constamment renouvelé par des cellules souches spécialisées nichées dans de petites cavités appelées cryptes. En conditions normales, ces cellules se divisent juste ce qu'il faut pour remplacer les tissus usés. Dans la plupart des cancers colorectaux, toutefois, un coup précoce porté à un gène protecteur nommé APC perturbe cet équilibre, entraînant une multiplication excessive des cellules souches et la formation des premiers foyers de croissance anormale. Les chercheurs se sont concentrés sur cette phase initiale d'initiation tumorale, en cherchant à comprendre pourquoi certaines cellules souches, une fois l'APC perdu, deviennent particulièrement susceptibles de conduire au cancer.
Un « écrivain » de l'ARN qui stimule la prolifération cellulaire
L'équipe s'est intéressée à NSUN2, une protéine qui modifie chimiquement l'ARN en ajoutant une petite étiquette appelée m5C sur certaines bases cytosine. En exploitant des données existantes et en examinant des intestins de souris ainsi que des échantillons tumoraux humains, ils ont constaté que les niveaux de NSUN2 augmentent fortement lorsque l'APC est perdu et dans les cancers colorectaux établis. Les patients dont les tumeurs présentent plus de NSUN2 ont tendance à avoir un pronostic plus défavorable. Dans des mini-intestins 3D cultivés à partir de cellules souches de souris, la réduction de NSUN2 a fortement diminué la capacité des cellules à former de nouveaux organoïdes, réduit leur taille et abaissé l'activité des marqueurs classiques des cellules souches — des signes nets que NSUN2 aide à maintenir un état de cellules souches de type cancéreux.
Essentiel pour la croissance cancéreuse, superflu pour la réparation normale
Pour observer le comportement de NSUN2 dans un tissu vivant, les scientifiques ont conçu des souris dans lesquelles ils pouvaient supprimer NSUN2, APC, ou les deux spécifiquement dans l'épithélium intestinal. La suppression d'APC seule a déclenché l'explosion attendue de divisions cellulaires et une hausse de l'expression des gènes des cellules souches. Fait frappant, lorsque NSUN2 a été également supprimé, cette hypercroissance a été largement atténuée : moins de cellules se divisaient et les marqueurs de cellules souches étaient beaucoup moins abondants. Pourtant, dans des intestins sains sans perte d'APC, la suppression de NSUN2 a eu peu d'effet sur la structure tissulaire, le renouvellement cellulaire ou l'expression des gènes des cellules souches. Ce contraste suggère que NSUN2 est particulièrement important pour les cellules souches malades déficientes en APC, tandis que l'entretien normal de l'intestin peut se poursuivre sans lui.
Décoder la chaîne d'événements moléculaires
Pour comprendre comment NSUN2 exerce ses effets, les chercheurs ont cartographié les marques m5C sur les ARNm des intestins de souris et des organoïdes. La perte de NSUN2 a provoqué la disparition de cette marque sur des ARNm spécifiques, en particulier ceux impliqués dans le traitement de l'ARN, le contrôle des cellules souches et une voie majeure de croissance connue sous le nom de MAPK/ERK. Ces ARNm hypométhylés tendaient également à diminuer en abondance, ce qui suggère que la marque m5C aide à stabiliser ces molécules ou à en améliorer l'utilisation. Lors de la suppression de NSUN2, la forme active et phosphorylée d'ERK — un interrupteur clé de la voie MAPK/ERK — diminuait dans les modèles déficients en APC, parallèlement aux caractéristiques des cellules souches. Mais l'introduction d'une version constitutivement active d'une autre protéine de signalisation, KRAS, a rétabli l'activité d'ERK et permis la reprise de l'expansion des cellules souches, même en l'absence de NSUN2. Cela place NSUN2 en amont de MAPK/ERK dans la chaîne d'événements qui conduit à la croissance tumorale précoce.
Implications pour la prévention future du cancer
Dans l'ensemble, ces travaux positionnent NSUN2 comme un médiateur moléculaire crucial reliant la chimie de l'ARN à la signalisation débridée qui transforme les cellules souches intestinales normales en cellules souches cancéreuses. Parce que le tissu intestinal sain peut tolérer la perte de NSUN2, alors que les cellules porteuses d'une mutation d'APC ne peuvent pas initier facilement une tumeur sans lui, NSUN2 ou ses marques m5C pourraient constituer une cible attrayante pour des thérapies visant à empêcher le cancer colorectal de s'installer pleinement. En bref, une petite modification chimique de l'ARN semble exercer une influence disproportionnée sur qui reste en bonne santé et qui développe une maladie potentiellement mortelle.
Citation: Bastem Akan, A., Billard, C.V., Chen, SY. et al. NSUN2 mediates intestinal stem cell expansion and colorectal tumour initiation via MAPK/ERK signalling. Cell Death Dis 17, 322 (2026). https://doi.org/10.1038/s41419-026-08560-0
Mots-clés: cancer colorectal, cellules souches intestinales, méthylation de l'ARN, NSUN2, signalisation MAPK ERK