Clear Sky Science · pl
NSUN2 pośredniczy w ekspansji komórek macierzystych jelita i inicjacji nowotworu jelita grubego poprzez szlak MAPK/ERK
Jak maleńska modyfikacja RNA może zapoczątkować raka jelita
Rak jelita grubego często zaczyna się na długo przed pojawieniem się objawów, gdy kilka komórek macierzystych głęboko w jelicie zaczyna dyskretnie zachowywać się nieprawidłowo. To badanie opisuje subtelną chemiczną modyfikację RNA — przekazów, które mówią komórkom, jakie białka produkować — i pokazuje, jak może ona popychać komórki macierzyste jelita w kierunku niekontrolowanego wzrostu. Zrozumienie tej ukrytej warstwy regulacji może otworzyć drzwi do wcześniejszego wykrywania oraz łagodniejszych, bardziej ukierunkowanych terapii raka jelita grubego.
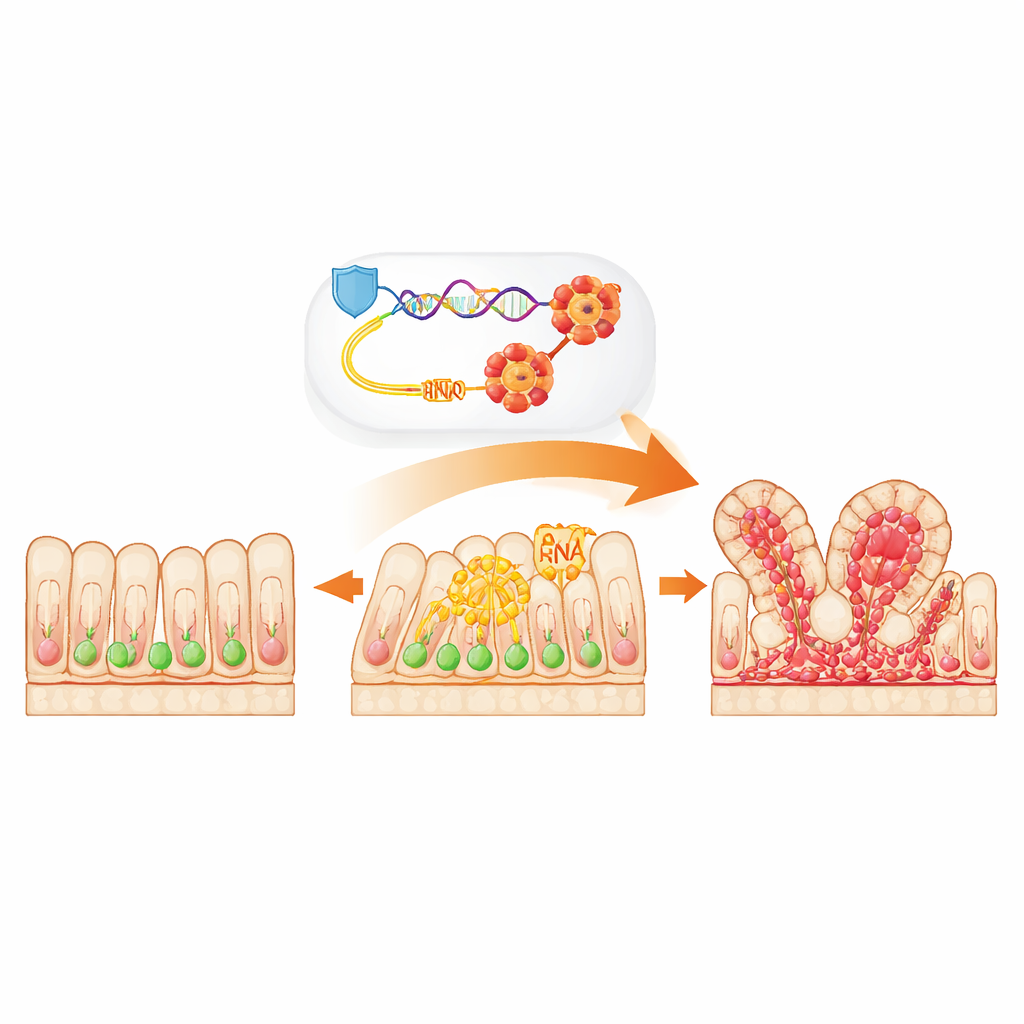
Komórki macierzyste u podstawy guzów jelita
Wyściółka naszych jelit jest nieustannie odnawiana przez wyspecjalizowane komórki macierzyste ukryte w maleńkich kieszonkach zwanych kryptami. W normalnych warunkach komórki te dzielą się w wystarczającym stopniu, by zastąpić zużytą tkankę. W większości przypadków raka jelita grubego jednak wczesne uszkodzenie genu „strażnika” o nazwie APC zaburza tę równowagę, powodując nadmierną proliferację komórek macierzystych i tworzenie pierwszych nieprawidłowych zgrubień. Badacze skupili się na tej najwcześniejszej fazie inicjacji guza, zadając pytanie, dlaczego niektóre komórki macierzyste, po utracie APC, stają się szczególnie skłonne do napędzania raka.
„Długopis” RNA, który zwiększa wzrost komórek
Zespół skupił się na NSUN2, białku, które chemicznie modyfikuje RNA, dodając małą etykietę zwaną m5C do niektórych zasad cytozynowych. Analizując istniejące dane oraz badając jelita myszy i próbki ludzkich nowotworów, odkryli, że poziomy NSUN2 gwałtownie rosną po utracie APC i w ustalonych nowotworach jelita grubego. Pacjenci, których guzy wykazują wyższe stężenie NSUN2, mają skłonność do gorszych wyników. W trójwymiarowych mini-jelitach hodowanych z mysich komórek macierzystych obniżenie poziomu NSUN2 znacząco zmniejszyło zdolność komórek do tworzenia nowych organoidów, zmniejszyło rozmiar organoidów i obniżyło aktywność klasycznych markerów komórek macierzystych — mocne sygnały, że NSUN2 pomaga podtrzymywać nowotworopodobny stan komórek macierzystych.
Niezbędny dla rozrostu nowotworowego, zbędny przy normalnej naprawie
Aby zobaczyć, jak NSUN2 zachowuje się w żywej tkance, naukowcy zmodyfikowali myszy tak, by mogli usuwać NSUN2, APC lub oba konkretnie w nabłonku jelita. Usunięcie samego APC wywołało oczekiwany wybuch podziałów komórkowych i wzrost aktywności genów komórek macierzystych. Co zaskakujące, gdy jednocześnie usunięto NSUN2, ten nadmierny wzrost został w dużej mierze stłumiony: mniej komórek ulegało podziałom, a markery komórek macierzystych były znacznie mniej liczne. Jednak w zdrowych jelitach, bez utraty APC, usunięcie NSUN2 niewiele zmieniało strukturę tkanki, obrót komórek ani ekspresję genów komórek macierzystych. Ten kontrast sugeruje, że NSUN2 jest szczególnie ważny dla chorych, pozbawionych APC komórek macierzystych, podczas gdy normalna utrzymanie jelita może przebiegać bez niego.
Odszyfrowanie molekularnego łańcucha reakcji
Aby odkryć, jak NSUN2 wywiera swoje efekty, badacze zmapowali oznaczenia m5C w całych mRNA zarówno mysich jelit, jak i organoidów. Utrata NSUN2 spowodowała, że konkretne RNA straciły tę modyfikację, zwłaszcza te zaangażowane w przetwarzanie RNA, kontrolę komórek macierzystych oraz w główny szlak wzrostu znany jako MAPK/ERK. Te hypometylowane RNA również miały tendencję do spadku obfitości, co sugeruje, że znak m5C pomaga je stabilizować lub efektywnie wykorzystywać. Gdy NSUN2 został usunięty, aktywna, ufosforylowana forma ERK — kluczowy przełącznik w szlaku MAPK/ERK — spadła w modelach z utratą APC, wraz z cechami komórek macierzystych. Jednak wprowadzenie trwale aktywnej wersji innego białka sygnalizacyjnego, KRAS, przywróciło aktywność ERK i uratowało ekspansję komórek macierzystych, nawet w braku NSUN2. To umieszcza NSUN2 powyżej MAPK/ERK w łańcuchu zdarzeń napędzających wczesny wzrost guza.
Co to oznacza dla przyszłej prewencji raka
Podsumowując, praca ta stawia NSUN2 w roli kluczowego pośrednika molekularnego łączącego chemię RNA z niekontrolowaną sygnalizacją, która przekształca normalne komórki macierzyste jelita w komórki macierzyste nowotworu. Ponieważ zdrowa tkanka jelita toleruje utratę NSUN2, podczas gdy komórki z mutacją APC nie są w stanie łatwo zainicjować guzów bez niego, NSUN2 lub jego znaczniki m5C mogą stanowić atrakcyjny cel dla terapii mających na celu zatrzymanie raka jelita grubego, zanim się w pełni rozwinie. Krótko mówiąc, drobna chemiczna modyfikacja RNA wydaje się mieć nieproporcjonalnie duży wpływ na to, kto pozostaje zdrowy, a kto rozwija potencjalnie śmiertelną chorobę.
Cytowanie: Bastem Akan, A., Billard, C.V., Chen, SY. et al. NSUN2 mediates intestinal stem cell expansion and colorectal tumour initiation via MAPK/ERK signalling. Cell Death Dis 17, 322 (2026). https://doi.org/10.1038/s41419-026-08560-0
Słowa kluczowe: rak jelita grubego, komórki macierzyste jelita, metylacja RNA, NSUN2, sygnalizacja MAPK ERK