Clear Sky Science · zh
NSUN2通过ALYREF/YBX1轴对YAP的m5C调控促进非小细胞肺癌肿瘤生长和转移
这项肺癌研究为何重要
肺癌是全球致死率最高的癌症,其中大多数死亡来自经常在被发现前就发生扩散的非小细胞肺癌(NSCLC)。本研究深入探讨了帮助肺肿瘤生长并在全身播散的分子“线路”。通过揭示一条特定的分子链条,该链条能增强癌细胞内的强大生长开关,研究为开发能在尽量不伤害健康组织的前提下减缓或阻止疾病的新药靶点提供了线索。
癌细胞中被掩盖的一层控制
我们的基因载于DNA,但RNA——作为遗传信息的工作拷贝——决定细胞何时合成哪些蛋白。近年来,科学家发现RNA本身带有化学标记,类似剧本边角的注释,可以改变RNA的寿命和被翻译的强度。其中一种标记是m5C,即加到RNA碱基胞嘧啶上的小化学标签。本研究显示,在NSCLC中,一种叫NSUN2的酶会在编码YAP的RNA上添加额外的m5C标记。患者的肿瘤组织中NSUN2和YAP水平均高于邻近正常组织,且任一蛋白水平更高的患者预后通常更差。
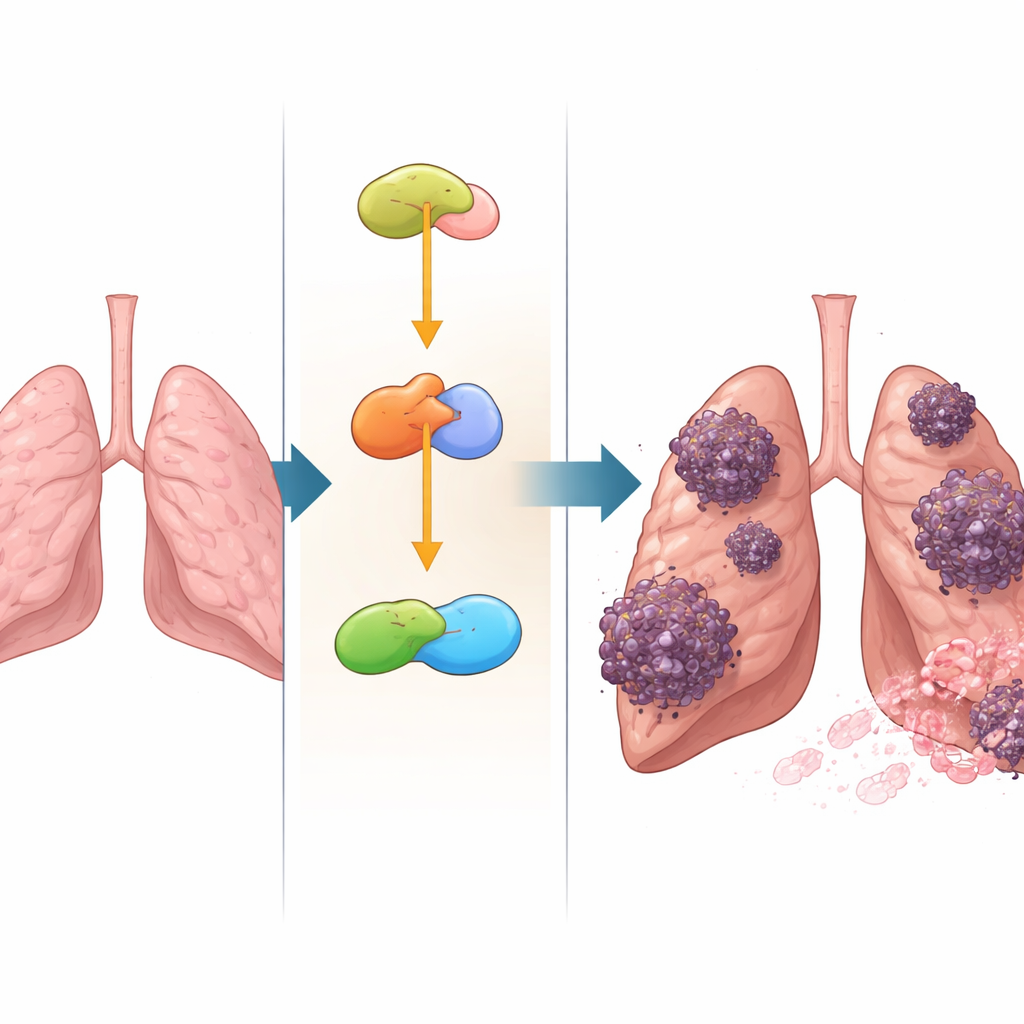
打开一个危险的生长开关
YAP像一个控制细胞增殖、运动和形态变化的中央节流阀。当其过度活化时,可推动细胞更快分裂、入侵周围组织并脱落形成转移。研究者发现NSUN2和YAP在NSCLC细胞中驱动许多相同的癌性行为:促进细胞分裂、迁移、穿越人工屏障的侵袭能力以及上皮—间质转化(epithelial–mesenchymal transition),这一过程中细胞松动附着并变得更具移动性。在小鼠体内,使肺癌细胞过表达NSUN2会形成更大、更具侵袭性的肿瘤并在肺内产生更多转移灶,而降低YAP则削弱了这些效应。这表明NSUN2对肿瘤生长的影响在很大程度上依赖于其提高YAP水平的能力。
保护癌性信息的接力团队
NSUN2并非独自作用。在它在YAP RNA上添加m5C标记后,两个RNA结合蛋白ALYREF和YBX1会识别并结合被修饰的信使。研究揭示了一种接力机制:ALYREF首先识别被标记的RNA,然后将其传递给YBX1,三者与NSUN2共同形成一个三元复合体。该复合体保护YAP RNA免受AGO2(一种通常帮助降解不需要信息的蛋白)的作用,并有助于招募将RNA翻译为蛋白的机器。结果是YAP RNA存留更久且被更高效地翻译,细胞内YAP蛋白累积增多。下游,YAP启动驱动细胞周期进展、侵袭和组织重塑酶的基因表达,均为侵袭性肿瘤的标志。
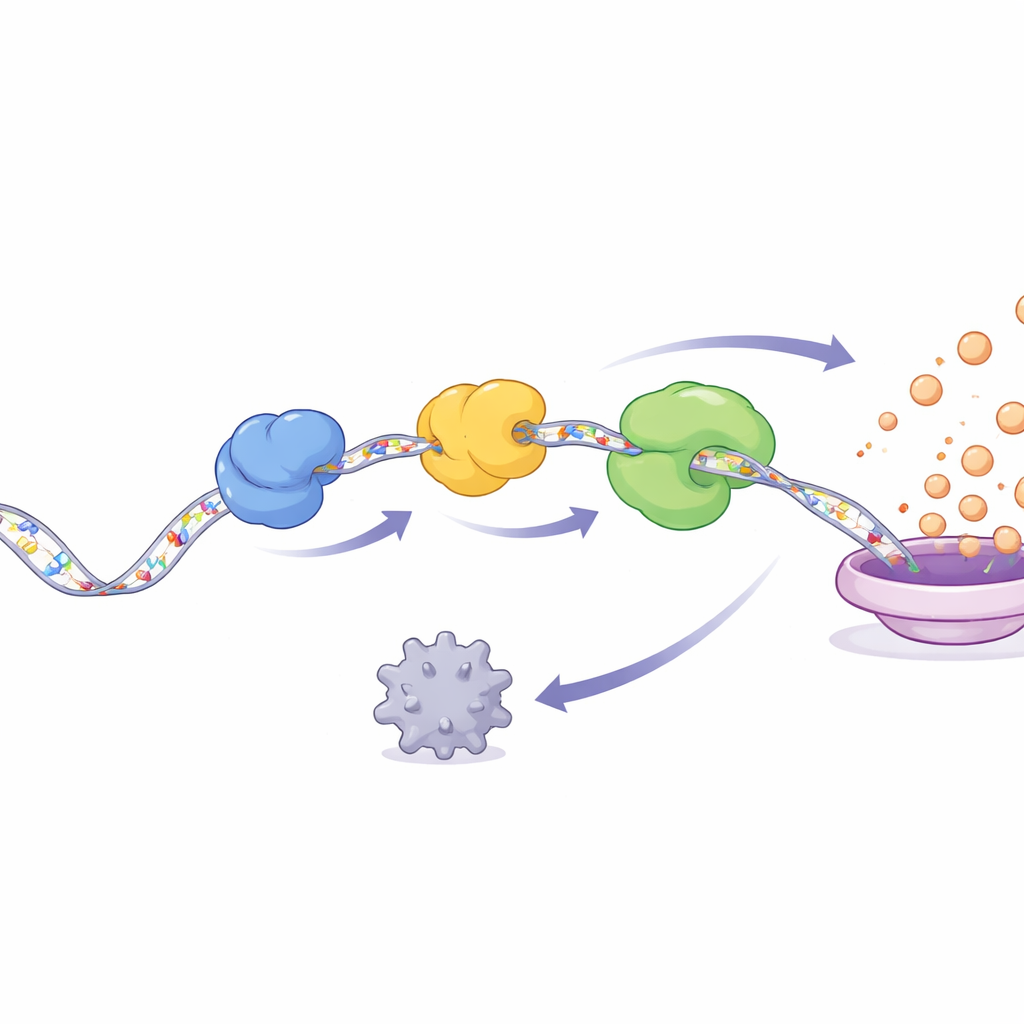
自我强化的癌性循环
耐人寻味的是,这种关系是双向的。YAP与一种叫TEAD2的DNA结合蛋白配合,开启许多基因的表达,研究团队发现NSUN2就是其中之一。在肺癌细胞中,活化的YAP–TEAD2复合体直接结合NSUN2基因的启动子区域并上调NSUN2的产生。反过来,这会增加YAP RNA上的m5C标记,进一步稳定并放大YAP自身的表达。这形成了一个正反馈环:更多的YAP导致更多的NSUN2,进而产生更多的YAP,将细胞锁定在高生长、促转移的状态。研究者认为破坏这一循环可能是减缓NSCLC进展的有力策略。
针对肺肿瘤的新途径
由于酶和RNA结合蛋白可以被小分子靶向,团队测试了干扰NSUN2催化活性和降低YBX1水平的实验性抑制剂。在肺癌细胞系中,每种化合物都降低了YAP蛋白、放慢细胞生长、抑制迁移与侵袭,并使细胞趋向于较不具侵袭性的状态。在小鼠模型中,两药合用比单用任何一种都更能缩小肿瘤并减少肺内转移病灶。重要的是,这些药物在培养的正常肺细胞中几乎不产生有害影响,暗示存在潜在的治疗窗口。
对患者可能意味着什么
对非专业读者来说,关键的信息是:这项研究揭示了肺癌细胞用来放大一个中心生长信号的特定分子回路。NSUN2在YAP信息上加化学标记,ALYREF与YBX1保护并促进其翻译,而YAP又反过来增强NSUN2,形成一个失控的循环,助长肿瘤生长与扩散。通过证明在细胞和小鼠中阻断NSUN2的标记功能和YBX1的支持作用可以打破该循环,工作为未来在RNA水平而非仅直接针对DNA或蛋白的药物奠定了基础。尽管这些化合物仍处于临床前阶段,但靶向促进癌症的RNA上的m5C标记这一概念为对抗NSCLC提供了新的思路。
引用: Li, R., Jin, D., Shao, S. et al. NSUN2 promoted tumor growth and metastatic via m5C-regulation of YAP through ALYREF/YBX1 axis in NSCLC. Cell Death Dis 17, 299 (2026). https://doi.org/10.1038/s41419-025-08353-x
关键词: 非小细胞肺癌, RNA修饰, YAP信号, NSUN2, 转移