Clear Sky Science · tr
NSUN2, NSCLC’de ALYREF/YBX1 ekseni üzerinden YAP’ın m5C-düzenlemesi ile tümör büyümesini ve metastazı teşvik etti
Bu akciğer kanseri çalışması neden önemli
Akciğer kanseri dünya çapında en ölümcül kanserdir ve ölümlerin çoğu genellikle erken saptanmadan yayılan non-müsküler hücreli akciğer kanseri (NSCLC) kaynaklıdır. Bu çalışma, akciğer tümörlerinin büyümesine ve vücuda metastaz tohumları ekmesine yardımcı olan moleküler “devreyi” inceliyor. Kanser hücreleri içinde güçlü bir büyüme anahtarını artıran belirli bir moleküler zinciri ortaya koyarak, sağlıklı dokuya zarar vermeden hastalığı yavaşlatabilecek veya durdurabilecek yeni ilaç hedeflerine işaret ediyor.
Kanser hücrelerinde gizli bir denetim katmanı
Genlerimiz DNA’da taşınır, ancak hücrelere hangi proteinleri ne zaman yapacaklarını söyleyen çalışan kopya RNA’dır. Son yıllarda, RNA’ların kendilerinin de yazının kenarına alınmış notlar gibi kimyasal işaretler taşıdığı ve bunların RNA’ların ne kadar süre kaldığını ve ne kadar verimli okunacağını değiştirebildiği keşfedildi. Bu işaretlerden biri m5C olarak adlandırılır; RNA’daki sitozin bazına konulan küçük bir kimyasal etikettir. Bu çalışma, NSCLC’de NSUN2 adlı bir enzimin YAP’ı kodlayan RNA’ya ekstra m5C işaretleri eklediğini gösteriyor; YAP büyüme ve hayatta kalmanın ana düzenleyicisidir. Hastalardan alınan tümörlerde yakın normal dokuya göre daha yüksek NSUN2 ve YAP düzeyleri görüldü ve bu proteinlerden daha fazla olan hastalar genellikle daha kötü sonuçlar aldı.
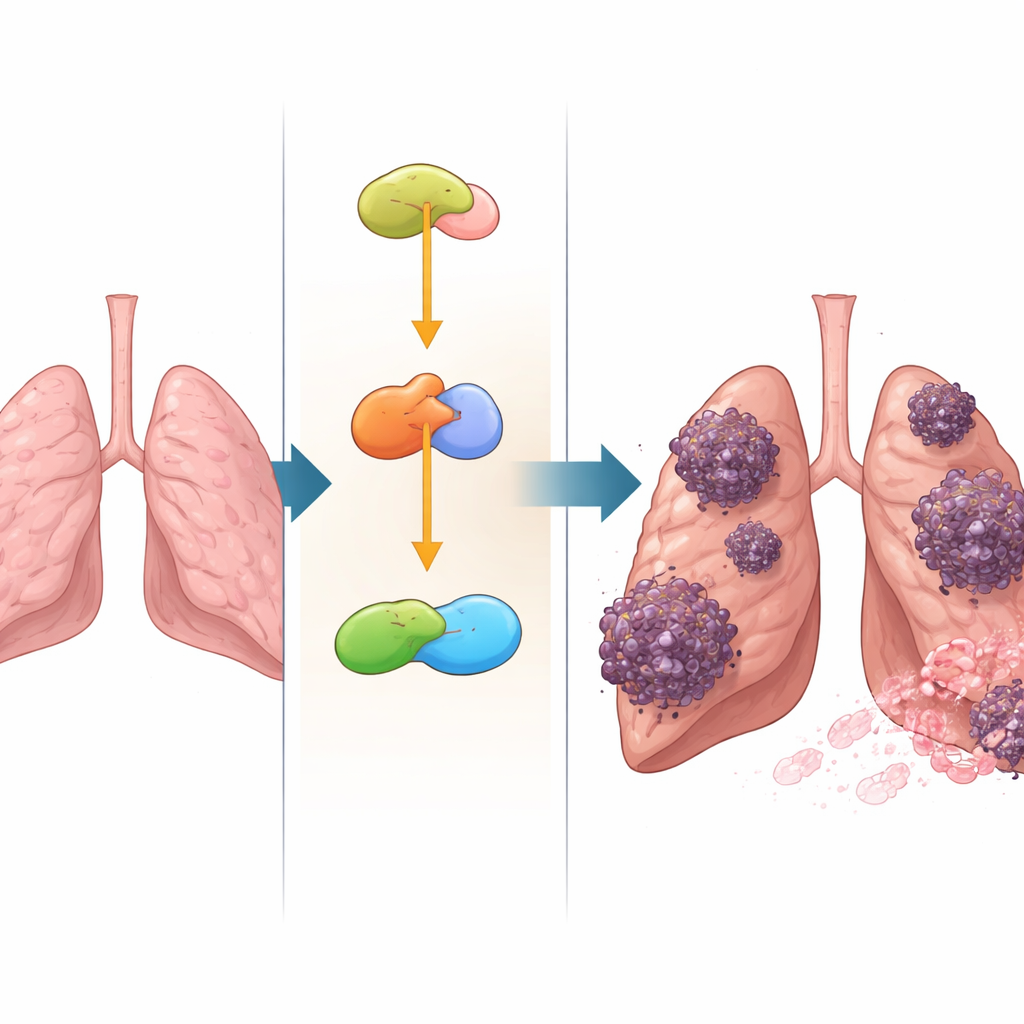
Tehlikeli bir büyüme anahtarını açmak
YAP, hücre çoğalması, hareketi ve şekil değişimi için merkezi bir gaz kolu gibi çalışır. Aşırı etkin olduğunda hücreleri daha hızlı bölünmeye, çevre dokuya saldırmaya ve metastaz oluşturmak için kopmaya zorlayabilir. Araştırmacılar NSUN2 ve YAP’ın NSCLC hücrelerinde hücre bölünmesini, göçü, yapay bariyerlerden geçme yeteneğini ve hücrelerin bağlantılarını gevşetip daha hareketli hâle geldiği epitel–mezenkimal geçiş sürecini güçlendirdiğini buldular. Farelerde, akciğer kanseri hücrelerini ekstra NSUN2 üretecek şekilde mühendislik etmek daha büyük, daha agresif tümörlere ve akciğerlerde daha fazla metastatik noktaya yol açtı; YAP’ı azaltmak bu etkileri zayıflattı. Bu, NSUN2’nin tümör büyümesi üzerindeki etkisinin büyük ölçüde YAP seviyelerini yükseltme yeteneğine bağlı olduğunu gösterdi.
Kanser mesajlarını koruyan bir röle takımı
NSUN2 tek başına hareket etmez. YAP RNA’sına m5C işaretleri koyduktan sonra iki RNA-bağlayan protein, ALYREF ve YBX1, değişmiş mesajı tanır ve ona bağlanır. Çalışma bir röleyi ortaya koyuyor: ALYREF önce işaretli RNA’yı tespit eder, sonra onu YBX1’e aktarır ve birlikte NSUN2 ile üç parçalı bir kompleks oluştururlar. Bu kompleks, genellikle istenmeyen mesajları parçalaymaya yardımcı olan AGO2 proteininden YAP RNA’sını korur ve aynı zamanda RNA’yı proteine çeviren çeviri mekanizmasını da devreye almayı kolaylaştırır. Sonuç olarak YAP RNA’sı daha uzun süre kalır ve daha verimli şekilde çevrilir; hücre YAP proteiniyle dolup taşar. Aşağı akımda YAP, hücre döngüsü ilerlemesini, istila yeteneklerini ve doku yeniden şekillendirme enzimlerini etkinleştirir; bunların hepsi agresif kanserin ayırt edici özellikleridir.
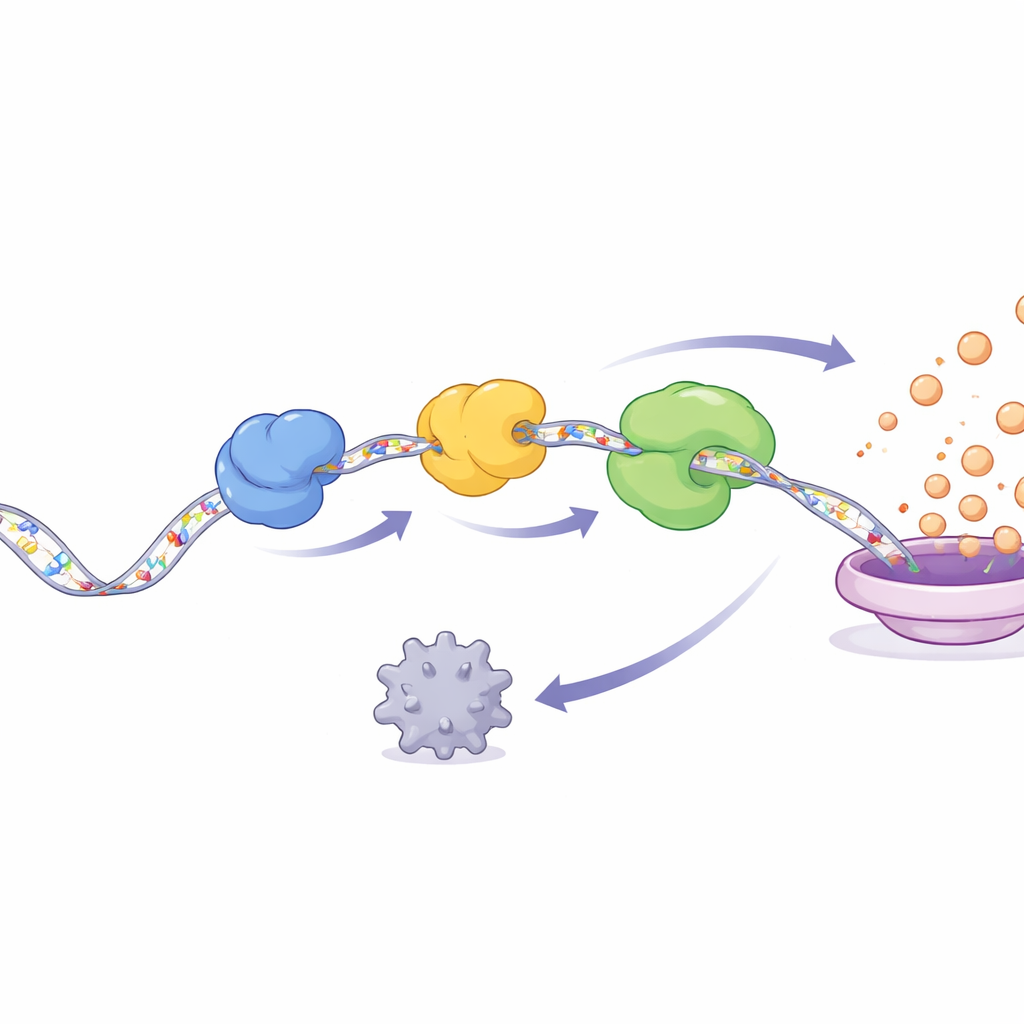
Kendini pekiştiren bir kanser döngüsü
Çarpıcı biçimde ilişki çift yönlüdür. YAP, birçok geni açmak için DNA’ya bağlanan TEAD2 adlı bir proteinle ortaklık kurar ve ekip NSUN2’nin bu genlerden biri olduğunu buldu. Akciğer kanseri hücrelerinde aktif YAP–TEAD2 doğrudan NSUN2 promotör bölgesine bağlanır ve NSUN2 üretimini artırır. Bu da YAP RNA’sında daha fazla m5C işareti oluşmasına yol açar, böylece YAP daha da kararlı hale gelir ve artar. Bu olumlu geri besleme döngüsü: daha fazla YAP daha fazla NSUN2’ye yol açar, o da daha fazla YAP üretir ve hücreleri yüksek büyüme, pro-metastatik bir duruma kilitler. Araştırmacılar bu döngüyü bozmanın NSCLC ilerlemesini yavaşlatmak için güçlü bir yol olabileceğini savunuyor.
Akciğer tümörlerini hedeflemenin yeni yolları
Enzimler ve RNA-bağlayan proteinler küçük moleküllerle hedeflenebildiğinden ekip, NSUN2’nin katalitik aktivitesini engelleyen ve YBX1 düzeylerini düşüren deneysel inhibitörleri test etti. Akciğer kanseri hücre hatlarında her bir bileşik YAP proteinini azalttı, hücre büyümesini yavaşlattı, hareket ve istila yeteneklerini kısıtladı ve hücreleri daha az invaziv bir duruma itti. Fare modellerinde her iki ilacı birlikte kullanmak tek başına olandan daha fazla tümör küçülmesi sağladı ve akciğerdeki metastatik lezyonları azalttı. Önemli olarak, bu ajanlar kültürdeki normal akciğer hücrelerine fazla zarar vermedi; bu da potansiyel bir terapötik pencereye işaret ediyor.
Bu hastalar için ne anlama gelebilir
Uzman olmayan biri için ana mesaj, bu çalışmanın akciğer kanseri hücrelerinin merkezi bir büyüme sinyalini yükseltmek için kullandığı spesifik bir moleküler devreyi ortaya koymasıdır. NSUN2 YAP mesajını kimyasal olarak etiketler, ALYREF ve YBX1 bunu korur ve çevirir, YAP ise karşılık olarak NSUN2’yi artırır ve hızlanan bir döngü tümör büyümesini ve yayılımı besler. NSUN2’nin işaretleme fonksiyonunu ve YBX1’in destek rolünü engellemenin bu döngüyü hücrelerde ve farelerde kırabildiğini göstererek çalışma, DNA veya yalnızca proteinler yerine RNA düzeyinde hareket eden gelecekteki ilaçlar için zemin hazırlıyor. Bu bileşikler hâlâ preklinik aşamada olsa da, kanser teşvik edici RNA’lardaki m5C işaretlerini hedefleme fikri NSCLC ile mücadelede taze bir açı sunuyor.
Atıf: Li, R., Jin, D., Shao, S. et al. NSUN2 promoted tumor growth and metastatic via m5C-regulation of YAP through ALYREF/YBX1 axis in NSCLC. Cell Death Dis 17, 299 (2026). https://doi.org/10.1038/s41419-025-08353-x
Anahtar kelimeler: non-small cell lung cancer, RNA modification, YAP signaling, NSUN2, metastasis