Clear Sky Science · pt
NSUN2 promoveu crescimento tumoral e metástase via regulação por m5C de YAP através do eixo ALYREF/YBX1 em NSCLC
Por que este estudo sobre câncer de pulmão é importante
O câncer de pulmão é o mais letal no mundo, e a maioria das mortes decorre do câncer de pulmão não pequenas células (NSCLC), que frequentemente se dissemina antes de ser detectado. Este estudo investiga a "fiação" molecular que ajuda tumores pulmonares a crescer e a semear metástases pelo corpo. Ao revelar uma cadeia específica de moléculas que aumenta um potente interruptor de crescimento dentro das células cancerosas, a pesquisa aponta para novos alvos farmacológicos que poderiam retardar ou interromper a doença poupando o tecido saudável.
Uma camada oculta de controle nas células cancerosas
Nossos genes estão no DNA, mas é o RNA — a cópia ativa da informação genética — que diz às células quais proteínas fabricar e quando. Nos últimos anos, cientistas descobriram que os próprios RNAs carregam marcas químicas, como notas nas margens de um roteiro, que podem alterar quanto tempo duram e com que intensidade são lidos. Uma dessas marcas é chamada m5C, uma pequena etiqueta química colocada na base de RNA citosina. Este trabalho mostra que no NSCLC, uma enzima chamada NSUN2 adiciona marcas m5C extras ao RNA que codifica YAP, um regulador mestre de crescimento e sobrevivência. Tumores de pacientes apresentaram níveis mais altos de NSUN2 e YAP do que tecido normal adjacente, e pacientes com mais de qualquer uma dessas proteínas tendiam a ter pior prognóstico.
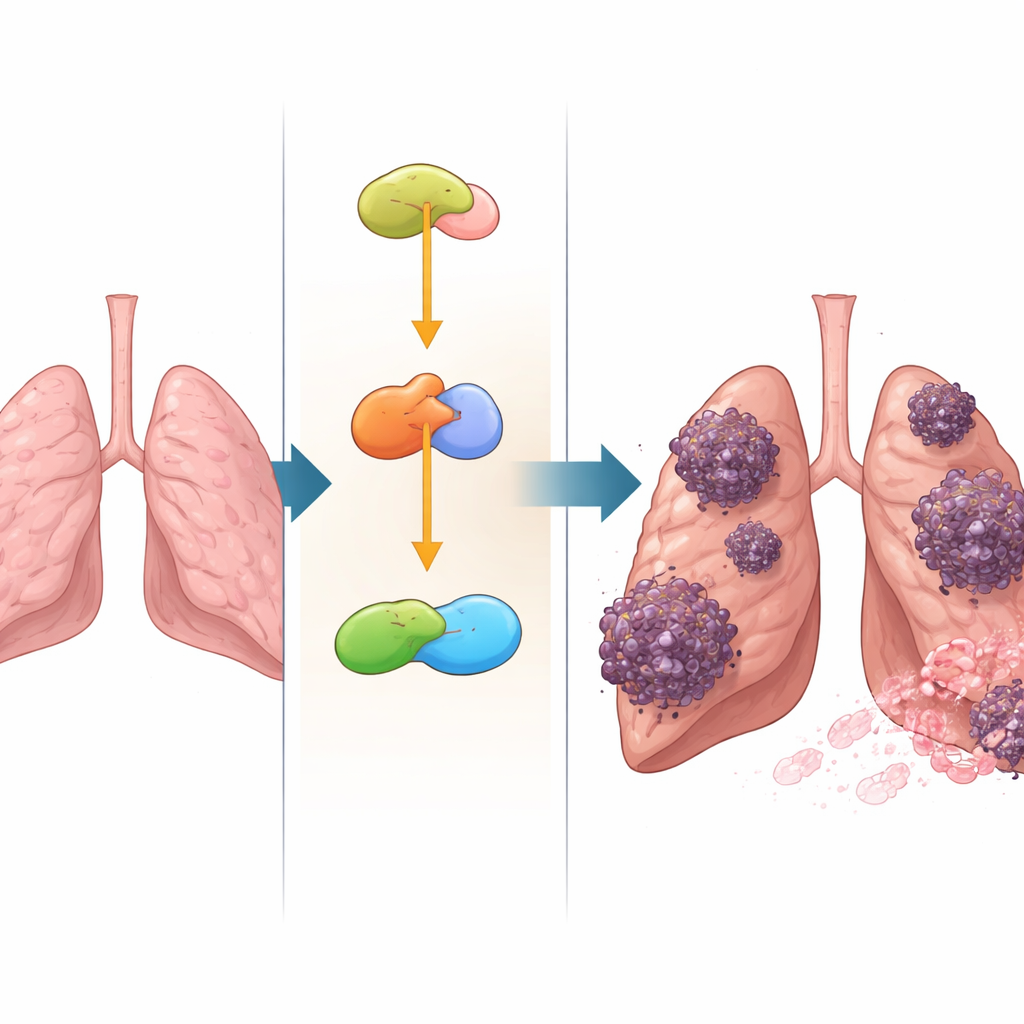
Ativando um perigoso interruptor de crescimento
YAP atua como um acelerador central para proliferação celular, movimento e mudança de forma. Quando hiperativo, pode empurrar as células a se dividirem mais rápido, invadir tecidos vizinhos e se desprender para formar metástases. Os pesquisadores descobriram que NSUN2 e YAP impulsionam muitos dos mesmos comportamentos cancerígenos em células de NSCLC: aumento da divisão celular, migração, invasão através de barreiras artificiais e um processo chamado transição epitélio–mesênquima, no qual as células afrouxam suas conexões e se tornam mais móveis. Em camundongos, a engenharia de células de câncer de pulmão para produzirem NSUN2 em excesso levou a tumores maiores e mais agressivos e a mais focos metastáticos nos pulmões, enquanto reduzir YAP atenuou esses efeitos. Isso mostrou que o impacto do NSUN2 no crescimento tumoral depende fortemente da sua capacidade de elevar os níveis de YAP.
Uma equipe de revezamento que protege as mensagens do câncer
NSUN2 não age sozinho. Uma vez que coloca marcas m5C no RNA de YAP, duas proteínas ligadoras de RNA, ALYREF e YBX1, reconhecem e se prendem à mensagem modificada. O estudo revela um revezamento: ALYREF primeiro detecta o RNA marcado, depois o passa para YBX1, e juntos formam um complexo tripartite com NSUN2. Esse complexo protege o RNA de YAP da AGO2, uma proteína que normalmente ajuda a degradar mensagens indesejadas, e também contribui para recrutar a maquinaria de tradução que converte RNA em proteína. O resultado é que o RNA de YAP persiste por mais tempo e é traduzido de forma mais eficiente, inundando a célula com a proteína YAP. A jusante, YAP ativa genes que promovem progressão do ciclo celular, invasão e enzimas de remodelamento tecidual, todos marcos do câncer agressivo.
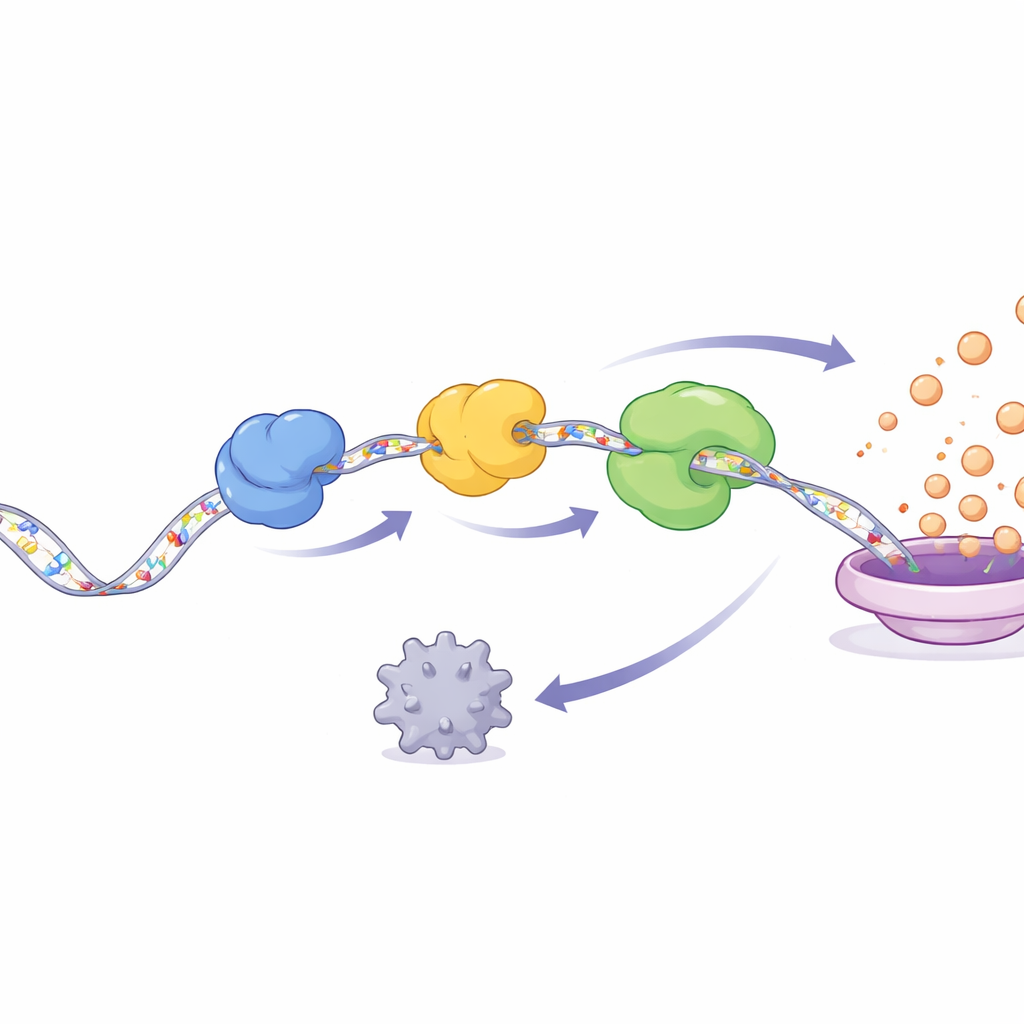
Um ciclo cancerígeno autorreforçador
De forma notável, a relação funciona em ambos os sentidos. YAP faz parceria com uma proteína que se liga ao DNA chamada TEAD2 para ativar muitos genes, e a equipe descobriu que NSUN2 é um deles. Em células de câncer de pulmão, o complexo ativo YAP–TEAD2 liga-se diretamente à região promotora do NSUN2 no DNA e aumenta a produção de NSUN2. Isso, por sua vez, aumenta as marcas m5C no RNA de YAP, estabilizando e amplificando ainda mais o próprio YAP. Isso cria um circuito de feedback positivo: mais YAP leva a mais NSUN2, o que gera ainda mais YAP, prendendo as células em um estado de alto crescimento e pró-metastático. Interromper esse circuito, argumentam os pesquisadores, poderia ser uma forma poderosa de desacelerar a progressão do NSCLC.
Novas maneiras de alvejar tumores pulmonares
Como enzimas e proteínas ligadoras de RNA podem ser alvo de pequenas moléculas, a equipe testou inibidores experimentais que interferem na atividade catalítica do NSUN2 e reduzem os níveis de YBX1. Em linhagens de células de câncer de pulmão, cada composto diminuiu a proteína YAP, retardou o crescimento celular, reduziu movimento e invasão, e empurrou as células de volta a um estado menos invasivo. Em modelos murinos, usar ambos os fármacos juntos encolheu tumores mais do que cada um isoladamente e reduziu as lesões metastáticas nos pulmões. Importante, esses agentes pouco prejudicaram células pulmonares normais em cultura, sugerindo uma possível janela terapêutica.
O que isso pode significar para pacientes
Para um público não especialista, a mensagem principal é que este estudo revela um circuito molecular específico que células de câncer de pulmão usam para amplificar um sinal central de crescimento. NSUN2 marca quimicamente a mensagem de YAP, ALYREF e YBX1 a protegem e a traduzem, e YAP por sua vez aumenta NSUN2, criando um ciclo em aceleração que alimenta o crescimento e a disseminação do tumor. Ao mostrar que bloquear a função de marcação do NSUN2 e o papel de suporte do YBX1 pode quebrar esse ciclo em células e em camundongos, o trabalho prepara o terreno para futuros fármacos que atuem ao nível do RNA em vez de diretamente no DNA ou somente nas proteínas. Embora esses compostos ainda estejam em estágio pré-clínico, o conceito de mirar marcas m5C em RNAs promotores de câncer oferece um ângulo novo na luta contra o NSCLC.
Citação: Li, R., Jin, D., Shao, S. et al. NSUN2 promoted tumor growth and metastatic via m5C-regulation of YAP through ALYREF/YBX1 axis in NSCLC. Cell Death Dis 17, 299 (2026). https://doi.org/10.1038/s41419-025-08353-x
Palavras-chave: câncer de pulmão não pequenas células, modificação de RNA, sinalização YAP, NSUN2, metástase