Clear Sky Science · zh
在BCMA靶向CAR-T细胞治疗后管理血液学毒性
这对血液癌症患者为何重要
对于难治性的血液癌症多发性骨髓瘤患者,新兴的“活体药物”——CAR-T细胞在其他治疗失效时带来了希望。但与其显著的抗癌能力并存的是一个严重的不良后果:许多患者的血细胞计数显著下降并长期维持在低位,使他们易感染并需频繁输血。本研究提出了一个患者和医生都关心的实用问题:我们能否预测谁最易出现这些血液问题,从而围绕该风险更好地安排日常护理?
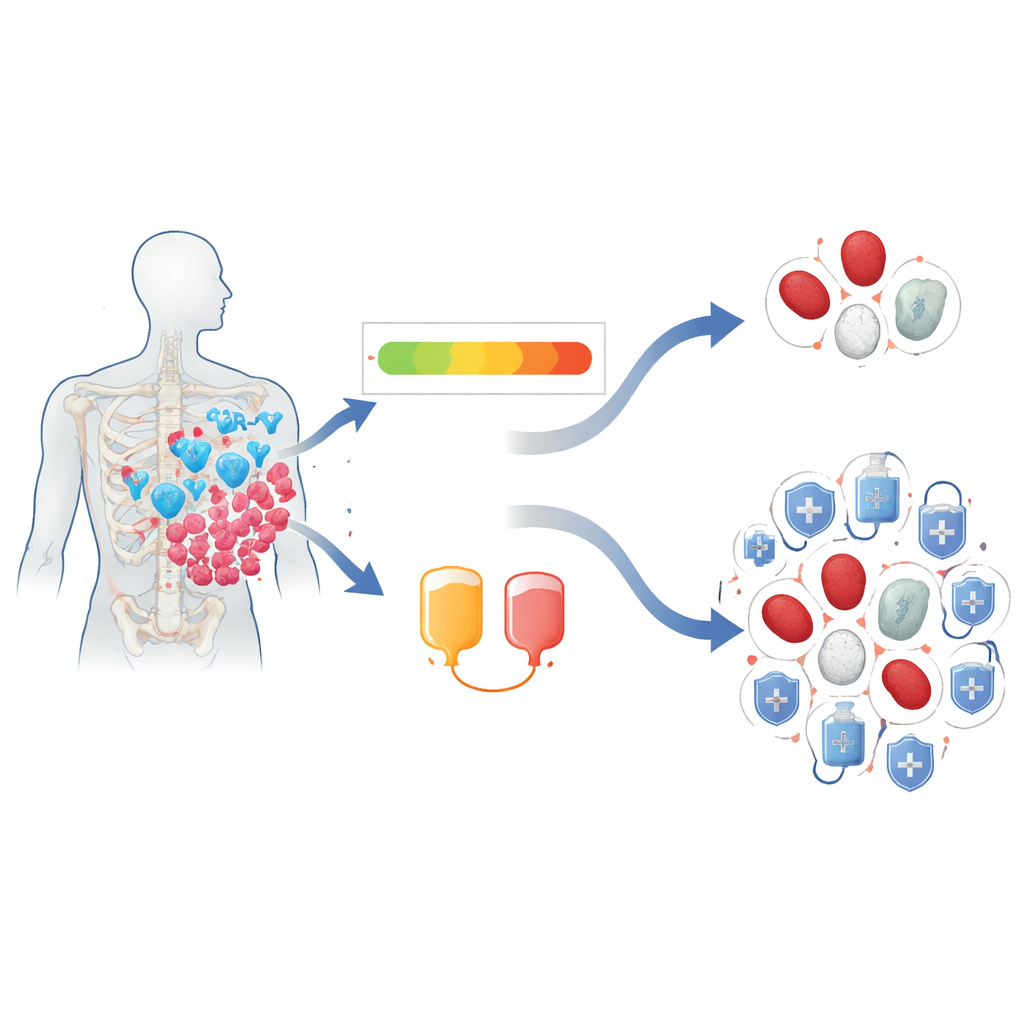
标记脆弱血液系统的评分
研究者关注一种称为CAR-HEMATOTOX(CAR-HT)的工具,该评分在CAR-T治疗前通过常规血液检查和炎症标志物计算得出。他们回顾了2016年至2024年间在梅奥诊所接受BCMA靶向CAR-T治疗的224例复发或难治性多发性骨髓瘤成年患者的病历。患者被分为“低分”和“高分”组,反映其骨髓(制造血细胞的“工厂”)看起来更健壮或更脆弱。研究组随后跟踪了患者出现红细胞、白细胞和血小板低下的频率与严重程度、恢复所需时间、所用的支持性治疗以及这些情况是否影响长期生存。
谁在CAR-T后最吃力
高CAR-HT评分的患者起始血象较差,在CAR-T治疗后出现更为严重的血细胞下降。他们发生严重且长期血细胞骤降的比率约为低评分患者的两倍,这一并发症现在称为免疫效应细胞相关血液毒性(ICAHT)。与低评分患者相比,高评分患者更易发生严重贫血和极低血小板,并在治疗后六个月内需要更多次红细胞与血小板输注。其中一小部分患者累积了惊人的输血次数,显示出对最脆弱人群而言负担有多沉重。感染——尤其是细菌感染和某些病毒感染——在高评分患者中也更常见,反映出其免疫系统长期处于虚弱状态。
支持性治疗的实际效果
为处理这些问题,医生采取了多种策略。许多患者接受了刺激白细胞生长的注射(G-CSF);少数患者使用促进血小板生成的药物;还有一小部分出现顽固性多系低下的患者接受了先前采集并保存的自体造血干细胞的额外输注,称为造血干细胞“增援”。造血干细胞增援仅用于约4%的患者,但特别有效,可在数周内恢复三系血细胞。相比之下,当原发骨髓瘤进展时,促血小板药物常常无效,这表明持续性低血小板可能是癌症复发的预警,而不仅仅是治疗副作用。
风险并不等同于更差的生存期
尽管高评分患者在输血、感染和支持性治疗方面负担更重,但在本研究中,他们的无进展生存期和总体生存期并未明显逊于低评分患者。不同的支持策略亦是如此:无论患者仅需输血、使用生长因子或接受造血干细胞增援,这些措施似乎都不会显著缩短或延长CAR-T对癌症的控制时间。这表明CAR-HT评分主要作为一个对恢复期粗糙程度的警示,而非预测癌症治疗效果的指标。
对患者及其医生的意义
简言之,这项研究表明,在CAR-T治疗前计算的一个简单评分可以可靠地提示谁更可能面临更严重的血液相关副作用和更高的输血需求。了解患者的CAR-HT评分可帮助医疗团队做好准备:安排更密切的监测、提前计划使用生长因子、考虑备份的造血干细胞,并在恢复期间向患者说明预期。同时,好消息是即便评分较高的患者仍可能从CAR-T治疗中获得相似的总体获益。该评分更关乎患者在治疗过程中骨髓需要多少支持,而不是CAR-T是否有效。
引用: Cook, J., Gupta, S., Abdallah, N. et al. Management of hematological toxicities after BCMA-directed CAR-T cell therapy. Blood Cancer J. 16, 49 (2026). https://doi.org/10.1038/s41408-026-01455-5
关键词: CAR-T疗法, 多发性骨髓瘤, 细胞减少症, 支持性治疗, 造血干细胞增援