Clear Sky Science · ar
إدارة السُمّيات الدموية بعد علاج الخلايا التائية المعدّلة CAR‑T الموجّهة ضد BCMA
لماذا يهم هذا الأشخاص المصابين بسرطان الدم
بالنسبة للأشخاص المصابين بالمايلوما المتعددة، وهو سرطان دم يصعب علاجه، قدّمت الأدوية "الحية" الجديدة المسماة خلايا CAR‑T أملاً عندما تتوقف العلاجات الأخرى عن العمل. لكن إلى جانب قدرتها المذهلة على مكافحة السرطان، هناك جانب سلبي خطير: انخفاض عدد خلايا الدم لدى العديد من المرضى وبقاؤها منخفضة، ما يجعلهم عرضة للعدوى والحاجة المتكررة لعمليات نقل الدم. تسأل هذه الدراسة سؤالاً عملياً يهم المرضى والأطباء معًا: هل يمكننا التنبؤ بمن هم الأكثر عرضة لهذه المشاكل الدموية والتخطيط لرعاية يومية أفضل بناءً على ذلك الخطر؟
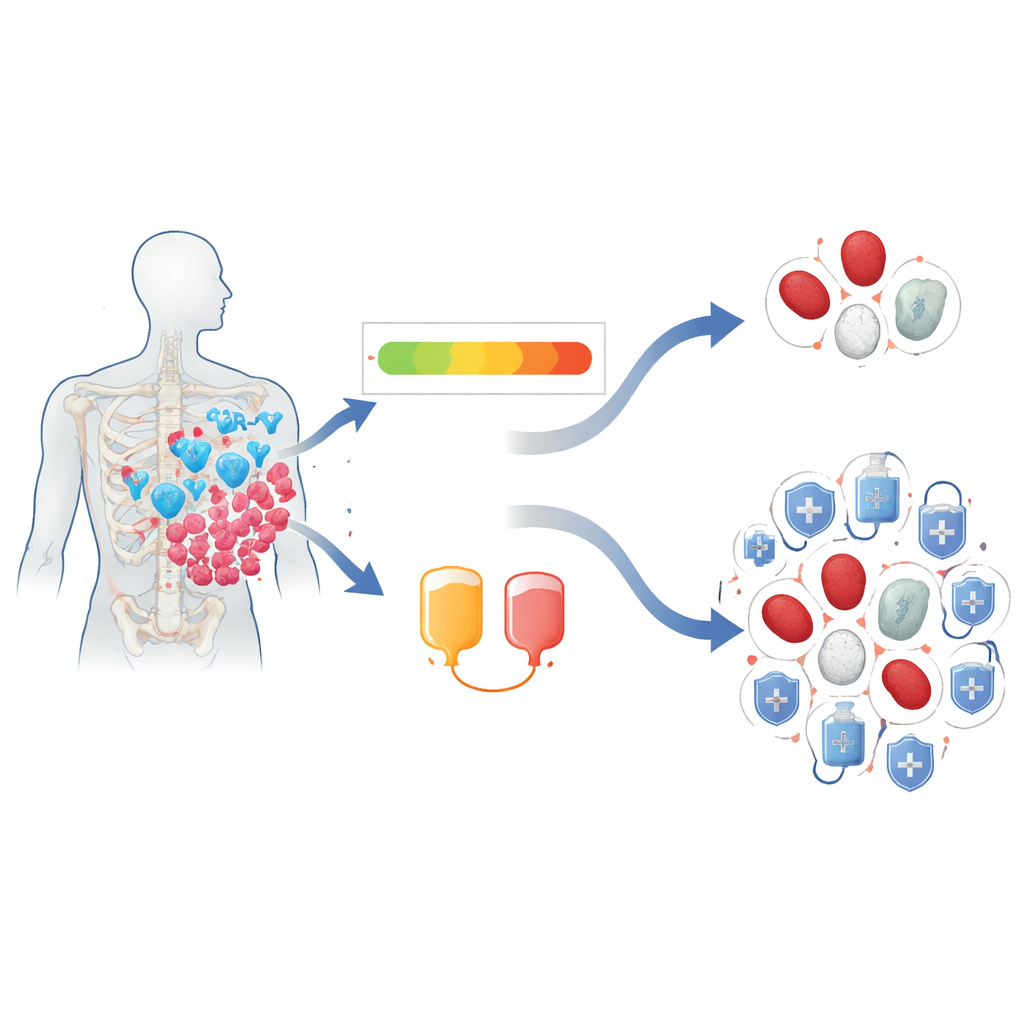
مقياس يضيء على الأنظمة الدموية الهشّة
ركز الباحثون على أداة تُدعى مقياس CAR‑HEMATOTOX (CAR‑HT)، والذي يُحسَب قبل علاج CAR‑T مباشرةً بالاعتماد على فحوصات دم روتينية وعلامات الالتهاب. راجعوا سجلات 224 بالغًا مصابين بالمايلوما المتعددة المنتكسـة أو المقاومة للعلاج والذين تلقوا علاج CAR‑T الموجّه ضد BCMA في مايو كلينك بين 2016 و2024. جُمِّع المرضى في مجموعتي "منخفض" و"مرتفع" بحسب نتيجة CAR‑HT، مما يعكس مدى قوة أو هشاشة نخاع العظم — المصنع الذي يصنع خلايا الدم. ثم تتبّع الفريق كم مرة وبأي شدة ظهر لدى المرضى انخفاض في خلايا الدم الحمراء والبيضاء والصفائح، ومدة التعافي، والعلاجات الداعمة المستخدمة، وما إذا كان لأي من ذلك تأثير على البقاء على المدى الطويل.
من يواجه صعوبات أكثر بعد CAR‑T
بدأ مرضى الفئة العالية بنتائج دم أضعف وتعرضوا لانخفاضات أكثر حدة بعد CAR‑T. كان لديهم تقريبًا ضعف معدل الانهيارات الشديدة والممتدة لعدّ خلايا الدم، وهي حالة تُسمى الآن السُمّية الدموية المرتبطة بخلايا التأثير المناعي (ICAHT). مقارنةً بمرضى الفئة المنخفضة، كانوا أكثر عرضة للإصابة بفقر دم شديد وانخفاض شديد في الصفائح، واحتاجوا إلى عدد أكبر من نقلات الدم وخزعات الصفائح خلال الأشهر الستة التي تلت العلاج. تراكمت مجموعة صغيرة من المرضى على عدد كبير من عمليات النقل، مما يبرهن على شدة العبء بالنسبة لأكثر الفئات ضعفًا. كما كانت العدوى — خاصة البكتيرية وبعض العدوى الفيروسية — أكثر تواترًا لدى المرضى ذوي النتيجة العالية، ما يعكس فترات مطوّلة من ضعف جهازهم المناعي.
ما فعله العلاجات الداعمة فعلاً
لإدارة هذه المشكلات استخدم الأطباء استراتيجيات مختلفة. تلقى كثير من المرضى حقنة لتحفيز خلايا الدم البيضاء (G‑CSF)؛ وحصل عدد قليل على أدوية تحفز نمو الصفائح؛ وحصلت مجموعة صغيرة ذات نقص متعدد السلالات عنيدة على تسريب إضافي لخلاياهم الجذعية المجمعة سابقًا، يُسمّى "تعزيز" بالخلايا الجذعية. كان للتعزيزات بالخلايا الجذعية — المستخدمة في نحو 4% فقط من المرضى — تأثير خاص، إذ أدت إلى تعافٍ لجميع أنواع خلايا الدم الثلاثة خلال بضعة أسابيع. بالمقابل، غالبًا ما فشلت أدوية تحفيز الصفائح عندما كان المايلوما تتقدم، مشيرة إلى أن استمرار انخفاض الصفائح قد يكون علامة تحذيرية على عودة السرطان بدلاً من كونه أثرًا جانبيًا فقط.
الخطورة لا تعني بالضرورة بقاءًا أسوأ
رغم العبء الأكبر من نقلات الدم والعدوى والرعاية الداعمة، لم يظهر لدى مرضى الفئة العالية بالضرورة بقاء دون تقدم أو بقاء كلي أسوأ مقارنة بمرضى الفئة المنخفضة في هذه الدراسة. وكان الحال نفسه بالنسبة لاستراتيجيات الدعم المختلفة: سواء احتاج المرضى إلى نقلات فقط، أو عوامل نمو، أو تعزيز بالخلايا الجذعية، لم تظهر هذه الإجراءات أنها تقصر أو تطيل المدة التي يبقى فيها العلاج CAR‑T مسيطراً على السرطان. وهذا يشير إلى أن مقياس CAR‑HT يعمل بشكل أساسي كتحذير لطبيعة فترة التعافي وصعوبتها، أكثر منه كمؤشر على فعالية علاج السرطان.
ماذا يعني هذا للمرضى وأطبائهم
ببساطة، تُظهر هذه الدراسة أن مقياسًا بسيطًا يحسب قبل علاج CAR‑T يمكنه أن يميّز بشكل موثوق من هم الأرجح أن يواجهوا آثارًا جانبية دموية أصعب وحاجات نقل دم أكبر. معرفة نتيجة CAR‑HT للمريض يمكن أن تساعد الفرق على الاستعداد: تنظيم مراقبة أقرب، والتخطيط لاستخدام مبكر لعوامل النمو، والنظر في وجود خلية جذعية احتياطية، وتوجيه المرضى لما يمكن توقعه أثناء التعافي. وفي الوقت نفسه، الخبر الجيد هو أن من لديهم نتائج عالية لا يزال بإمكانهم الحصول على فائدة إجمالية مماثلة من CAR‑T ضد السرطان. المقياس أقل بشأن ما إذا كان CAR‑T سينجح، وأكثر بشأن مقدار الدعم الذي سيحتاجه نخاع العظم خلال العلاج والتعافي.
الاستشهاد: Cook, J., Gupta, S., Abdallah, N. et al. Management of hematological toxicities after BCMA-directed CAR-T cell therapy. Blood Cancer J. 16, 49 (2026). https://doi.org/10.1038/s41408-026-01455-5
الكلمات المفتاحية: علاج CAR‑T, المايلوما المتعددة, نقص الخلايا الدموية, الرعاية الداعمة, تعزيز بالخلايا الجذعية