Clear Sky Science · de
Management hämatologischer Toxizitäten nach BCMA‑gerichteter CAR‑T‑Zelltherapie
Warum das für Menschen mit Blutkrebs wichtig ist
Für Patientinnen und Patienten mit multiplem Myelom, einem schwer zu behandelnden Blutkrebs, haben neue „lebende Medikamente“ namens CAR‑T‑Zellen Hoffnung gebracht, wenn andere Therapien versagen. Neben ihrer beeindruckenden krebsbekämpfenden Wirkung gibt es jedoch eine ernste Kehrseite: Bei vielen Patienten brechen die Blutwerte zusammen und bleiben niedrig, sodass sie anfälliger für Infektionen sind und häufig Transfusionen benötigen. Diese Studie stellt eine praktische Frage, die sowohl Patienten als auch Ärztinnen und Ärzte beschäftigt: Können wir vorhersagen, wer am stärksten für diese Blutprobleme gefährdet ist, und die Alltagsversorgung besser an dieses Risiko anpassen?
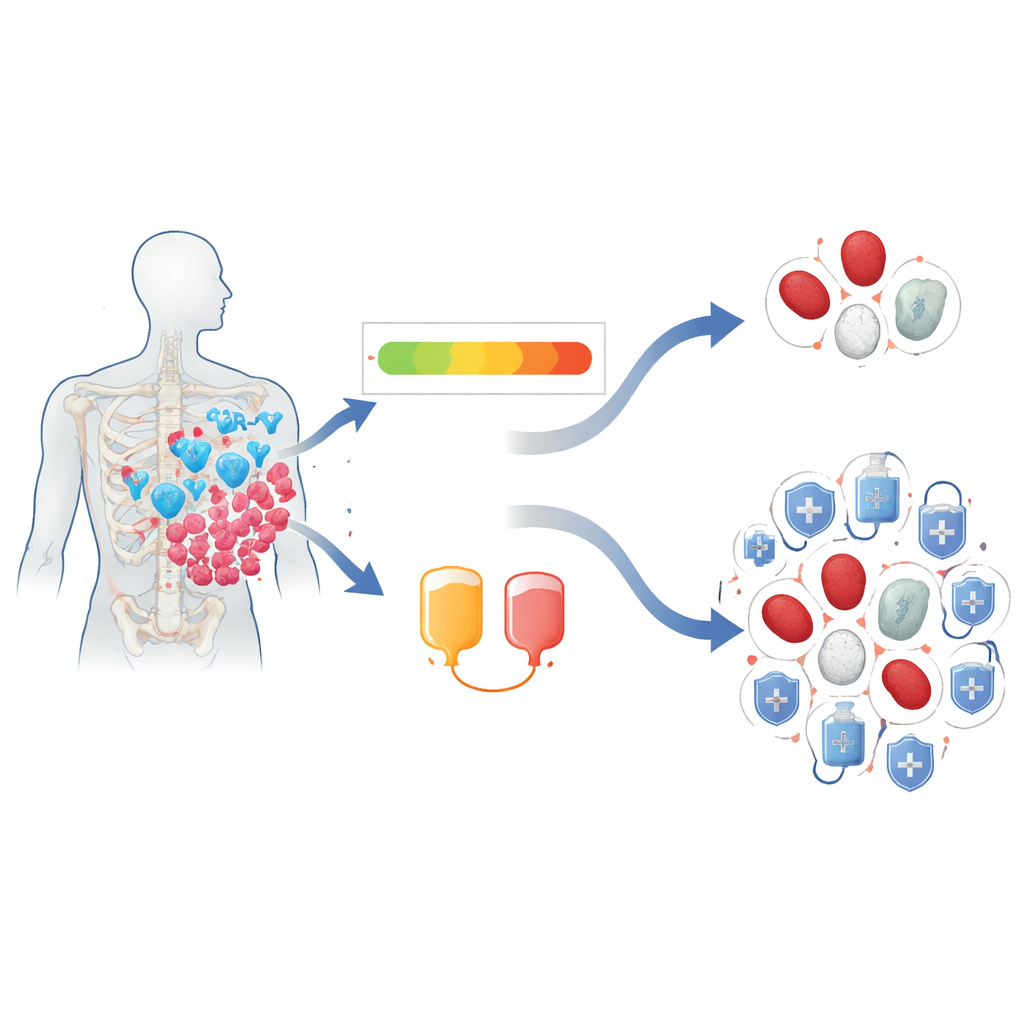
Ein Score, der fragile Blut‑Systeme markiert
Die Forschenden konzentrierten sich auf ein Instrument namens CAR‑HEMATOTOX (CAR‑HT)‑Score, der kurz vor der CAR‑T‑Therapie aus Routinebluttests und Entzündungsmarkern berechnet wird. Sie werteten die Unterlagen von 224 erwachsenen Patientinnen und Patienten mit rezidiviertem oder refraktärem multiplem Myelom aus, die zwischen 2016 und 2024 am Mayo Clinic eine BCMA‑gerichtete CAR‑T‑Therapie erhielten. Die Patienten wurden in „niedrigen“ und „hohen“ CAR‑HT‑Scores eingeteilt, je nachdem, wie robust oder fragil das Knochenmark — die Fabrik für Blutzellen — erschien. Das Team verfolgte dann, wie häufig und wie schwer Patienten Anämie, Leukozytopenie und Thrombozytopenie entwickelten, wie lange die Erholung dauerte, welche unterstützenden Behandlungen eingesetzt wurden und ob sich dies auf das Langzeitüberleben auswirkte.
Wer nach CAR‑T am meisten zu kämpfen hat
Patienten mit hohem CAR‑HT‑Score begannen mit schwächeren Blutwerten und erlebten nach der CAR‑T‑Therapie deutlich häufiger schwere Einbrüche. Sie hatten etwa doppelt so hohe Raten schwerer, lang anhaltender Blutbildstörungen, einer Komplikation, die nun als immune effector cell–associated hematotoxicity (ICAHT) bezeichnet wird. Im Vergleich zu Patienten mit niedrigem Score entwickelten sie deutlich häufiger schwere Anämien und sehr niedrige Thrombozytenzahlen und benötigten in den sechs Monaten nach der Behandlung viel mehr Transfusionen von Erythrozyten und Thrombozyten. Eine kleine Untergruppe akkumulierte eine auffallend hohe Anzahl an Transfusionen, was zeigt, wie intensiv die Belastung für die verwundbarsten Patienten sein kann. Infektionen — insbesondere bakterielle und bestimmte virale Infektionen — traten bei Patienten mit hohem Score ebenfalls häufiger auf, was die verlängerten Phasen widerspiegelt, in denen ihr Immunsystem geschwächt war.
Was unterstützende Behandlungen wirklich bewirken
Zur Bewältigung dieser Probleme setzten Ärztinnen und Ärzte verschiedene Strategien ein. Viele Patienten erhielten eine Injektion zur Stimulation der weißen Blutkörperchen (G‑CSF); einige erhielten Medikamente, die das Thrombozytenwachstum anregen; und eine kleine Gruppe mit hartnäckigen, multilineage Zytopenien erhielt eine zusätzliche Infusion ihrer zuvor gewonnenen eigenen Stammzellen, einen sogenannten Stammzell‑„Boost“. Die Stammzell‑Boosts — bei nur etwa 4 % der Patienten eingesetzt — waren besonders effektiv und führten innerhalb weniger Wochen zur Erholung aller drei großen Blutzelllinien. Im Gegensatz dazu schlugen Thrombozyten‑stimulierende Medikamente häufig fehl, wenn das zugrunde liegende Myelom progredierte, was darauf hinweist, dass persistierende Thrombozytopenie eher ein Warnzeichen für ein Wiederauftreten des Krebses als nur eine Nebenwirkung sein kann.
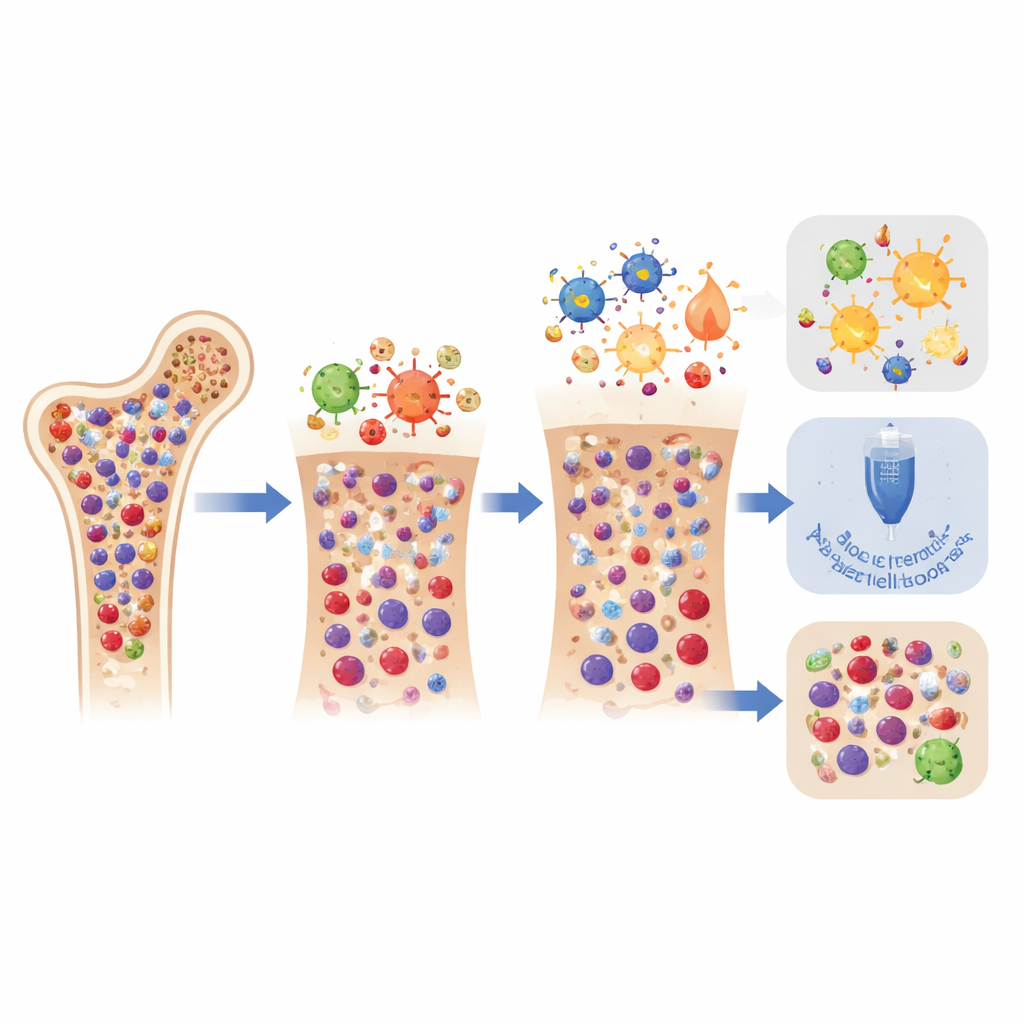
Risiko bedeutet nicht schlechteres Überleben
Trotz der höheren Belastung durch Transfusionen, Infektionen und supportive Maßnahmen hatten Patienten mit hohem Score in dieser Studie nicht klar schlechteres krankheitsfreies oder Gesamtüberleben als Patienten mit niedrigem Score. Gleiches galt für die verschiedenen Unterstützungsstrategien: Ob Patienten nur Transfusionen, Wachstumsfaktoren oder einen Stammzell‑Boost benötigten, diese Maßnahmen schienen weder die Dauer zu verkürzen noch zu verlängern, in der die CAR‑T‑Therapie den Krebs unter Kontrolle hielt. Das deutet darauf hin, dass der CAR‑HT‑Score vor allem als Warnsignal für einen schwierigeren Erholungsverlauf dient und weniger als Vorhersage dafür, wie wirksam die Krebsbehandlung sein wird.
Was das für Patienten und ihre Ärztinnen und Ärzte bedeutet
Einfach gesagt zeigt diese Arbeit, dass ein vor der CAR‑T‑Therapie berechneter, leichter ermittelbarer Score zuverlässig anzeigt, wer voraussichtlich stärkere blutbezogene Nebenwirkungen und höheren Transfusionsbedarf haben wird. Die Kenntnis des CAR‑HT‑Scores kann Teams helfen, sich besser vorzubereiten: engere Überwachung zu organisieren, den frühzeitigen Einsatz von Wachstumsfaktoren zu planen, eine Stammzell‑Reserve in Betracht zu ziehen und Patientinnen und Patienten realistischer über den Verlauf der Erholung aufzuklären. Gleichzeitig ist die gute Nachricht, dass selbst Personen mit hohem Score weiterhin ähnlich von der CAR‑T‑Therapie gegen ihren Krebs profitieren können. Der Score sagt weniger darüber aus, ob CAR‑T wirkt, als darüber, wie viel Unterstützung das Knochenmark einer Person während des Verlaufs benötigen wird.
Zitation: Cook, J., Gupta, S., Abdallah, N. et al. Management of hematological toxicities after BCMA-directed CAR-T cell therapy. Blood Cancer J. 16, 49 (2026). https://doi.org/10.1038/s41408-026-01455-5
Schlüsselwörter: CAR‑T‑Therapie, multiples Myelom, Zytopenie, supportive Versorgung, Stammzell‑Boost