Clear Sky Science · zh
葡萄糖响应性生物凝胶释放钒离子重塑巨噬细胞代谢以加速糖尿病创面修复
为何难愈合的糖尿病创面重要
对许多糖尿病患者来说,脚上的一个小水泡或划伤可能悄然演变为慢性、难以愈合的溃疡,带来感染、截肢甚至更严重的风险。这类伤口常常对常规敷料和抗生素抵抗性强,因为高血糖会悄悄扰乱局部免疫系统和能量供应。本研究探讨一种新型“智能”创面凝胶,它能在高葡萄糖条件下释放微量金属钒。目标是温和地重调关键免疫细胞的代谢,使它们从助长炎症的状态切换为积极重建组织的状态。
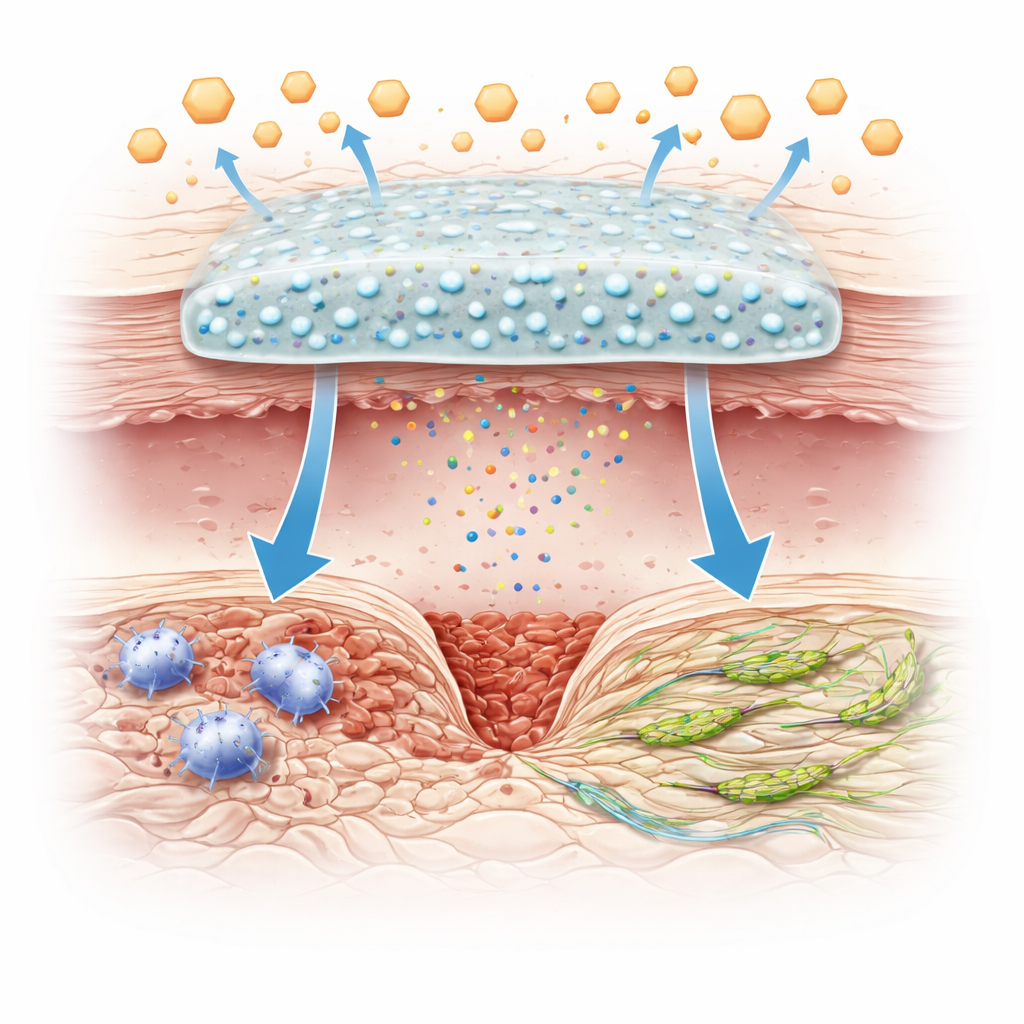
免疫细胞如何陷入困境
巨噬细胞是前线免疫细胞,同时也充当现场修复队。创伤早期它们呈现战士般的形态,攻击病原体并引发炎症;后期应当转为养护型,平息炎症并支持新组织生长。这个转变与细胞如何产生能量密切相关:促炎表型依赖快速的糖代谢,而促愈合表型则依赖于线粒体的较慢、需氧能量。在糖尿病创面中,持续的高糖和异常的胰岛素信号扰乱了这一能量开关,使巨噬细胞被困在愤怒的促炎模式,从而使创面长期处于慢性不愈合状态。
对糖敏感的智能凝胶
为了解决这一问题,研究者制备了含钒的微小玻璃状球体,由钙、硅、磷和钒的氧化物构成。这些球体被嵌入由改性明胶和一种对葡萄糖膨胀的壳聚糖基组分制成的软性水凝胶中。在类似糖尿病创面的高糖环境下,凝胶吸水膨胀,其内部网络松动,含钒颗粒和离子以可控方式释放。体外测试表明,将这些球体载入凝胶不会破坏其结构,反而增强了力学性能并实现了稳定的葡萄糖触发性钒释放。
加速糖尿病小鼠的创面修复
当该凝胶敷于糖尿病小鼠的全层皮肤伤口时,与未处理伤口或不含钒的凝胶相比,愈合显著改善。负载钒的敷料使伤口面积更快闭合,表皮再生更好,胶原沉积更有序,这些都是健康修复的标志。组织的化学代谢分析显示,该处理减少了与糖尿病相关的酸性代谢产物和其他代谢废物的堆积。同时,过度炎症的信号分子如TNF-α和IL-6下降,而抗炎信号和新生血管形成增加。巨噬细胞标志物染色显示,在早期时间点促愈合状态的细胞增加、促炎状态的细胞减少,表明凝胶是积极重塑免疫环境,而不仅仅是覆盖伤口。
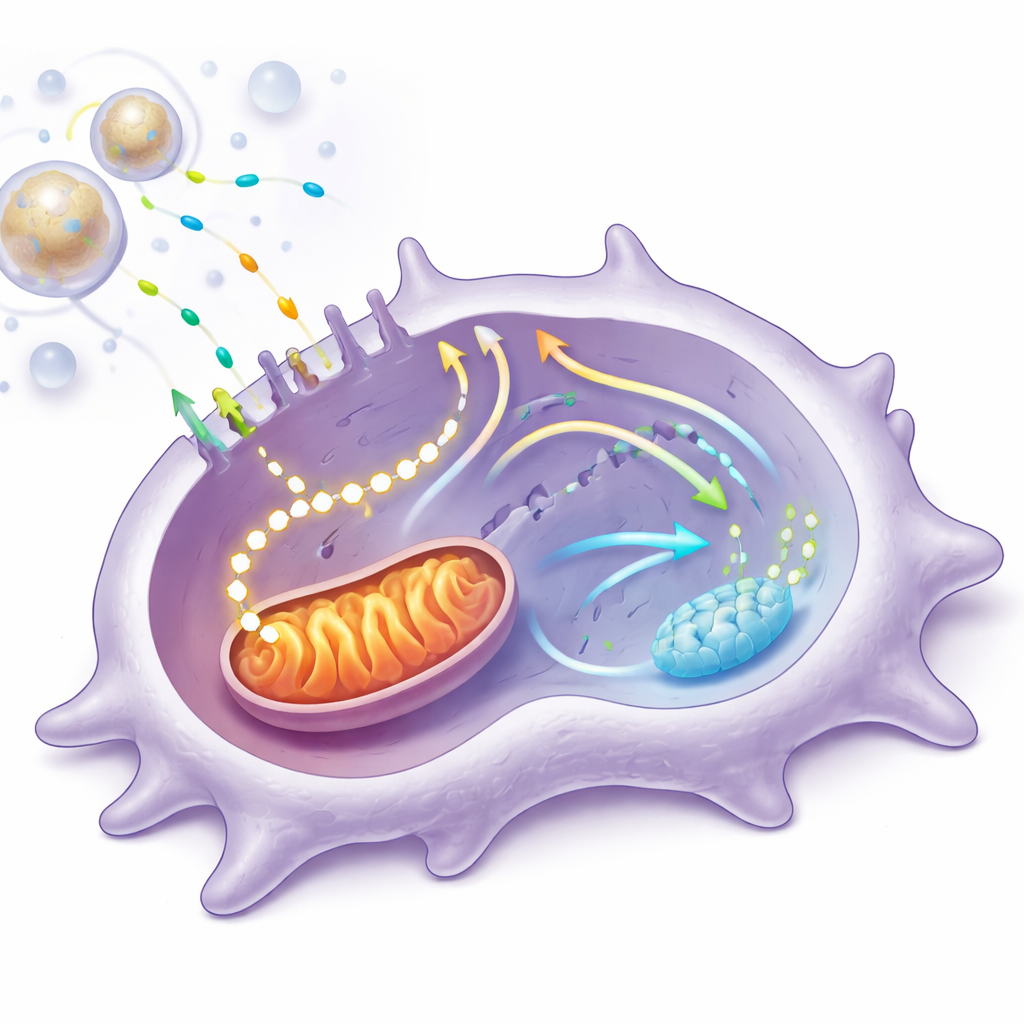
重连细胞能量用途
进一步研究中,团队分离巨噬细胞并在高糖、炎症条件下用释放钒的提取物处理。这些细胞行为向愈合表型转变:与炎症相关的基因和蛋白表达下降,而与组织修复相关的上升。高级代谢测试显示,钒促使细胞摄取更多葡萄糖并将其引导进入线粒体呼吸而不是简单的糖发酵。线粒体的耗氧量和线粒体产生的ATP增加,线粒体内部结构变得更大且更互联——这些都是能量系统更强、更高效的标志。阻断糖来源燃料进入线粒体会大幅抵消这些益处,说明额外的线粒体能量对于巨噬细胞的性格转变至关重要。
连接糖、能量与愈合的信号通路
研究还绘制了巨噬细胞内的信号级联。钒增强了细胞表面胰岛素受体的活性并激活了下游的PI3K–AKT通路,该通路已知调控葡萄糖处理。这进一步增加了膜上葡萄糖转运蛋白(GLUT4)的存在,使更多葡萄糖流入。细胞中心能量循环的酶活性提高,柠檬酸及其衍生物乙酰辅酶A水平上升,不仅为能量生产提供底物,还促进对细胞DNA包装蛋白的微妙化学修饰。与启动愈合相关基因表达上调有关的一种组蛋白修饰增加。当研究者化学抑制胰岛素受体、PI3K或GLUT4时,代谢增强和巨噬细胞向修复模式的转变均显著减弱。综上,这些结果表明钒作为局部的模拟胰岛素信号,恢复了高糖、线粒体高效能量使用与促愈合免疫行为之间被破坏的联系。
这对患者意味着什么
这项工作表明,应对糖尿病创面可能不仅仅是向代谢敌对的环境上添加生长因子或细胞。通过设计一种在高糖部位定点释放钒的葡萄糖响应性凝胶,研究者能够从内部重新编程创面的免疫细胞,平息慢性炎症并在小鼠中促进再生。尽管仍需开展长期安全性研究——尤其是监测潜在的钒蓄积——该方法提供了一种有前景的无细胞策略,可与现有的外用敷料临床实践相衔接。如果成功转化到人类,这类智能材料或能将顽固的糖尿病溃疡变为能够再次记起如何愈合的伤口。
引用: Li, J., Li, Z., Han, L. et al. Macrophage metabolic reprogramming by vanadium released from glucose-responsive bio-gel accelerates diabetic wound repair. Sig Transduct Target Ther 11, 148 (2026). https://doi.org/10.1038/s41392-026-02647-y
关键词: 糖尿病创面愈合, 巨噬细胞极化, 钒生物材料, 葡萄糖响应性水凝胶, 免疫代谢