Clear Sky Science · ja
グルコース応答性バイオゲルから放出されるバナジウムによるマクロファージ代謝の再プログラミングが糖尿病性創傷修復を加速する
なぜ手ごわい糖尿病性創傷が問題なのか
糖尿病の多くの人にとって、足の小さな水ぶくれや切り傷がいつの間にか慢性で治りにくい潰瘍に進行し、感染や切断、さらには命に関わる事態を招くことがあります。これらの創傷は、高血糖が局所の免疫系やエネルギー供給を密かに乱すため、一般的な被覆材や抗生物質に抵抗することが多いです。本研究は、高グルコースに応答して微量金属のバナジウムを放出する新しいタイプの“スマート”創傷ゲルを検討します。目的は、主要な免疫細胞の代謝を穏やかに調整し、炎症を助長する状態から組織再生を促す状態へとスイッチさせることです。
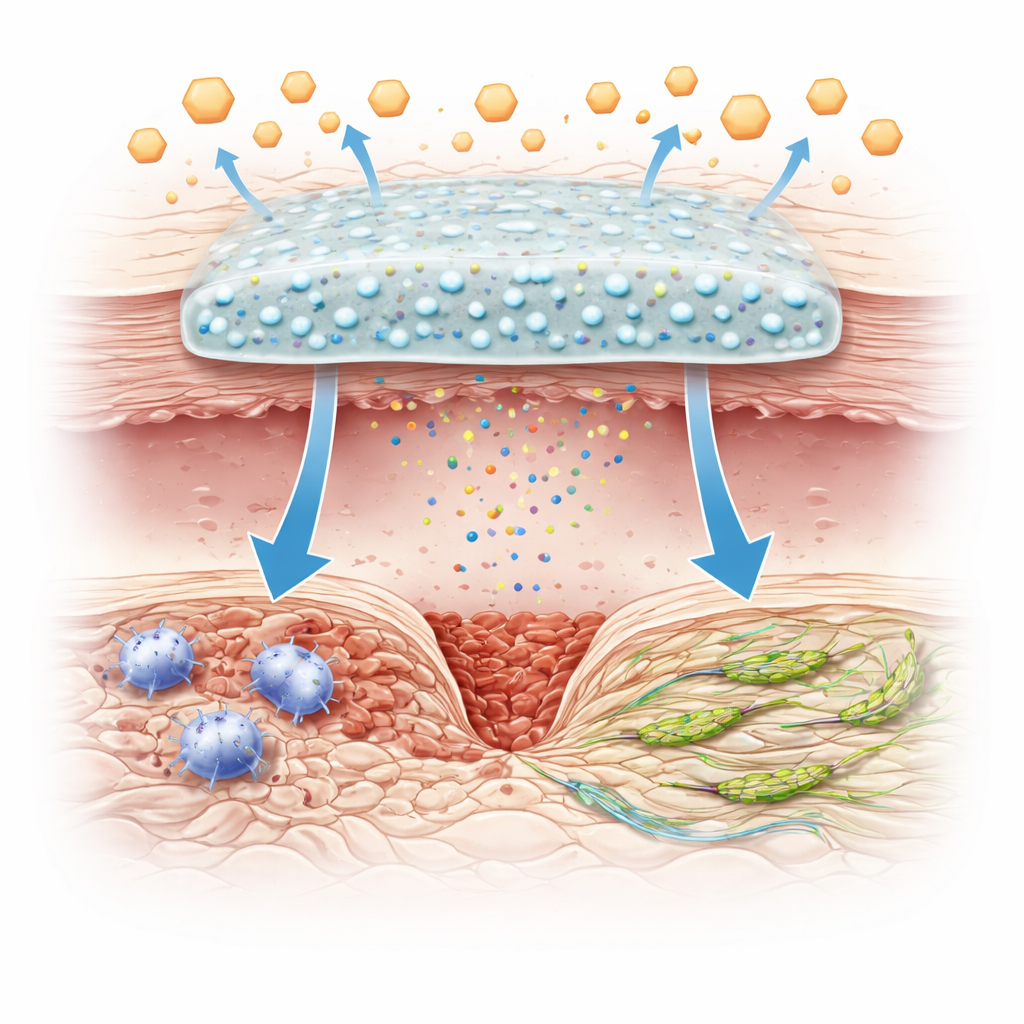
免疫細胞が行き詰まるしくみ
マクロファージは最前線の免疫細胞であると同時に、現場での修復作業を担う存在です。創傷治癒の初期には、病原体と戦い炎症を引き起こす戦闘的な形をとり、後期には炎症を鎮め新しい組織の成長を支える育成的なモードへと移行するはずです。この移行は細胞のエネルギー生成方法と密接に結びついています:炎症促進状態は速やかな糖代謝に依存し、治癒促進状態はミトコンドリアによる酸素依存のより緩やかなエネルギー産生を用います。糖尿病性創傷では持続する高糖と不十分なインスリンシグナルがこのエネルギースイッチを乱し、マクロファージを炎症促進の“怒った”状態に閉じ込め、創傷を慢性の治らない状態に保ちます。
糖に反応するスマートゲル
この問題に対処するため、研究者らはカルシウム、ケイ素、リン、バナジウム酸化物から成るバナジウム含有の小さなガラス様球体を作製しました。これらの球体は改変ゼラチンとグルコースに応答して膨潤するキトサン系成分からなる柔らかいヒドロゲルに埋め込まれました。糖が高い条件(糖尿病性創傷に類似)では、ゲルはより多くの水を吸収して内部ネットワークが緩み、バナジウム含有粒子やイオンが制御された形で放出されます。試験では、これらの球体をゲルに組み込んでも構造を損なわず、機械的性質が強化され、グルコースに誘導された安定的なバナジウム放出が可能になることが示されました。
糖尿病マウスでの修復促進
完全厚さの皮膚創にこのゲルを適用すると、無治療やバナジウムを含まないゲルと比べて治癒が劇的に改善しました。バナジウムを含む創傷被覆は創面の速やかな閉鎖、外層皮膚のより良い再形成、そして秩序だったコラーゲン沈着をもたらし、これらはすべて健康な修復の特徴です。組織の化学プロファイリングでは、糖尿病に関連する酸性代謝産物や代謝廃棄物の蓄積が減少していました。同時に、TNF-αやIL-6のような過剰炎症の指標は低下し、抗炎症性のシグナルや新生血管形成は増加しました。マクロファージマーカーの染色では、初期の時点で治癒促進状態の細胞が増え、炎症促進状態の細胞が減少しており、ゲルが単に創を覆うだけでなく免疫環境を能動的に再形成していることを示していました。
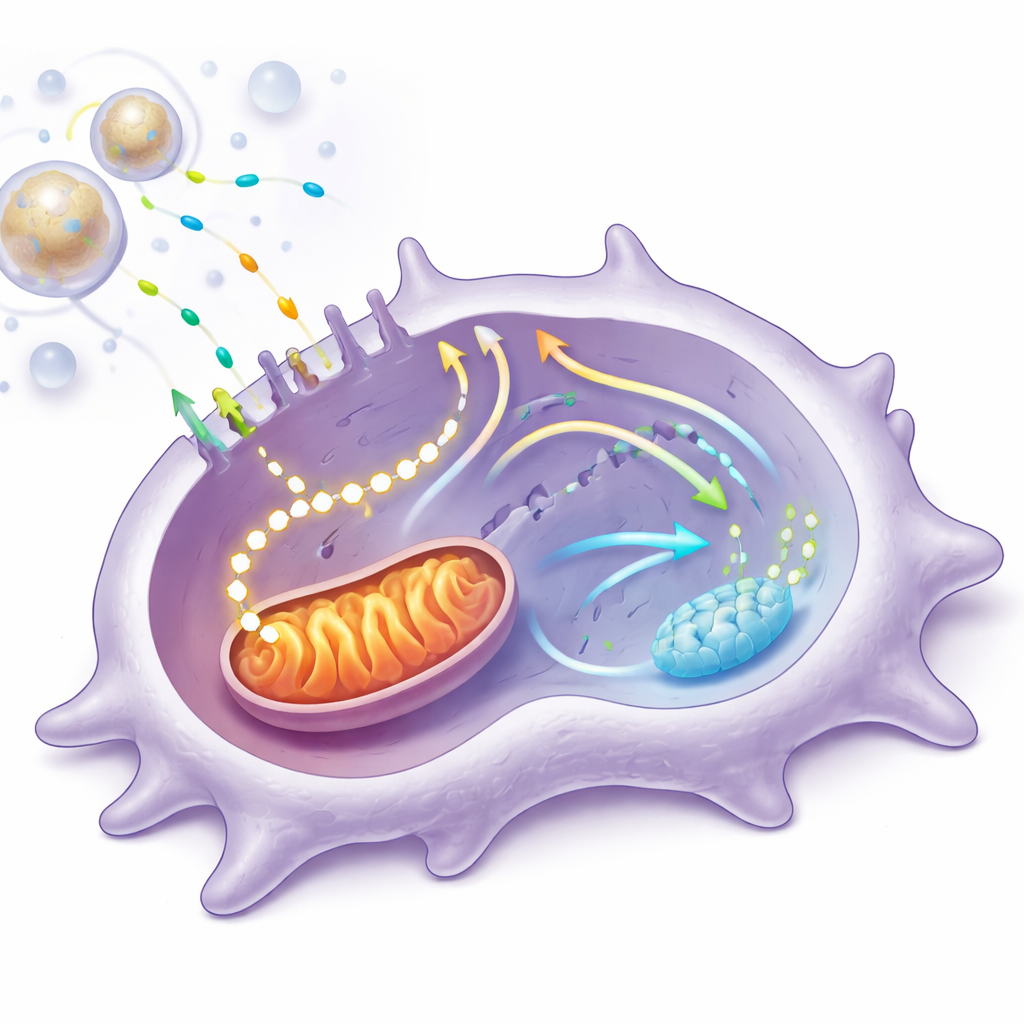
細胞のエネルギー利用を書き換える
さらに解析を進めるため、研究チームはマクロファージを単離し、高グルコースかつ炎症誘導条件下でバナジウム放出抽出液に曝露しました。これらの細胞は治癒表現型へと挙動を変え、炎症に関連する遺伝子やタンパク質は低下し、組織修復に関連するものは増加しました。高度な代謝解析により、バナジウムが細胞により多くのグルコースを取り込み、それを単純な糖発酵ではなくミトコンドリア呼吸に振り向けるよう促すことが示されました。ミトコンドリアの酸素消費量とATP産生は増加し、ミトコンドリアの内部構造は大きくより相互接続的になり、より強く効率的なエネルギーシステムの兆候が現れました。糖由来燃料のミトコンドリアへの流入を遮断するとこれらの利点はほとんど消失し、余分なミトコンドリアエネルギーがマクロファージの性質変化に不可欠であることが示されました。
糖、エネルギー、治癒をつなぐシグナル経路
研究はさらにマクロファージ内部のシグナルカスケードを明らかにしました。バナジウムは細胞表面のインスリン受容体の活性を高め、下流のPI3K–AKT経路をオンにしました。この経路はグルコース処理を調節することで知られており、その結果としてGLUT4というグルコーストランスポーターが細胞膜上に増加し、より多くの糖が細胞内に流入しました。細胞の中心的エネルギー回路の酵素活性が高まり、クエン酸やその誘導体であるアセチル-CoAのレベルが上がり、エネルギー生産に加えて細胞のDNAを包むタンパク質への微妙な化学的変化にも寄与しました。特に治癒関連遺伝子をオンにすることに関連するヒストン修飾が増加しました。インスリン受容体、PI3K、あるいはGLUT4を化学的に阻害すると、代謝的ブーストもマクロファージの修復モードへの移行も大きく減少しました。これらの結果は、バナジウムが局所的なインスリン類似シグナルとして働き、高グルコースと効率的なミトコンドリアエネルギー利用および治癒促進免疫挙動との断たれた結びつきを回復することを示しています。
患者にとっての意義
この研究は、糖尿病性創傷の治療には単に成長因子や細胞を代謝的に敵対的な環境の上に載せるだけでは不十分な場合があることを示唆します。糖が高い場所に精確にバナジウムを届けるグルコース応答性ゲルを設計することで、研究者らは創傷の免疫細胞を内側から書き換え、慢性的な炎症を鎮めマウスでの再生を促しました。長期的な安全性試験、特にバナジウムの蓄積の可能性を監視する必要は残りますが、このアプローチは既存の外用被覆材の臨床使用と整合する有望な細胞を用いない戦略を提示します。ヒトへうまく移行できれば、こうしたスマート材料は手ごわい糖尿病性潰瘍をついに治癒を思い出す創へと変える可能性があります。
引用: Li, J., Li, Z., Han, L. et al. Macrophage metabolic reprogramming by vanadium released from glucose-responsive bio-gel accelerates diabetic wound repair. Sig Transduct Target Ther 11, 148 (2026). https://doi.org/10.1038/s41392-026-02647-y
キーワード: 糖尿病性創傷治癒, マクロファージの極性化, バナジウムバイオマテリアル, グルコース応答性ヒドロゲル, 免疫代謝