Clear Sky Science · fr
Reprogrammation métabolique des macrophages par le vanadium libéré d’un bio-gel glucose‑sensible accélère la réparation des plaies diabétiques
Pourquoi les plaies diabétiques persistantes comptent
Pour de nombreuses personnes diabétiques, une petite ampoule ou une coupure au pied peut silencieusement évoluer en un ulcère chronique difficile à cicatriser, menaçant d’infection, d’amputation, voire de décès. Ces plaies résistent souvent aux pansements et aux antibiotiques car l’hyperglycémie perturbe discrètement le système immunitaire local et l’approvisionnement énergétique. Cette étude explore un nouveau type de gel « intelligent » pour les plaies qui libère un oligo‑élément, le vanadium, en réponse à une forte concentration de glucose. L’objectif est de réajuster en douceur le métabolisme des cellules immunitaires clés afin qu’elles passent d’un état favorisant l’inflammation à un état actif de reconstruction tissulaire.
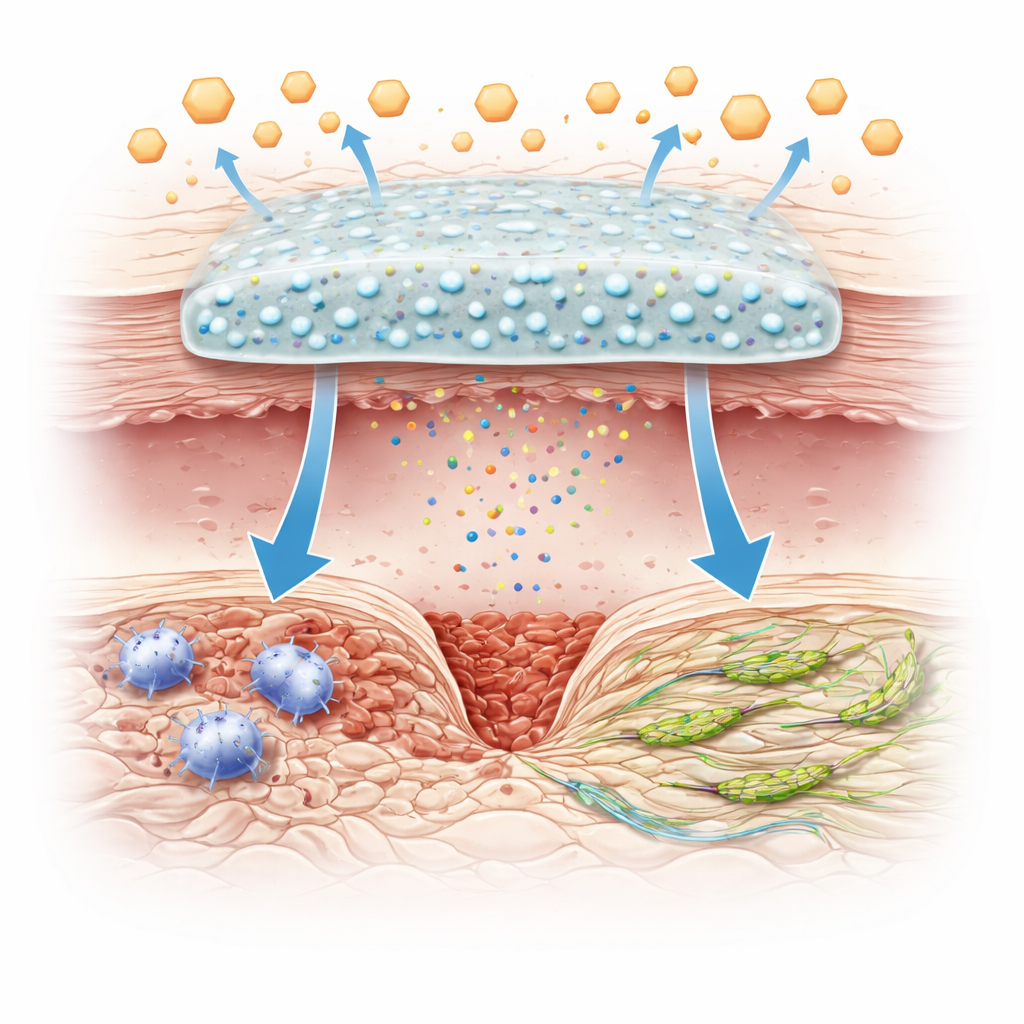
Comment les cellules immunitaires se retrouvent bloquées
Les macrophages sont des cellules immunitaires de première ligne qui jouent aussi le rôle d’équipes de réparation locales. En début de cicatrisation, ils adoptent une posture combattante qui attaque les germes et déclenche l’inflammation ; plus tard, ils devraient basculer vers un mode nourricier qui calme l’inflammation et soutient la formation de nouveau tissu. Ce basculement est étroitement lié à la manière dont les cellules produisent de l’énergie : l’état pro‑inflammatoire repose sur une chimie rapide de combustion du sucre, tandis que l’état pro‑réparation utilise une énergie plus lente, dépendante de l’oxygène, fournie par les mitochondries, centrales énergétiques de la cellule. Dans les plaies diabétiques, la glycémie constamment élevée et la mauvaise signalisation de l’insuline font dérailler cet interrupteur énergétique, piégeant les macrophages dans un mode agressif et inflammatoire et maintenant la plaie dans un état chronique et non cicatrisant.
Un gel intelligent qui répond au sucre
Pour s’attaquer à ce problème, les chercheurs ont créé de minuscules sphères vitrifiées contenant du vanadium, fabriquées à partir d’oxydes de calcium, de silicium, de phosphore et de vanadium. Ces sphères ont ensuite été incorporées dans un hydrogel souple à base de gélatine modifiée et d’un composant à base de chitosane qui gonfle en présence de glucose. Dans des conditions de forte glycémie, comme celles des plaies diabétiques, le gel absorbe plus d’eau, son réseau interne se relâche et les particules et ions contenant du vanadium sont libérés de manière contrôlée. Les tests en laboratoire ont montré que l’incorporation de ces sphères n’endommageait pas la structure du gel, mais renforçait ses propriétés mécaniques et permettait une libération soutenue de vanadium déclenchée par le glucose.
Accélérer la réparation chez des souris diabétiques
Lorsqu’on a appliqué le gel sur des plaies cutanées en pleine épaisseur chez des souris diabétiques, la cicatrisation s’est nettement améliorée par rapport aux plaies non traitées ou aux gels sans vanadium. Le pansement chargé en vanadium a entraîné une fermeture plus rapide de la zone de la plaie, une meilleure reformation des couches cutanées externes et un dépôt de collagène plus ordonné, autant de signes d’une réparation saine. Le profilage chimique des tissus a montré que le traitement réduisait l’accumulation de sous‑produits acides et d’autres déchets métaboliques associés au diabète. Parallèlement, les signaux d’inflammation excessive, tels que TNF‑α et IL‑6, ont diminué, tandis que les signaux anti‑inflammatoires et la néovascularisation ont augmenté. La coloration des marqueurs de macrophages a révélé davantage de cellules en état pro‑réparation et moins en état pro‑inflammatoire aux premiers instants, indiquant que le gel remodelait activement l’environnement immunitaire, et ne se contentait pas de couvrir la plaie.
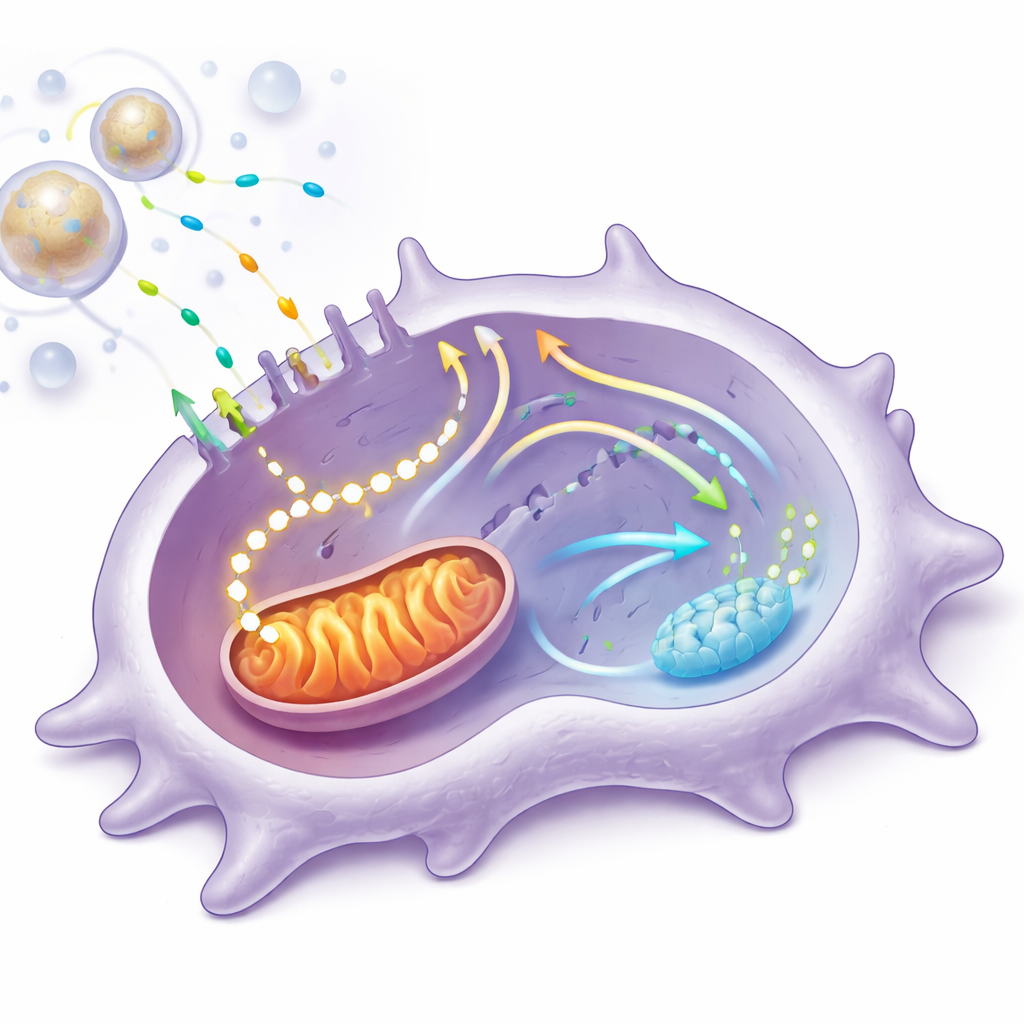
Reconfigurer l’utilisation énergétique cellulaire
En approfondissant, l’équipe a isolé des macrophages et les a exposés à des extraits libérant du vanadium dans des conditions de forte glycémie et d’inflammation. Ces cellules ont orienté leur comportement vers un phénotype de réparation : les gènes et protéines liés à l’inflammation ont été diminués, tandis que ceux associés à la réparation tissulaire ont augmenté. Des tests métaboliques avancés ont montré que le vanadium incitait les cellules à capter davantage de glucose et à l’acheminer vers la respiration mitochondriale plutôt que vers la simple fermentation du sucre. La consommation d’oxygène et la production d’ATP par les mitochondries ont augmenté, et la structure interne des mitochondries est devenue plus large et plus interconnectée — des signes d’un système énergétique plus robuste et plus efficace. Le blocage de l’entrée du carburant dérivé du glucose dans les mitochondries abolissait en grande partie ces bénéfices, montrant que l’apport énergétique mitochondrial supplémentaire était essentiel pour le changement de comportement du macrophage.
Une voie de signalisation qui relie sucre, énergie et réparation
L’étude a également cartographié la cascade de signalisation à l’intérieur des macrophages. Le vanadium a renforcé l’activité du récepteur de l’insuline à la surface cellulaire et activé la voie PI3K–AKT en aval, connue pour réguler la gestion du glucose. Cela a augmenté la présence d’un transporteur de glucose (GLUT4) sur la membrane cellulaire, permettant à plus de sucre d’entrer. Les enzymes du cycle énergétique central de la cellule sont devenues plus actives, et les niveaux de citrate et de son dérivé acétyl‑CoA ont augmenté, alimentant non seulement la production d’énergie mais aussi des modifications chimiques subtiles des protéines empaquetant l’ADN. Une modification d’histone particulière, liée à l’activation de gènes impliqués dans la réparation, a augmenté. Lorsque les chercheurs ont bloqué chimiquement le récepteur de l’insuline, la PI3K ou GLUT4, à la fois le boost métabolique et la transition du macrophage vers un mode réparation ont été fortement réduits. Ensemble, ces résultats montrent que le vanadium agit comme un signal local mimant l’insuline qui restaure le lien rompu entre hyperglycémie, utilisation mitochondriale efficace de l’énergie et comportement immunitaire pro‑réparation.
Ce que cela pourrait signifier pour les patients
Ce travail suggère que s’attaquer aux plaies diabétiques peut exiger plus que l’ajout de facteurs de croissance ou de cellules sur un environnement métaboliquement hostile. En concevant un gel glucose‑sensible qui délivre le vanadium exactement là où le sucre est élevé, les chercheurs ont pu reprogrammer de l’intérieur les cellules immunitaires de la plaie, apaisant l’inflammation chronique et favorisant la régénération chez la souris. Bien que des études de sécurité à long terme soient encore nécessaires — notamment pour surveiller un éventuel dépôt de vanadium — l’approche propose une stratégie prometteuse, sans cellules, compatible avec la pratique clinique actuelle d’application de pansements topiques. Si elle est correctement traduite chez l’humain, ce type de matériau intelligent pourrait transformer des ulcères diabétiques rebelles en plaies qui retrouvent enfin leur capacité à cicatriser.
Citation: Li, J., Li, Z., Han, L. et al. Macrophage metabolic reprogramming by vanadium released from glucose-responsive bio-gel accelerates diabetic wound repair. Sig Transduct Target Ther 11, 148 (2026). https://doi.org/10.1038/s41392-026-02647-y
Mots-clés: guérison des plaies diabétiques, polarisation des macrophages, biomatériaux au vanadium, hydrogel glucose‑sensible, métabolisme immunitaire