Clear Sky Science · zh
伴REM睡眠行为障碍的帕金森病患者具有不同的代谢组学和蛋白质组学特征
为何睡眠与肠道在帕金森病中至关重要
许多人把帕金森病主要视为一种运动障碍,以震颤和僵硬为特征。但在这些症状出现很久之前,睡眠和消化方面的微妙变化可能已经开始。本研究探讨了为何那些在深度睡眠中会“演绎”梦境——称为REM睡眠行为障碍的人——往往病情更严重、进展更快。通过仔细分析血液中的分子和肠道中的微生物,研究者揭示了代谢和肠道菌群的变化如何可能推动这种更具侵袭性的帕金森病亚型。
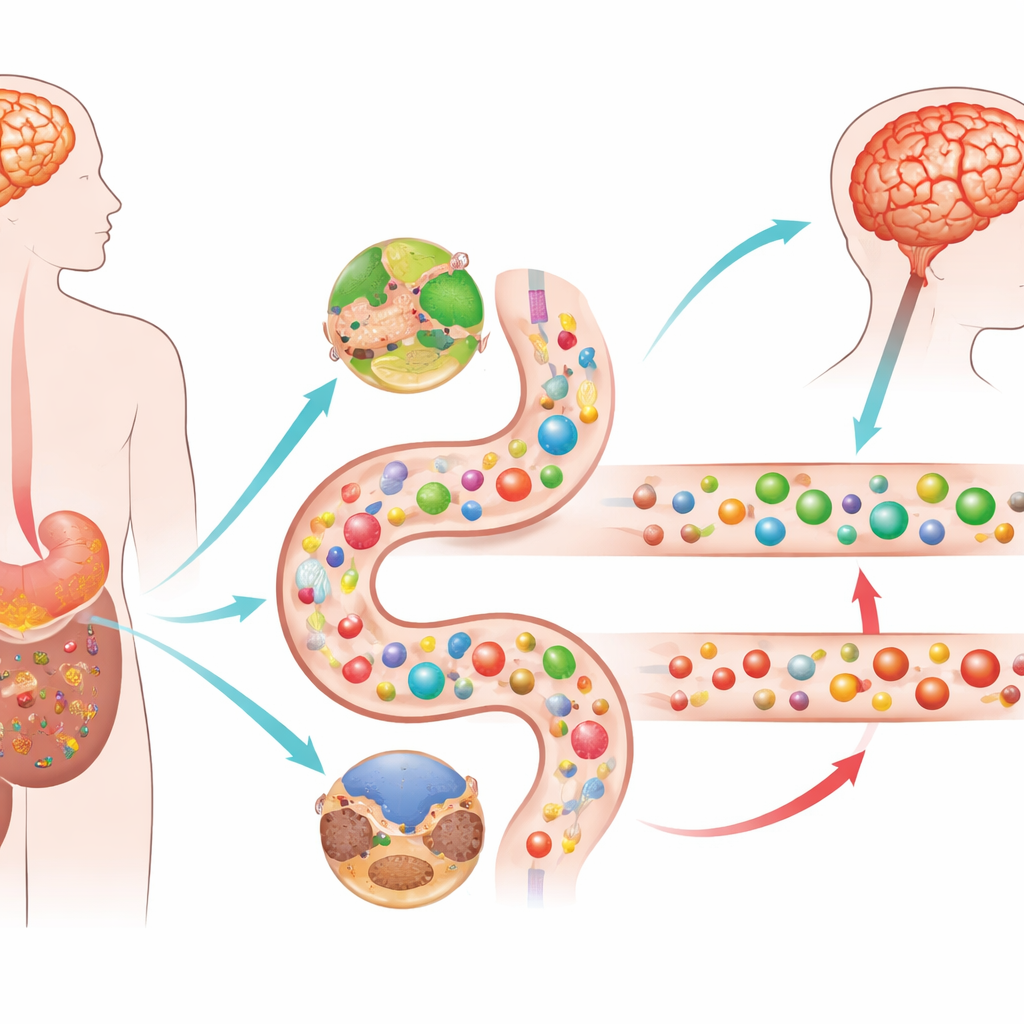
同一疾病的两种面貌
研究者招募了400多名参与者,包括有与无梦境演绎睡眠行为的帕金森患者、仅有孤立REM睡眠行为障碍但尚无运动症状的人,以及健康志愿者。他们在血样中测量了数百种小分子(代谢物和脂类)以及与炎症相关的蛋白质。无论是否有睡眠问题,两组帕金森患者都表现出能量代谢的广泛变化。细胞主要产能循环中的某些化学物质堆积,而多种碳水化合物和“健康”脂肪下降。与此同时,血液中的免疫与炎性信号明显增强,显示出一种全身性的应激反应,而不仅仅是大脑的问题。
能量、废物与脂质失衡
研究团队发现,帕金森病患者的脑细胞与体细胞更依赖于快速但效率较低的糖酵解,而较少依靠线粒体内的常规能量循环。这一转变导致了乳酸和某些有机酸等过量副产物的累积,可能加剧氧化应激与细胞损伤。正常帮助清除氨并维持脑内化学稳定的尿素循环也出现了紊乱,可能增加神经元的负担。同时,构成细胞膜的多种复杂脂类减少,而一类称为溶血磷脂(lysophospholipids)的分解产物增加。这些脂类变化可能削弱细胞膜并干扰细胞清除系统,进而促使类似α-突触核蛋白等有毒蛋白的堆积。
当肠道将蛋白质变成毒物
研究者在比较有无梦境演绎睡眠行为的帕金森患者时,得到了最明显的分化结果。伴有该睡眠障碍的患者血中几种由肠道细菌在发酵膳食蛋白质和某些氨基酸时产生的分子显著升高。这些包括对甲酚(p-cresol)及其相关化合物,以及苯乙酰谷氨酰胺(phenylacetylglutamine),它们与氧化应激、血管损伤和炎症相关。被视为帕金森早期预警状态的孤立REM睡眠行为障碍患者展现了类似模式,表明这种有毒的“化学指纹”在典型运动症状出现之前就已存在。粪便宏基因组分析支持这一结论:这些个体的肠道微生物较少分解膳食纤维,更多地分解蛋白质和肠黏膜,从而促进了这些有害代谢物的产生。
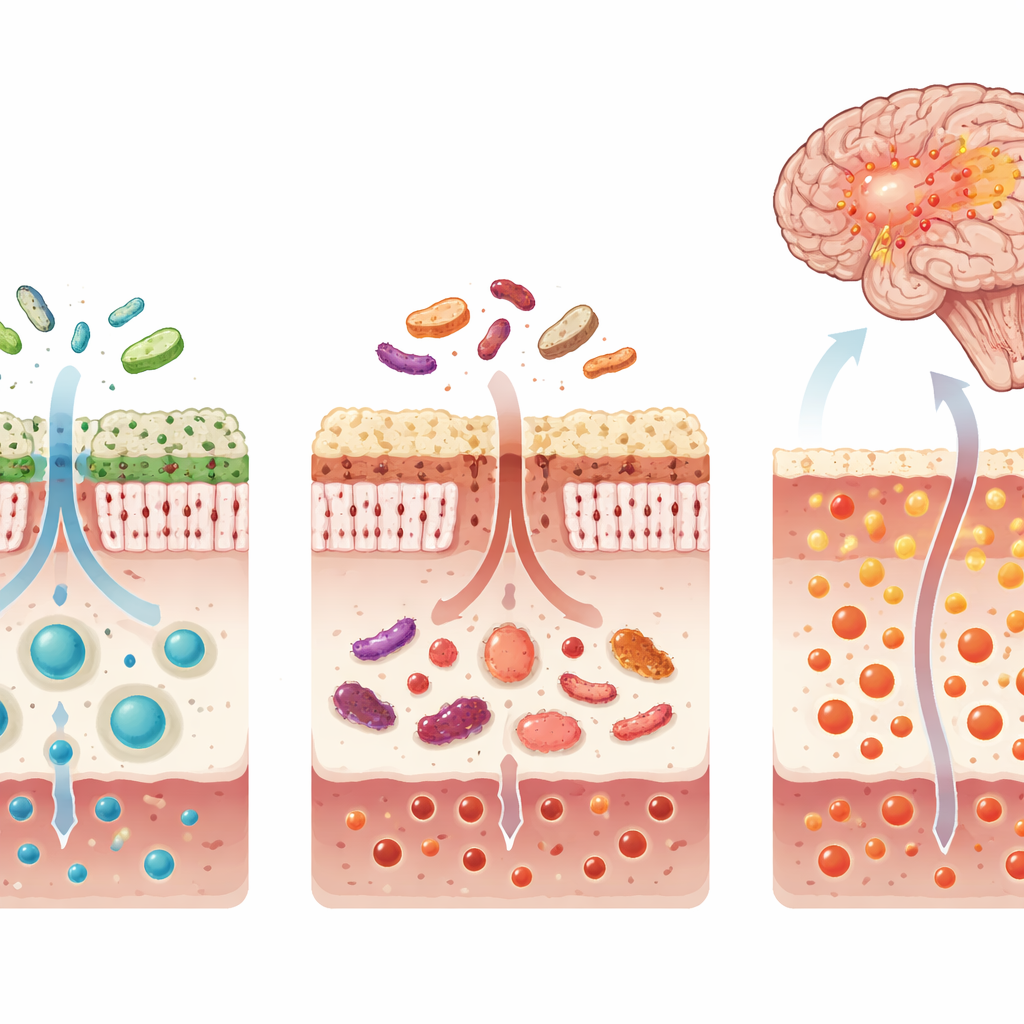
从肠道化学到大脑炎症
许多在这类伴睡眠相关侵袭性亚型中升高的肠源毒素,与血中参与免疫激活、氧化应激和肠道炎症的蛋白质密切相关。同时,合成关键抗氧化剂谷胱甘肽的构件——尤其是氨基酸甘氨酸——减少,而提示抗氧化生成受损的副产物增加。总体上,这表明一种双重打击:肠道更多有毒化合物进入血流,同时机体内的防御系统,尤其是大脑和全身的抗氧化能力被削弱。基于这些血中分子,研究者构建了一套九种代谢物的组合,在两组独立的患者队列中可靠地区分出伴REM睡眠行为障碍的帕金森患者与非该亚型患者。
这对患者与未来意味着什么
对非专业读者而言,信息是:帕金森不仅仅是大脑疾病,而且并非所有帕金森都相同。在REM睡眠中演绎梦境的人似乎走的是一种“身体优先”的途径,肠道微生物及其化学产物可能帮助触发或加速大脑损伤。研究显示,这一路径在血液中留下了可识别的指纹——能量使用、脂质平衡和肠源毒素的改变——这些变化甚至在仅有睡眠障碍但尚未出现运动问题的人群中就能观察到。这些见解指向新的可能性:通过血液检测更早识别高风险个体,以及针对肠道菌群、饮食或特定代谢通路的治疗,以减缓或改变这种更具侵袭性的帕金森病的病程。
引用: Shao, Y., Wang, J., Liu, Y. et al. Distinct metabolomic and proteomic signatures in Parkinson’s disease patients with REM sleep behavior disorder. Sig Transduct Target Ther 11, 115 (2026). https://doi.org/10.1038/s41392-026-02613-8
关键词: 帕金森病, REM睡眠行为障碍, 肠道微生物组, 代谢组学, 神经炎症