Clear Sky Science · fr
Signatures métabolomiques et protéomiques distinctes chez les patients atteints de la maladie de Parkinson avec trouble du comportement en sommeil paradoxal
Pourquoi le sommeil et l’intestin comptent dans la maladie de Parkinson
Beaucoup de personnes considèrent la maladie de Parkinson principalement comme un trouble du mouvement, caractérisé par des tremblements et une raideur. Mais bien avant l’apparition de ces symptômes, des changements subtils du sommeil et de la digestion peuvent déjà être en cours. Cette étude examine pourquoi les personnes atteintes de Parkinson qui rejouent leurs rêves pendant le sommeil profond — un état appelé trouble du comportement en sommeil paradoxal (TCSP) — présentent souvent des symptômes plus sévères et une progression plus rapide de la maladie. En analysant attentivement les molécules dans le sang et les microbes dans l’intestin, les chercheurs mettent en lumière comment des altérations du métabolisme et du microbiote intestinal pourraient contribuer à cette forme plus agressive de Parkinson.
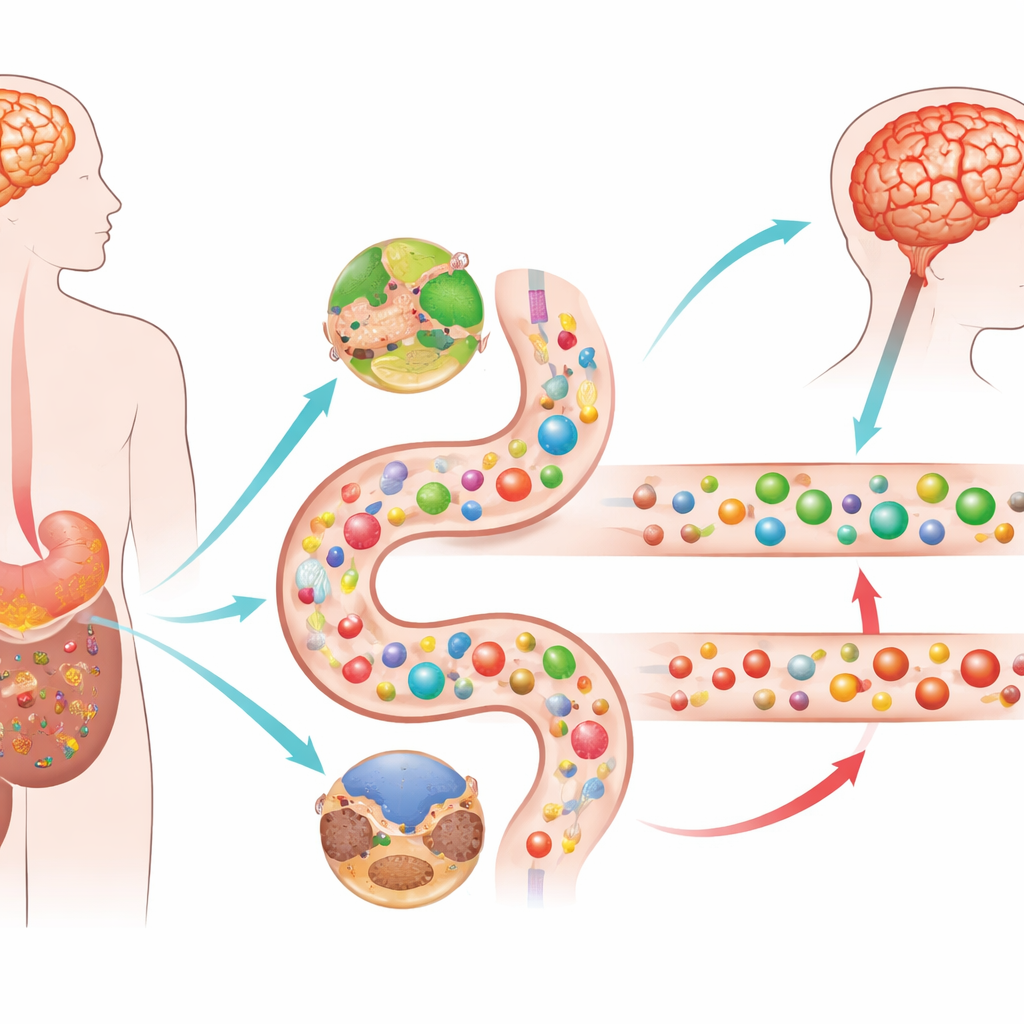
Deux visages d’une même maladie
Les chercheurs ont étudié plus de 400 participants, comprenant des personnes atteintes de Parkinson avec et sans comportement de rejouement des rêves, des personnes présentant un TCSP isolé sans symptômes moteurs encore, et des volontaires sains. Ils ont mesuré des centaines de petites molécules (métabolites et lipides) et des protéines liées à l’inflammation dans des échantillons sanguins. Les deux groupes parkinsoniens, indépendamment des troubles du sommeil, ont montré de larges modifications du traitement de l’énergie par l’organisme. Des composés issus du principal cycle de production d’énergie cellulaire se sont accumulés, tandis que de nombreux glucides et lipides « sains » ont diminué. En parallèle, la signalisation immunitaire et inflammatoire dans le sang était nettement amplifiée, indiquant une réponse de stress à l’échelle du corps et pas seulement un problème localisé au cerveau.
Déséquilibre entre énergie, déchets et lipides
L’équipe a trouvé des signes que les cellules cérébrales et corporelles chez les patients parkinsoniens s’appuient davantage sur une combustion rapide et moins efficace des sucres et moins sur leur cycle énergétique habituel au sein des mitochondries. Ce basculement laisse des sous-produits en excès, tels que l’acide lactique et certains acides organiques, qui peuvent alimenter un cercle vicieux de stress oxydatif et de dommage cellulaire. Le cycle de l’urée, qui aide normalement à éliminer l’ammoniaque et à stabiliser la chimie cérébrale, était aussi perturbé, ce qui peut augmenter la contrainte sur les neurones. Parallèlement, de nombreux lipides complexes formant les membranes cellulaires étaient réduits, tandis qu’un groupe particulier de produits de dégradation appelés lysophospholipides était augmenté. Ces modifications lipidiques peuvent fragiliser les membranes cellulaires et perturber les systèmes de nettoyage cellulaires qui préviennent normalement l’accumulation de protéines toxiques comme l’alpha-synucléine.
Quand l’intestin transforme les protéines en poisons
La distinction la plus nette est apparue lorsque les chercheurs ont comparé les patients parkinsoniens avec et sans TCSP. Ceux présentant le trouble du sommeil avaient des niveaux nettement plus élevés de plusieurs molécules produites par des bactéries intestinales lors de la fermentation de protéines alimentaires et de certains acides aminés. Il s’agit notamment du p-cresol et de composés apparentés, ainsi que de la phenylacetylglutamine, qui ont été associés au stress oxydatif, aux dommages vasculaires et à l’inflammation. Les personnes avec un TCSP isolé — considéré comme un état précoce annonciateur de la maladie de Parkinson — présentaient un schéma similaire, suggérant que cette « empreinte chimique » toxique apparaît avant les symptômes moteurs classiques. L’analyse métagénomique des selles corrobore ce tableau : chez ces individus, les microbes intestinaux semblaient moins orientés vers la dégradation des fibres alimentaires et davantage vers la digestion des protéines et du mucus intestinal, favorisant la production de ces métabolites nocifs.
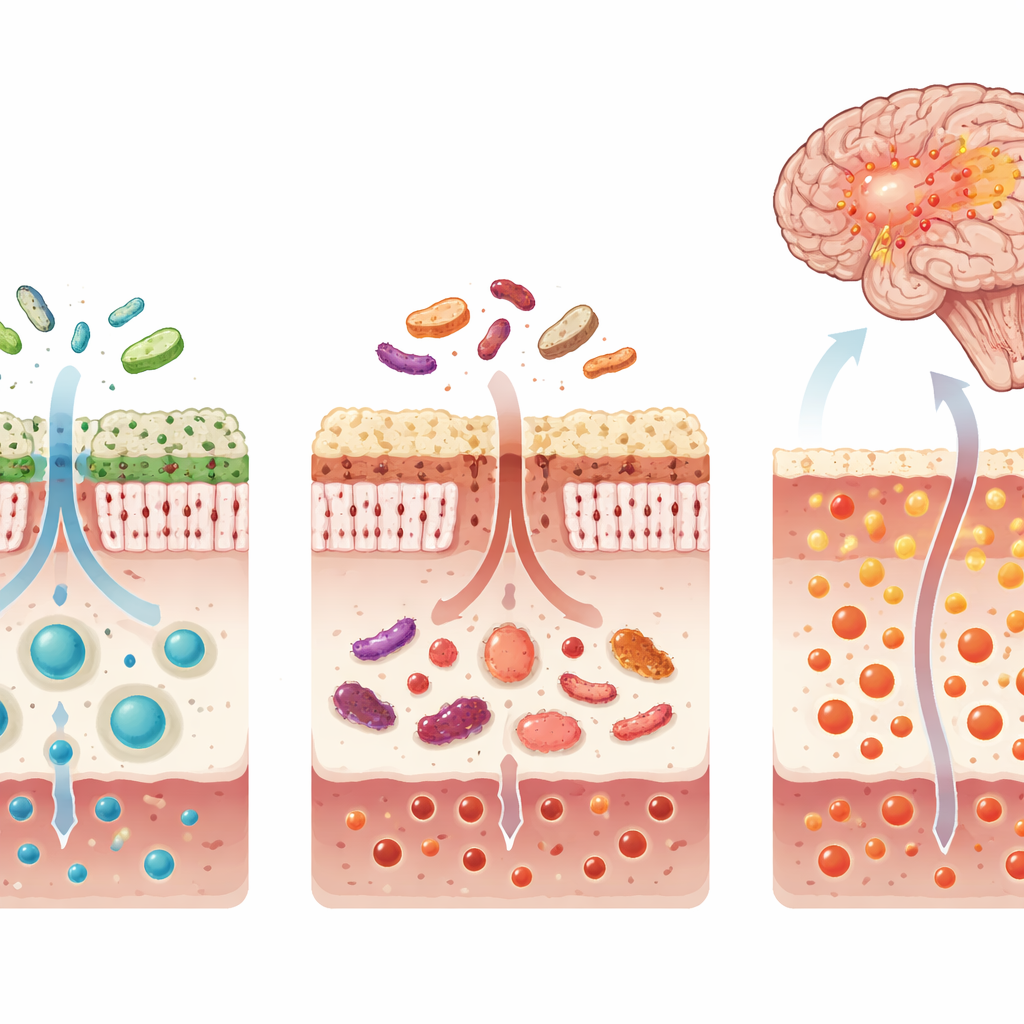
De la chimie intestinale à l’inflammation cérébrale
Nombre des toxines d’origine intestinale retrouvées à des niveaux plus élevés dans le sous‑type parkinsonien lié au sommeil étaient étroitement liées à des protéines sanguines impliquées dans l’activation immunitaire, le stress oxydatif et l’inflammation intestinale. Parallèlement, les éléments constitutifs de l’antioxydant clé glutathion — en particulier l’acide aminé glycine — étaient diminués, tandis que des sous‑produits indiquant une production antioxydante altérée étaient augmentés. Ensemble, cela suggère un double effet : davantage de composés toxiques entrant dans la circulation depuis l’intestin et un système de défense interne affaibli dans le cerveau et le reste du corps. À partir de ces molécules sanguines, les chercheurs ont construit un panel de neuf métabolites capable de distinguer de manière fiable les patients parkinsoniens avec TCSP de ceux sans, dans deux cohortes indépendantes.
Ce que cela signifie pour les patients et l’avenir
Pour un non‑spécialiste, le message est que la maladie de Parkinson n’est pas seulement une maladie du cerveau, et que tous les Parkinson ne se ressemblent pas. Les personnes qui rejouent leurs rêves en sommeil paradoxal semblent suivre une trajectoire « du corps vers le cerveau », où les microbes intestinaux et leurs produits chimiques peuvent contribuer à déclencher ou accélérer les lésions cérébrales. L’étude montre que cette voie laisse une empreinte reconnaissable dans le sang — des changements dans l’utilisation énergétique, l’équilibre lipidique et des toxines d’origine intestinale — qui est déjà visible chez les personnes ayant le trouble du sommeil mais pas encore les troubles moteurs. Ces connaissances ouvrent de nouvelles perspectives : des tests sanguins pour repérer plus tôt les individus à haut risque, et des thérapies ciblant les bactéries intestinales, l’alimentation ou des voies métaboliques spécifiques pour ralentir ou modifier le cours de cette forme particulièrement agressive de la maladie de Parkinson.
Citation: Shao, Y., Wang, J., Liu, Y. et al. Distinct metabolomic and proteomic signatures in Parkinson’s disease patients with REM sleep behavior disorder. Sig Transduct Target Ther 11, 115 (2026). https://doi.org/10.1038/s41392-026-02613-8
Mots-clés: Maladie de Parkinson, Trouble du comportement en sommeil paradoxal, Microbiote intestinal, Métabolomique, Neuroinflammation