Clear Sky Science · ru
Отличительные метаболомные и протеомные сигнатуры у пациентов с болезнью Паркинсона и расстройством поведения во сне во время БДГ
Почему сон и кишечник важны при болезни Паркинсона
Многие считают, что болезнь Паркинсона в первую очередь — нарушение движения, проявляющееся тремором и скованностью. Но задолго до появления этих симптомов могут накапливаться тонкие изменения сна и пищеварения. В этом исследовании изучают, почему у людей с болезнью Паркинсона, которые «воспроизводят» свои сны во время глубокого сна — состояние, называемое расстройством поведения во сне во время быстрого сна (БДГ) — часто наблюдаются более выраженные симптомы и более быстрое прогрессирование болезни. Внимательно исследуя молекулы в крови и микробов в кишечнике, авторы показывают, как изменения в метаболизме и составе микробиоты могут способствовать этой более агрессивной форме Паркинсона.
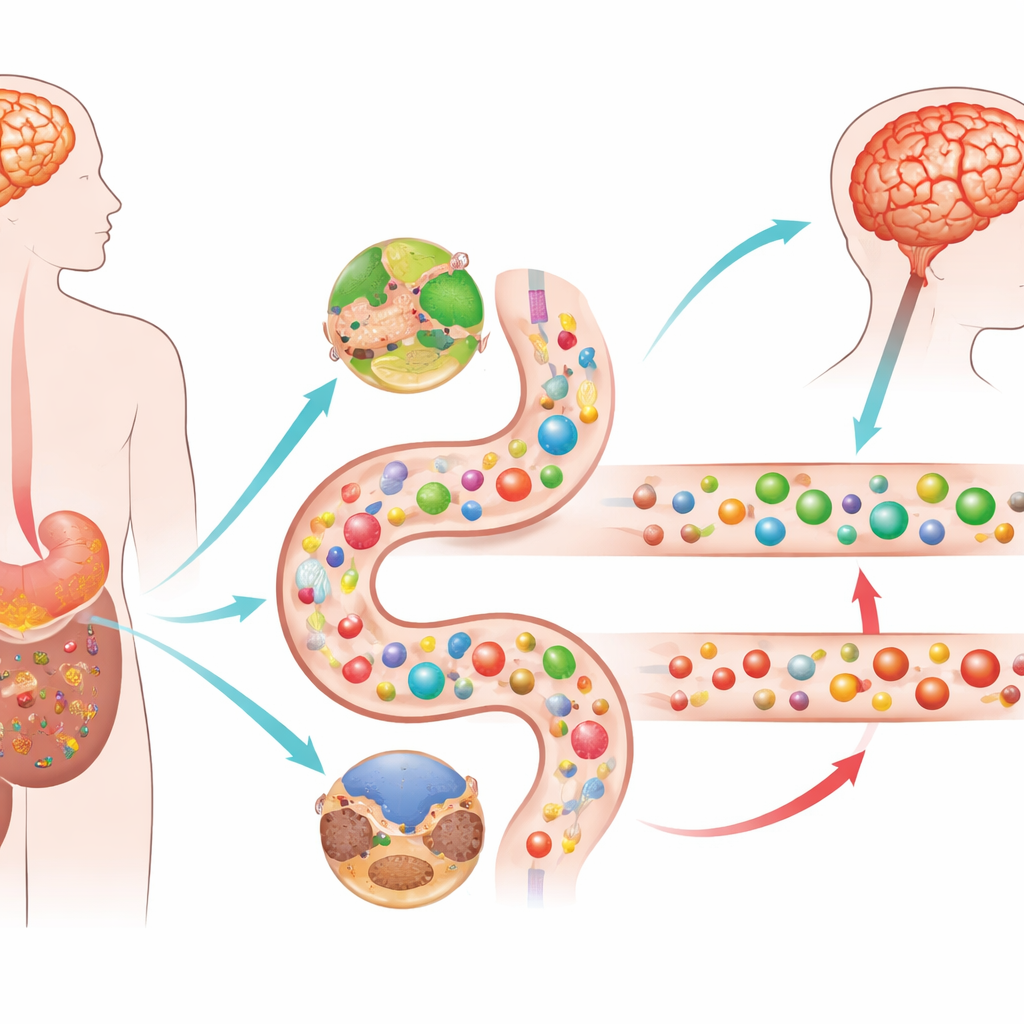
Две грани одного заболевания
Исследователи обследовали более 400 участников, включая пациентов с болезнью Паркинсона с расстройством поведения во сне и без него, людей с изолированным расстройством поведения во сне во время БДГ, у которых еще нет двигательных симптомов, а также здоровых добровольцев. Они измеряли сотни малых молекул (метаболитов и липидов) и белков, связанных с воспалением, в образцах крови. Обе группы пациентов с Паркинсоном, независимо от проблем со сном, показали широкие сдвиги в том, как их организм перерабатывает энергию. Накопились метаболиты главного энергетического цикла клетки, тогда как многие углеводы и полезные жиры снизились. Одновременно в крови отчетливо усилилось иммунное и провоспалительное сигналирование, что указывает на системный стрессовый ответ, а не только на локальную проблему в мозге.
Нарушения в энергии, отходах и липидах
Команда обнаружила признаки того, что клетки мозга и тела при Паркинсоне все чаще полагаются на быстрый, но менее эффективный путь сжигания сахара и меньше — на обычный митохондриальный энергетический цикл. Этот сдвиг приводит к избытку побочных продуктов, таких как молочная кислота и некоторые органические кислоты, которые могут подпитывать порочный круг окислительного стресса и повреждения клеток. Также был нарушен цикл мочевины, который обычно помогает выводить аммиак и поддерживать стабильность химии мозга, что может дополнительно нагружать нервные клетки. Одновременно уменьшилось множество сложных липидов, формирующих мембраны клеток, тогда как уровень определенной группы продуктов распада — лифофосфолипидов — повысился. Эти изменения липидного состава могут ослаблять клеточные мембраны и мешать системам очистки клетки, которые обычно предотвращают накопление токсичных белков, таких как альфа-синуклеин.
Когда кишечник превращает белки в токсины
Самая явная разница появилась при сравнению пациентов с Паркинсоном с расстройством поведения во сне и без него. У тех, кто страдает этим расстройством, отмечались резко повышенные уровни нескольких молекул, которые вырабатывают кишечные бактерии при ферментации пищевых белков и некоторых аминокислот. К ним относятся p-крезол и родственные соединения, а также фенилуксусилглутамин, которые связывают с окислительным стрессом, повреждением сосудов и воспалением. Люди с изолированным расстройством поведения во сне во время БДГ — рассматриваемым как ранний предвестник Паркинсона — продемонстрировали аналогичный профиль, что указывает на то, что этот токсичный «химический знак» появляется до классических моторных симптомов. Метагеномный анализ стула подтвердил эту картину: у таких людей микробы кишечника были менее настроены на расщепление пищевых волокон и больше — на переваривание белка и слизи кишечной оболочки, что способствует образованию этих вредных метаболитов.
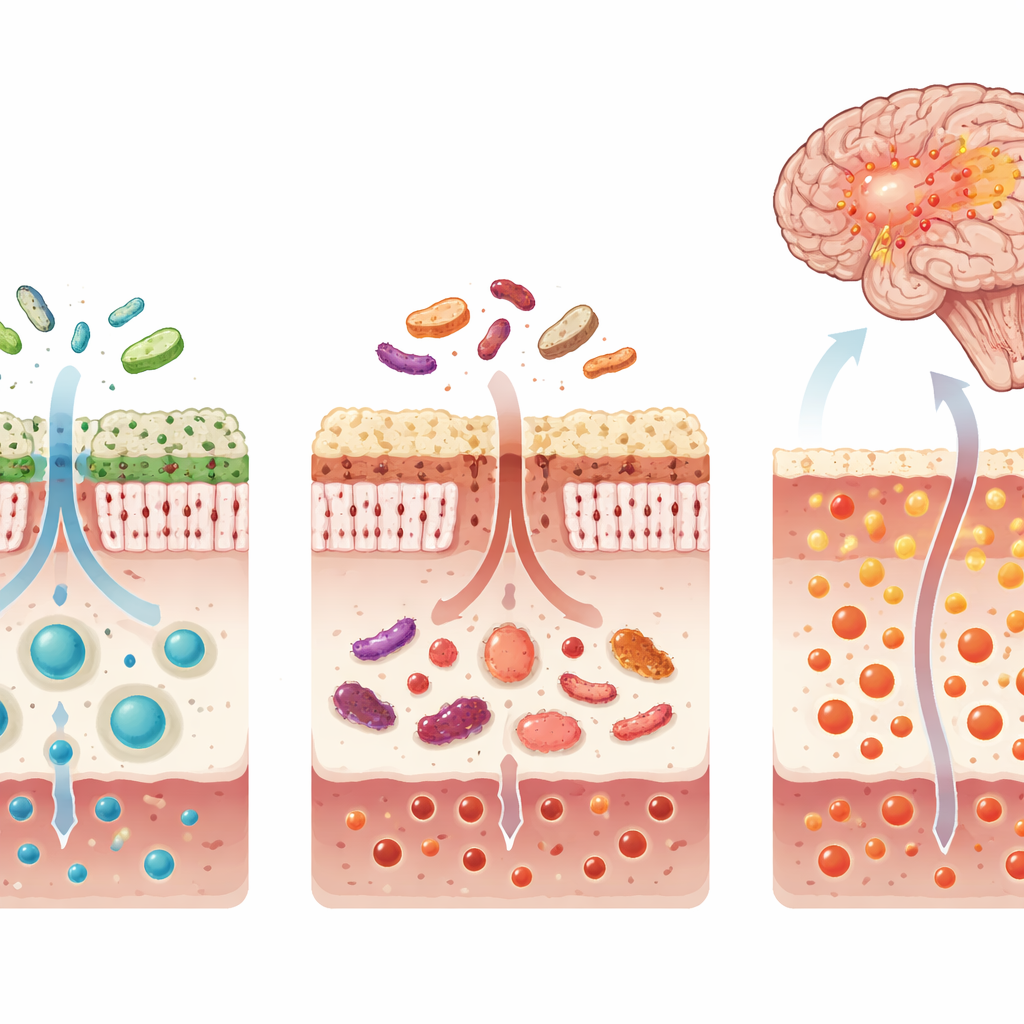
От химии кишечника к воспалению мозга
Многие токсичные соединения кишечного происхождения, обнаруженные в повышенных концентрациях у агрессивного подтипа Паркинсона, связанного со сном, были тесно ассоциированы с белками крови, участвующими в активации иммунитета, окислительном стрессе и воспалении кишечника. Одновременно снизились строительные блоки для ключевого антиоксиданта глутатиона — особенно аминокислота глицин — а также повысились побочные продукты, указывающие на нарушенное производство антиоксидантов. Вместе это указывает на двойной удар: больше токсичных соединений, попадающих в кровь из кишечника, и ослабленная внутренняя система защиты в мозге и теле. На основе этих молекул крови исследователи составили панель из девяти метаболитов, которая надежно отличала пациентов с болезнью Паркинсона и расстройством поведения во сне от тех, у кого этого расстройства не было, в двух независимых группах пациентов.
Что это значит для пациентов и будущего
Для неспециалиста основной вывод таков: болезнь Паркинсона — это не только заболевание мозга, и не все случаи Паркинсона одинаковы. Люди, которые «воспроизводят» свои сны во время БДГ, похоже, следуют «путю тела-начала», при котором микробы кишечника и их химические продукты могут способствовать запуску или ускорению повреждения мозга. Исследование показывает, что этот путь оставляет узнаваемый отпечаток в крови — сдвиги в использовании энергии, балансе липидов и уровнях кишечных токсинов — которые уже видны у людей с расстройством сна, но без двигательных проблем. Эти открытия открывают новые возможности: анализы крови для ранней идентификации людей с высоким риском и терапевтические подходы, нацеленные на микробиоту кишечника, диету или конкретные метаболические пути, чтобы замедлить или изменить течение этой особенно агрессивной формы Паркинсона.
Цитирование: Shao, Y., Wang, J., Liu, Y. et al. Distinct metabolomic and proteomic signatures in Parkinson’s disease patients with REM sleep behavior disorder. Sig Transduct Target Ther 11, 115 (2026). https://doi.org/10.1038/s41392-026-02613-8
Ключевые слова: болезнь Паркинсона, расстройство поведения во сне во время БДГ, микробиом кишечника, метаболомика, нейровоспаление