Clear Sky Science · zh
使用惯性液滴微流控实现类器官和球体的高保真生物组装,用于精准肿瘤学和肿瘤微环境建模
为什么微小的三维组织对癌症护理重要
医生和研究人员越来越依赖在实验室中培养的肿瘤和器官的小型版本来预测真实患者对治疗的反应。这些称为球体(spheroids)和类器官(organoids)的三维细胞团,比起平板上的单层细胞,更能模仿体内组织的结构与行为。然而,现有的培养方法往往速度慢、浪费多且一致性差,难以在药物筛选或个性化癌症治疗中大规模应用。本文介绍了一种名为 OsciSphere 的新平台,旨在快速且可靠地批量生产高度一致的三维迷你组织,并使用可融入标准实验室流程的设备。 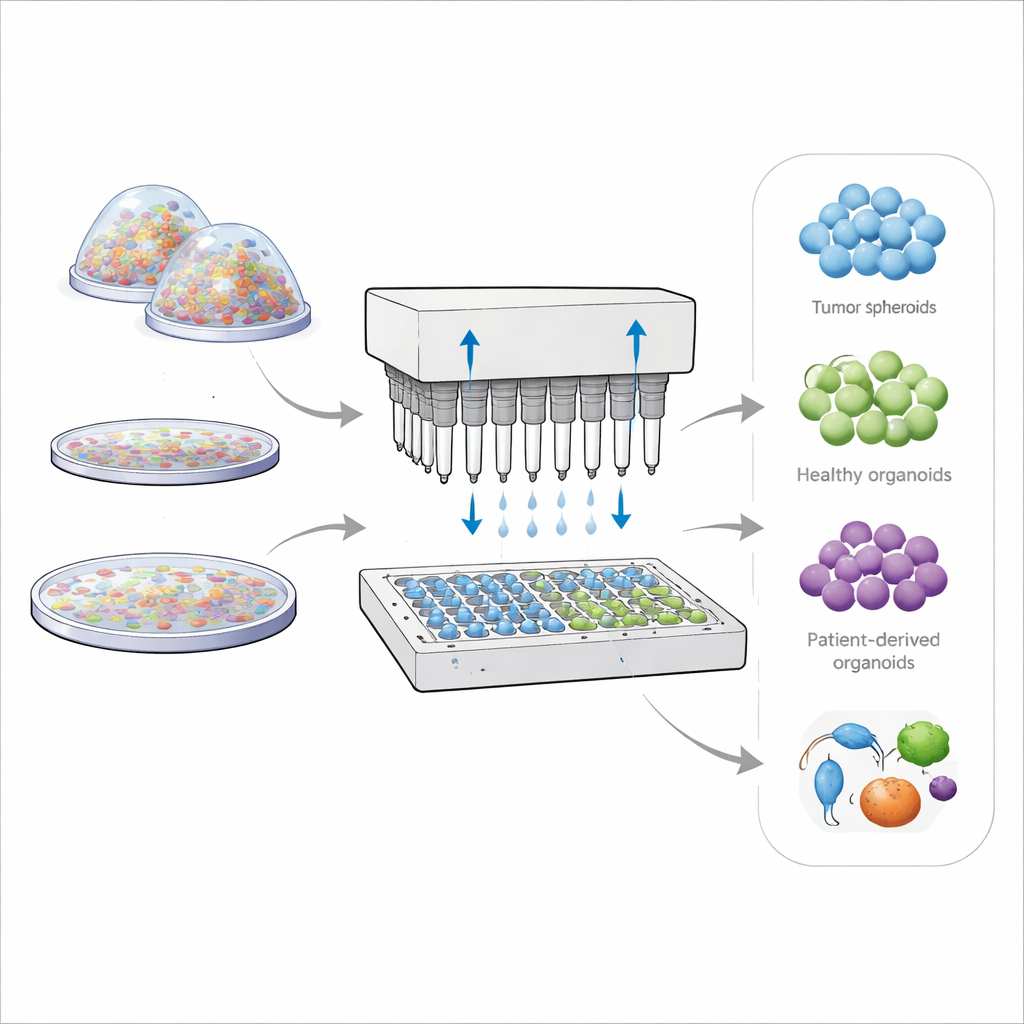
当前三维细胞培养的问题
目前大多数三维培养方法可分为两类:“无支架”系统允许细胞自然聚集,以及将细胞嵌入凝胶中的“有支架”系统。像悬滴法或低粘附培养板等较简便的方法,往往导致每个孔的团块大小差异巨大,使得药物反应数据噪声大、难以比较。由 Matrigel 等材料制成的凝胶穹顶能支持更像真实组织的结构,但体积庞大且难以操作。在这些大穹顶内部,氧气和营养物质无法均匀到达所有细胞,导致坏死核心和不均匀的生长,从而扭曲组织对药物的反应。
一种无芯片的制备均一迷你组织的方法
OsciSphere 通过在常见的实验板内将浓稠、载细胞的凝胶直接转变为许多相同的小液滴来解决这些问题,无需复杂的微流控芯片。该系统使用一组往复振荡的移液器头,以可控的速度和振幅前后移动。这一运动利用惯性而非脆弱的表面力,将等体积的凝胶液滴切割到置于培养基上方的油层中。温度控制在此步骤中保持凝胶处于液态,随后加温使液滴固化成小球,并被温和转移到下方的培养基中。每个固化的凝胶小球成为细胞组装成均一肿瘤球体或类器官的微小“居所”,仅使用常规所需凝胶的一小部分。 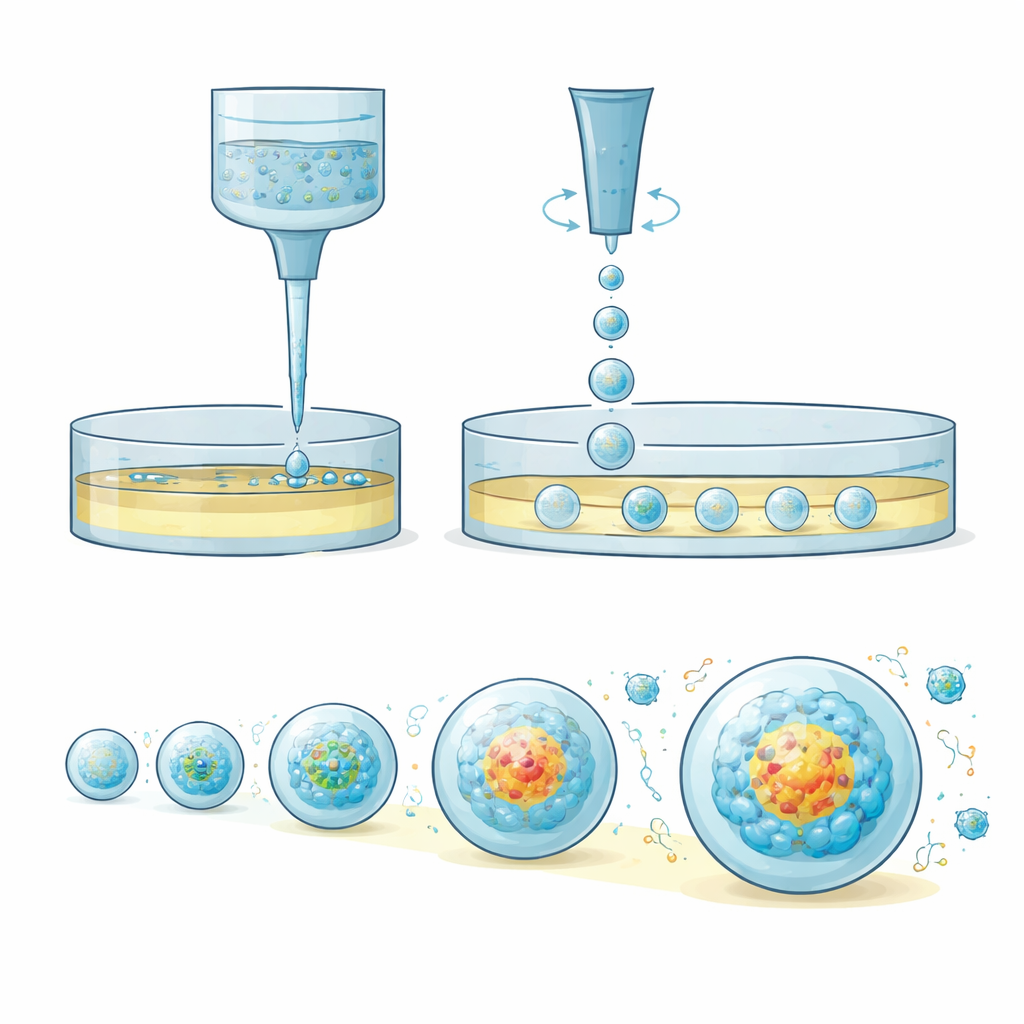
构建更逼真的肿瘤和器官模型
由于每个液滴几乎相同且含有精确控制的细胞数,OsciSphere 能生成在直径和形状上高度一致的三维肿瘤球体。作者展示了这些迷你肿瘤模型重现了真实癌症的关键特征:更慢、更贴近生理的生长速率、内部化学梯度、应激信号以及与侵袭性和类干性行为相关的基因程序。在用小凝胶球培养迷你化的肠道类器官时,这些小球避免了大穹顶的扩散瓶颈。类器官生长更快,显示出更接近肠道内膜的高级结构,并在整个体积内保持均一存活,而不是形成扭曲实验结果的坏死中心。
从药物测试到微生物组和免疫研究
一旦建立起可靠的迷你组织阵列,该平台即可成为强大的测试引擎。用 OsciSphere 制备的肿瘤球体显示出与临床更为匹配的药物耐受模式,而处于小凝胶中的类器官相比埋在厚穹顶中的样本更真实地暴露于化疗药物。这使团队能够快速筛查多种常规结直肠癌药物组合,并识别出在相对低浓度下协同有效的剂量组合。他们进一步将肿瘤球体暴露于数十种肠道细菌分泌的分子,很快找出能强烈抑制肿瘤生长并触发癌细胞死亡通路的菌种代谢产物。最后,他们使用患者来源的肿瘤类器官和该患者自身的免疫细胞来模拟免疫疗法的作用,表明小而可达的微球使免疫细胞能够渗透并激活,这在笨重的穹顶中常难以实现。
这将如何改变精准肿瘤学
简而言之,OsciSphere 提供了一种实用路径,可以使用许多实验室已有的工具来培养数千个近乎相同、行为更像体内组织的迷你肿瘤和迷你器官。通过将凝胶环境缩小为微小且均一的球体,并严格控制每个球体中的细胞数量,该平台提高了用于癌症研究的三维模型的真实度、一致性和速度。这反过来使药物测试、微生物组研究和免疫治疗评估更可信且更易扩展。如果被广泛采用,此类技术可能推动真正的个性化治疗向前发展——在临床给药之前,在患者自身的迷你肿瘤上筛选治疗方案,离日常癌症护理更近一步。
引用: Li, Y., Cao, Z., Xu, Y. et al. High-fidelity bioassembly of organoids and spheroids using inertial droplet microfluidics for precision oncology and tumor microenvironment modeling. Microsyst Nanoeng 12, 152 (2026). https://doi.org/10.1038/s41378-026-01244-x
关键词: 类器官, 肿瘤球体, 微流控, 精准肿瘤学, 肿瘤微环境