Clear Sky Science · pl
Wysokiej wierności bioasemblacja organoidów i sferoidów za pomocą bezwładnościowej mikrofluidyki kroplowej do onkologii precyzyjnej i modelowania mikrośrodowiska guza
Dlaczego małe tkanki 3D mają znaczenie dla opieki nad chorymi na raka
Lekarze i naukowcy coraz częściej polegają na miniaturowych wersjach guzów i organów hodowanych w laboratorium, aby przewidzieć, jak prawdziwi pacjenci zareagują na leczenie. Te trójwymiarowe skupiska komórek, zwane sferoidami i organoidami, odwzorowują strukturę i zachowanie tkanek w organizmie znacznie lepiej niż płaskie warstwy komórkowe na szalkach. Jednak obecne metody ich hodowli są często wolne, marnotrawne i niekonsekwentne, co utrudnia skalowanie do testów leków czy spersonalizowanej terapii onkologicznej. W pracy przedstawiono nową platformę nazwaną OsciSphere, której celem jest masowa produkcja wysoce jednorodnych mini‑tkanek 3D szybko i niezawodnie, przy użyciu sprzętu mieszczącego się w standardowych procedurach laboratoryjnych. 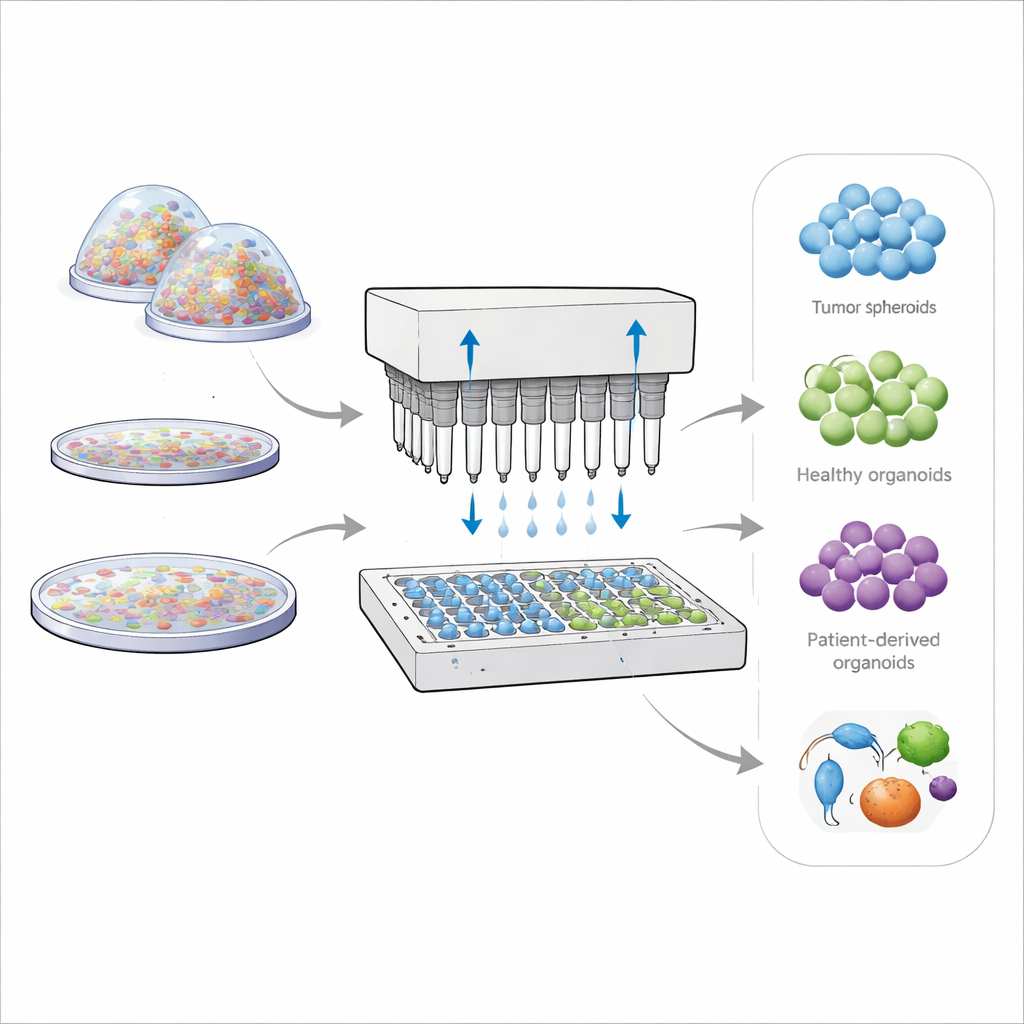
Problem współczesnych kultur komórek 3D
Większość obecnych podejść do kultur 3D dzieli się na dwa obozy: systemy „bez rusztowania”, które pozwalają komórkom naturalnie się zlepiać, oraz systemy „z rusztowaniem”, które zatapiają je w żelu. Prostsze metody, takie jak zwieszane krople czy płytki o niskiej adhezji, zwykle dają skupiska o bardzo różnej wielkości z dołka na dołek, co sprawia, że dane o odpowiedzi na leki są hałaśliwe i trudne do porównania. Kopuły żelowe wykonane z materiałów takich jak Matrigel wspierają bardziej przypominające tkanki struktury, ale są nieporęczne i trudne w obsłudze. Wewnątrz dużych kopuł tlen i składniki odżywcze nie docierają równomiernie do wszystkich komórek, prowadząc do martwych jąder i nierównomiernego wzrostu, co zniekształca odpowiedź tkanek na leki.
Sposób bez chipów na tworzenie jednorodnych mini‑tkanek
OsciSphere rozwiązuje te problemy, zamieniając gęsty żel z komórkami w wiele identycznych, drobnych kropli bezpośrednio w zwykłych płytach laboratoryjnych, bez użycia skomplikowanych chipów mikrofluidycznych. System wykorzystuje matrycę oscylujących końcówek pipet, które poruszają się tam i z powrotem z kontrolowaną prędkością i amplitudą. Ten ruch wykorzystuje bezwładność zamiast delikatnych sił powierzchniowych do odcinania kropli żelu o równej wielkości do warstwy oleju spoczywającej nad medium hodowlanym. Kontrola temperatury utrzymuje żel w stanie ciekłym podczas tego kroku, a następnie podgrzewanie utwardza krople w małe kuleczki, które są delikatnie przenoszone do medium poniżej. Każda stała kula żelowa staje się mini „domem”, w którym komórki mogą się zebrać w jednorodne sferoidy nowotworowe lub organoidy, zużywając tylko ułamek żelu potrzebnego zwykle. 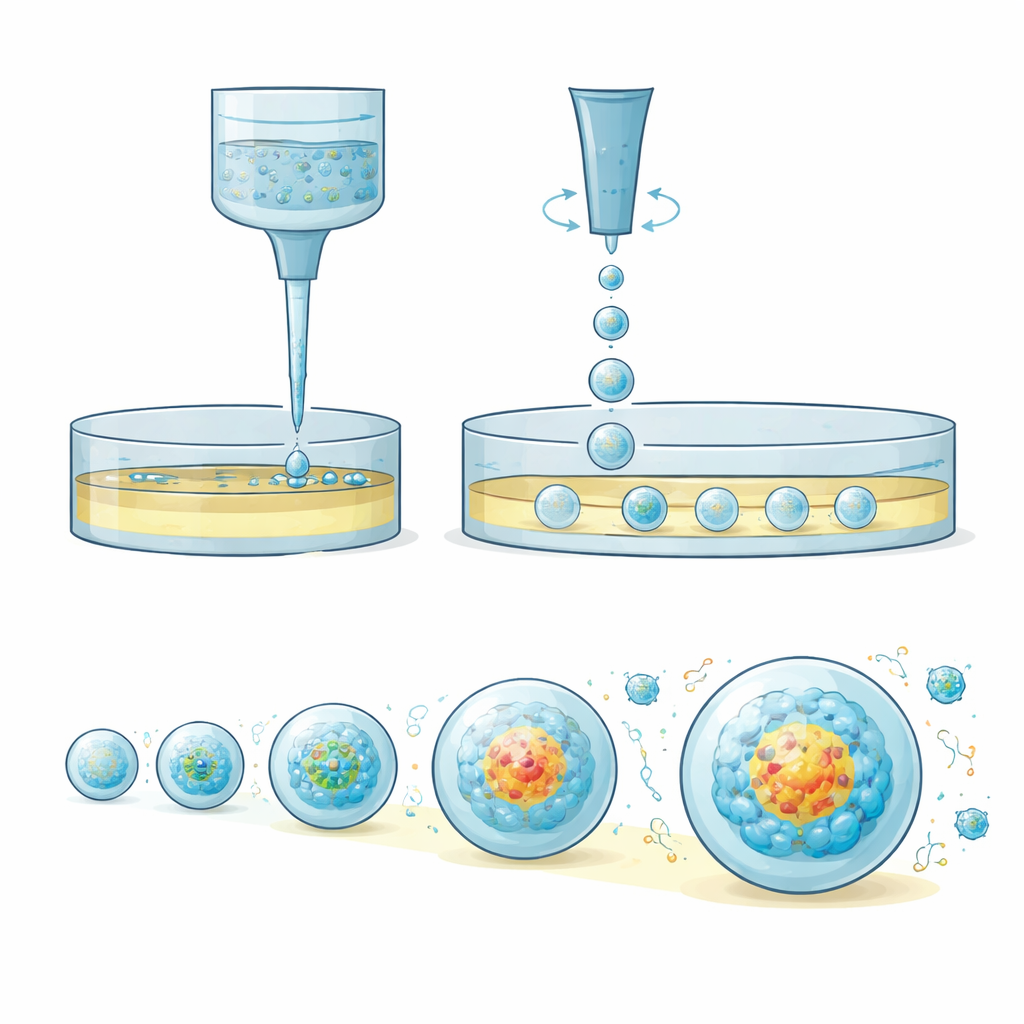
Budowanie bardziej realistycznych modeli guza i organów
Dzięki temu, że każda kropla ma niemal tę samą wielkość i zawiera precyzyjnie dobraną liczbę komórek, OsciSphere wytwarza 3D‑owe sferoidy nowotworowe o ścisłej kontroli średnicy i kształtu. Autorzy pokazują, że te mini‑modele guzów odtwarzają kluczowe cechy prawdziwych nowotworów: wolniejsze, bardziej realistyczne tempo wzrostu, wewnętrzne gradienty chemiczne, sygnały stresowe oraz programy genowe związane z inwazją i zachowaniami przypominającymi komórki macierzyste. W przypadku miniaturowych organoidów jelitowych małe kuleczki żelowe omijają problemy dyfuzyjne dużych kopuł. Organoidy rosną szybciej, wykazują bardziej zaawansowane struktury przypominające wyściółkę jelita i pozostają równomiernie żywe w całej objętości, zamiast rozwijać martwe centra, które zniekształcają wyniki eksperymentów.
Od testów leków po badania mikrobiomu i układu odpornościowego
Gdy niezawodne układy mini‑tkanek są dostępne, platforma staje się potężnym narzędziem testowym. Sferoidy nowotworowe stworzone z użyciem OsciSphere wykazują wzorce oporności na leki bliższe temu, co obserwuje się u pacjentów, podczas gdy organoidy w małych żelach są bardziej uczciwie wystawione na działanie chemioterapii niż te zatopione w grubych kopułach. Pozwoliło to zespołowi na szybkie przetestowanie kombinacji standardowych leków stosowanych w raku jelita grubego i identyfikację dawek, które współdziałają skutecznie przy stosunkowo niskich stężeniach. Poszli dalej, eksponując sferoidy nowotworowe na wydzielane molekuły pochodzące od dziesiątek bakterii jelitowych, szybko wskazując gatunki, których metabolity silnie hamują wzrost guza i uruchamiają ścieżki prowadzące do śmierci komórek nowotworowych. Wreszcie użyli organoidów pochodzących od pacjentów oraz ich własnych komórek odpornościowych, aby modelować działanie terapii immunologicznych, pokazując, że małe, dostępne mikrosfery umożliwiają infiltrację i aktywację komórek odpornościowych w sposób, którego nie dają masywne kopuły.
Jak to może zmienić onkologię precyzyjną
Mówiąc prosto, OsciSphere oferuje praktyczną drogę do hodowli tysięcy niemal identycznych mini‑guzów i mini‑organów, które zachowują się bardziej jak tkanki w organizmie, używając narzędzi, które posiada wiele laboratoriów. Zmniejszając środowisko żelowe do maleńkich, jednorodnych kulek i ściśle kontrolując liczbę komórek w każdej z nich, platforma poprawia realizm, spójność i szybkość modeli 3D stosowanych w badaniach nad rakiem. To z kolei sprawia, że testowanie leków, badania mikrobiomu oraz ocena terapii immunologicznych są bardziej wiarygodne i skalowalne. Jeśli technologia zostanie powszechnie przyjęta, może pomóc przybliżyć rzeczywistą spersonalizowaną terapię — w której terapie są najpierw testowane na miniaturowych guzach danego pacjenta, zanim zastosuje się je w klinice — do codziennej opieki onkologicznej.
Cytowanie: Li, Y., Cao, Z., Xu, Y. et al. High-fidelity bioassembly of organoids and spheroids using inertial droplet microfluidics for precision oncology and tumor microenvironment modeling. Microsyst Nanoeng 12, 152 (2026). https://doi.org/10.1038/s41378-026-01244-x
Słowa kluczowe: organoidy, sferoidy nowotworowe, mikrofluidyka, onkologia precyzyjna, mikrośrodowisko guza