Clear Sky Science · sv
Högfidel bioassembly av organoider och spheroider med inertial droppmikrofluidik för precision-onkologi och modellering av tumörmikromiljön
Varför små 3D-vävnader spelar roll för cancerbehandling
Läkare och forskare förlitar sig i allt högre grad på miniatyrer av tumörer och organ odlade i laboratoriet för att förutsäga hur verkliga patienter kommer att svara på behandling. Dessa tredimensionella cellkluster, kallade spheroider och organoider, efterliknar vävnaders struktur och beteende i kroppen mycket bättre än platta cellskikt på en platta. Ändå är dagens metoder för att odla dem ofta långsamma, slösaktiga och inkonsekventa, vilket gör det svårt att skala upp för läkemedelstester eller personaliserad cancerterapi. Denna artikel presenterar en ny plattform, kallad OsciSphere, som syftar till att massproducera högst uniforma 3D-mini‑vävnader snabbt och pålitligt, med utrustning som passar in i standardlaboratoriers arbetsflöden. 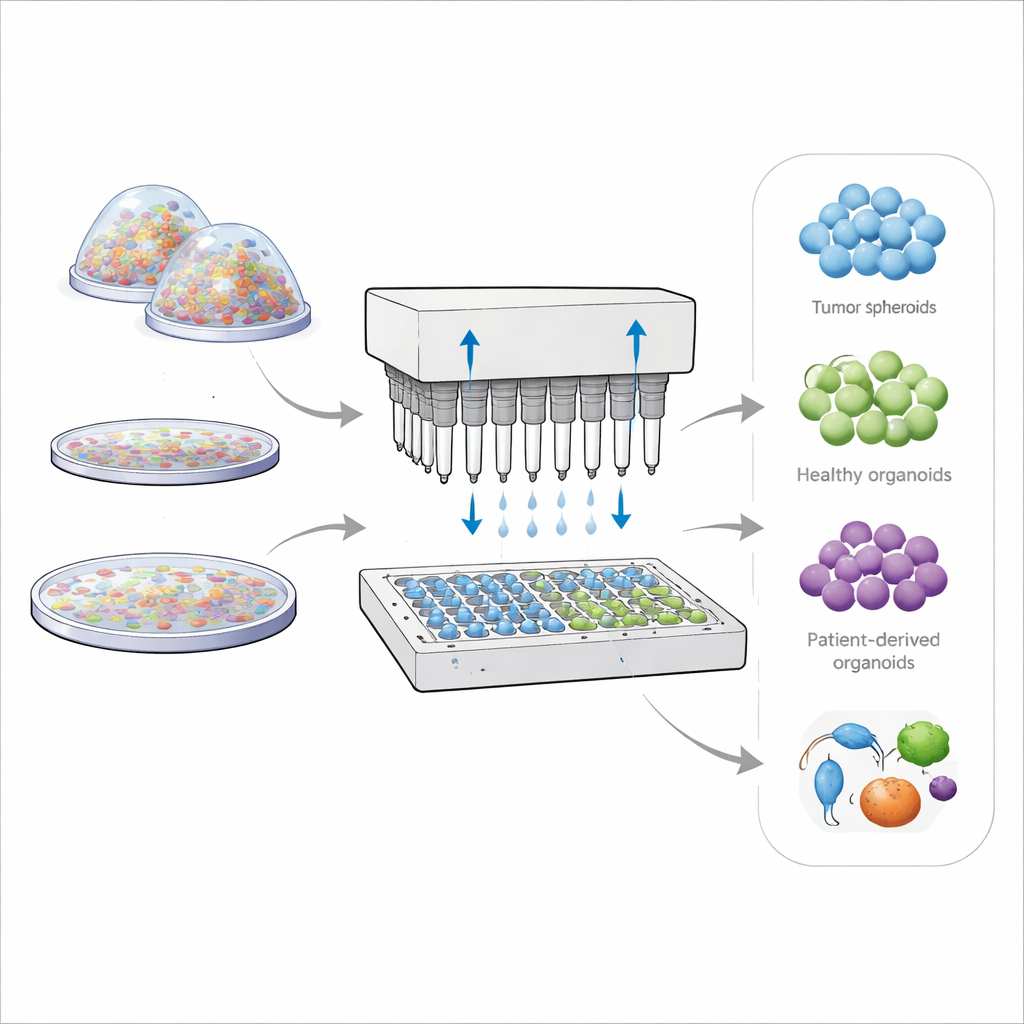
Problemet med dagens 3D-cellkulturer
De flesta nuvarande tillvägagångssätt för 3D-kulturer faller i två läger: ”scaffold‑free” system som låter celler klumpa ihop sig naturligt, och ”scaffold‑baserade” system som innesluter dem i en gel. Enklare metoder som hängande droppar eller låg‑adhesionsplattor tenderar att ge kluster i mycket varierande storlek från brunn till brunn, vilket gör läkemedelsresponserna brusiga och svåra att jämföra. Geledomer gjorda av material som Matrigel stöder mer livstrogna vävnadsstrukturer, men de är skrymmande och svåra att hantera. Inuti dessa stora domer når inte syre och näring alla celler lika väl, vilket leder till döda kärnor och ojämn tillväxt som förvränger hur vävnaderna svarar på läkemedel.
En chip‑fri metod för att skapa uniforma mini‑vävnader
OsciSphere löser dessa problem genom att omvandla tjock, cellfylld gel till många identiska små droppar direkt i vanliga laboratorieplattor, utan att använda komplexa mikrofluidiska chip. Systemet använder ett fält av oscillerande pipettspetsar som rör sig fram och tillbaka med kontrollerade hastigheter och amplituder. Denna rörelse utnyttjar tröghet snarare än känsliga ytspänningar för att nypa av likadana geldroppar i ett oljelager som ligger ovanför odlingsmedium. Temperaturkontroll håller gelen flytande under detta steg, och vid uppvärmning stelnar dropparna till små sfärer som försiktigt överförs ner i mediet. Varje solid gelssfär blir ett mini‑”hem” där celler kan samla sig till uniforma tumörspheroider eller organoider, med endast en bråkdel av den gel som normalt krävs. 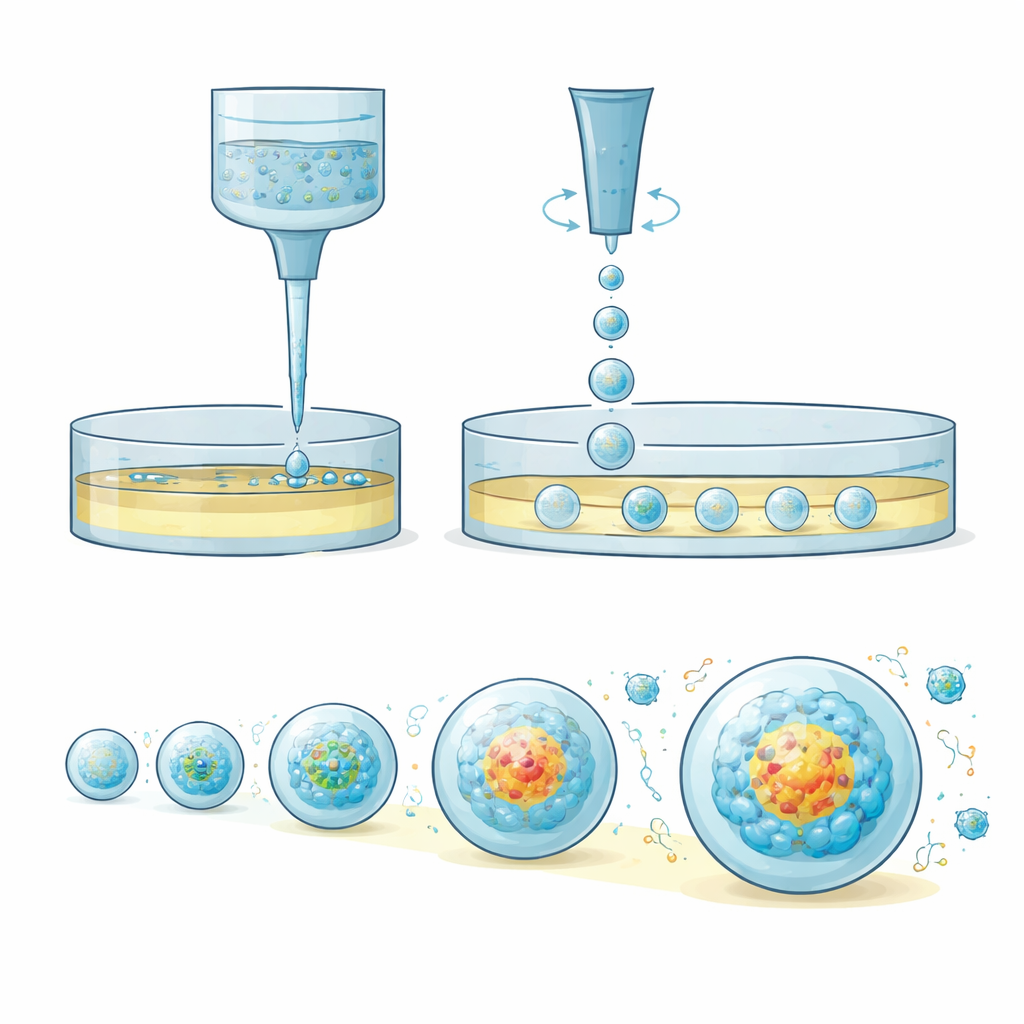
Att bygga mer realistiska tumör‑ och organmodeller
Eftersom varje dropp är nästan lika stor och innehåller ett precist anpassat antal celler, producerar OsciSphere 3D‑tumörspheroider med strikt kontroll över diameter och form. Författarna visar att dessa mini‑tumörmodeller återger viktiga kännetecken hos riktiga cancerformer: långsammare, mer realistiska tillväxthastigheter, interna kemiska gradienter, stressignaler och genprogram kopplade till invasion och stamliknande beteende. När man använde metoden för att odla miniaturiserade tarmorganoider undviker de små gelskärvorna de diffusionsbegränsningar som finns i stora domer. Organoiderna växer snabbare, visar mer avancerade strukturer som liknar tarmens slemhinna och förblir jämnt livskraftiga genom hela strukturen i stället för att utveckla döda centrar som snedvrider experimentella resultat.
Från läkemedelstester till studier av mikrobiom och immunsystem
När tillförlitliga arrayer av mini‑vävnader är på plats blir plattformen ett kraftfullt testpaket. Tumörspheroider skapade med OsciSphere visar läkemedelsresistensmönster som bättre motsvarar vad kliniker ser hos patienter, medan organoider i små gelformer är mer uppriktigt exponerade för cytostatika än de som ligger begravda i tjocka domer. Detta möjliggjorde för teamet att snabbt screena kombinationer av standardläkemedel mot kolorektal cancer och identifiera doser som fungerar effektivt tillsammans vid relativt låga koncentrationer. De gick vidare genom att utsätta tumörspheroider för sekret från dussintals tarmbakterier och identifierade snabbt arter vars metaboliter starkt hämmar tumörtillväxt och utlöser celldödssignaler i cancer. Slutligen användes patient‑härledda tumörorganoider och patientens egna immunceller för att modellera hur immunterapier fungerar, vilket visade att de små, lättillgängliga mikrosfärerna tillåter immunceller att infiltrera och aktiveras på sätt som skrymmande domer inte möjliggör.
Hur detta kan förändra precision‑onkologin
Enkelt uttryckt erbjuder OsciSphere en praktisk väg att odla tusentals nästintill identiska mini‑tumörer och mini‑organ som beter sig mer som vävnader i kroppen, med verktyg som många laboratorier redan har. Genom att krympa gelemiljön till små, enhetliga sfärer och noggrant kontrollera hur många celler som går in i varje, förbättrar plattformen realismen, konsekvensen och snabbheten i 3D‑modeller som används för cancerforskning. Detta gör i sin tur läkemedelstester, studier av mikrobiomet och utvärdering av immunterapier mer pålitliga och skalbara. Om tekniken antas i stor skala kan den bidra till att föra verkligt personaliserad behandling — där terapier testas på en patients egna mini‑tumörer innan de ges kliniskt — närmare vardaglig cancervård.
Citering: Li, Y., Cao, Z., Xu, Y. et al. High-fidelity bioassembly of organoids and spheroids using inertial droplet microfluidics for precision oncology and tumor microenvironment modeling. Microsyst Nanoeng 12, 152 (2026). https://doi.org/10.1038/s41378-026-01244-x
Nyckelord: organoider, tumörspheroider, mikrofluidik, precision-onkologi, tumörmikromiljö