Clear Sky Science · tr
Hepatit B virüsüyle ilişkili foliküler lenfomanın erken nüksünde çok hücreli dinamikleri ortaya çıkaran mekânsal profilleme
Hastalar ve aileleri için bunun önemi
Hepatit B virüsü (HBV) enfeksiyonu yaşayan veya iyileşen bazı kişiler, foliküler lenfoma adı verilen yaygın bir kan kanseri türünü geliştirebiliyor. Modern kemoterapi‑immünoterapiye rağmen, bu hastaların birçoğunda hastalık iki yıl içinde hızla geri dönebiliyor; klinisyenlerin POD24 olarak adlandırdığı bu durum bir uyarı işareti. Bu çalışma, tümör hücreleri ile bağışıklık hücrelerinin lenf düğümleri içinde yerinde nasıl etkileştiğini izlemek için gelişmiş “mekânsal” gen‑haritalama araçlarını kullanarak, HBV ilişkili foliküler lenfomanın neden erken nüks edebileceğini ve yeni tedavilerin nerede devreye girebileceğini ortaya koyuyor.
Tümörlerin üç boyutlu incelenmesi
Araştırmacılar, HBV enfeksiyon öyküleri ve viral DNA düzeyleri dikkatle izlenmiş, nüks etmiş foliküler lenfoma tanılı 17 kişiden alınan lenf düğümü örneklerini inceledi. CosMx Spatial Molecular Imaging adlı bir teknoloji kullanarak, dokudaki her hücrenin tam konumunu korurken on binlerce bireysel hücrede yaklaşık 1.000 genin aktivitesini ölçtüler. Bunu tek hücreli RNA dizileme verileriyle birleştirerek ana hücre gruplarını etiketlediler: kanserli B hücreleri, sağlıklı B hücreleri, çeşitli T hücresi tipleri, makrofajlar, foliküler dendritik hücreler (FDC’ler) ve fibroblastlar. Bu yaklaşım, hangi hücrelerin bulunduğunu göstermekle kalmayıp kimin kimin yanında oturduğunu ve hangi genleri etkinleştirdiklerini gösteren ayrıntılı “haritalar” üretti.
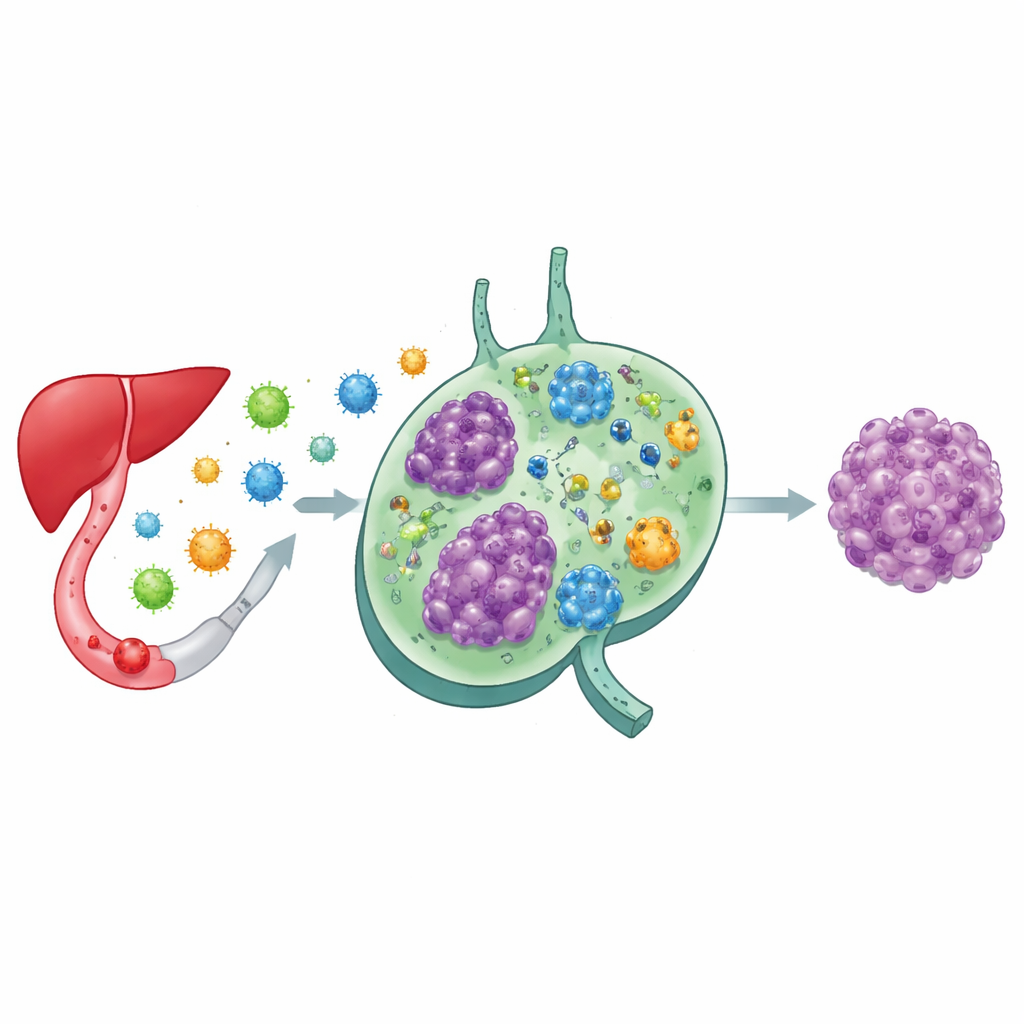
Kronik hepatit B’nin tümör çevresini nasıl yeniden şekillendirdiği
Tedavi öncesi ve sonrası alınan örnekleri ve farklı HBV DNA düzeylerini karşılaştıran ekip, kronik veya uzun süreli HBV enfeksiyonunun ayırt edici bir bağışıklık peyzajı ile birlikte gittiğini gördü. Yüksek viral yük taşıyan hastaların tümörleri, geçmiş enfeksiyonları “hatırlayan” uzun ömürlü bellek B hücreleri, savaşma gücünü büyük ölçüde kaybetmiş tükenmiş T hücreleri ve yoğun FDC ağları bakımından zengindi. Antiviral tedavi HBV DNA’sını düşürdükçe veya temizledikçe bu tükenmiş T hücreleri, düzenleyici T hücreleri ve FDC’ler sayıca azaldı ve malign ile sağlıklı hücreler arasındaki denge kaydı. Bu desen, sürekli bir viral antijen akışının bağışıklık sistemini tükenmeye ittiği ve kanser hücrelerini korumaya yardımcı olabileceği fikrini destekliyor.
Gizli bir bellek‑benzeri kanser hücresi havuzu
Kanserli B hücrelerine daha derinlemesine bakıldığında, bilim insanları dört ana malign program buldular. İkisi klasik foliküler lenfoma hücrelerine benziyordu, biri daha çok plazma hücrelerine benziyordu ve bellek B hücresi‑benzeri malign (MBLM) alt tipi adını verdikleri bir grup hem normal bellek B hücrelerinin hem de tümör hücrelerinin özelliklerini taşıyordu. Genetik “yolculuk” analizleri, sıradan bellek B hücrelerinden atipik bir ara aşamadan geçerek bu bellek‑benzeri malign hücrelere doğru bir yol olduğunu öne sürdü. MBLM hücreleri özellikle yüksek HBV yükü ve uzun süreli enfeksiyonlu tümörlerde yaygındı ve mekânsal olarak bellek B hücrelerine ve belirli FDC alt kümelerine yakın kümeler oluşturma eğilimindeydi. Bu durum, HBV ve tümör antijenleri tarafından tekrarlanan şekilde uyarılan bellek B hücrelerinin malign evrim için önemli bir tohum yatağı olduğunu işaret ediyor.
Sorunu besleyen destek hücreleri
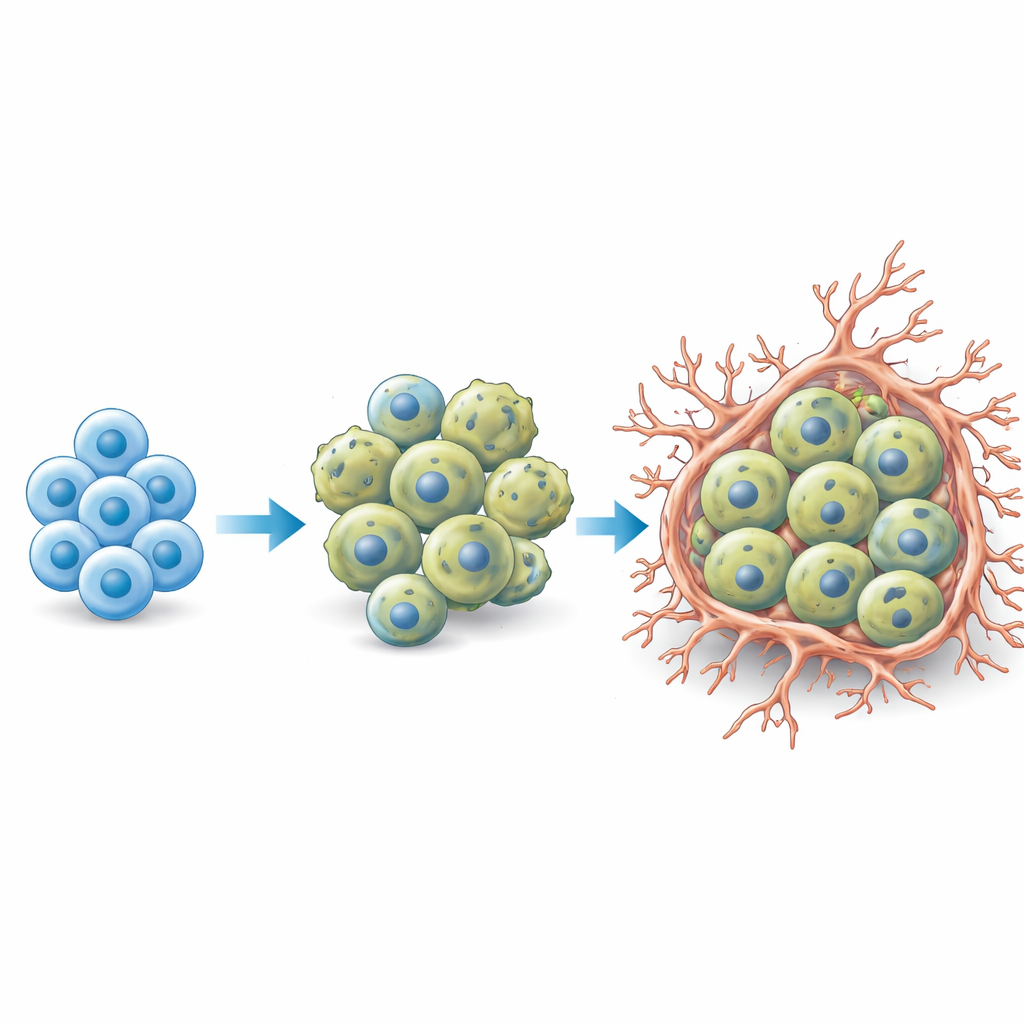
Çalışma ayrıca foliküler dendritik hücreleri dört işlevsel türe ayırdı: T hücrelerini aktive eden hücreler, antijen taşıma ve sunumuyla ilgili hücreler, adezyona odaklı hücreler ve hepatit B yollarıyla ilişkili genler açısından zenginleştirilmiş “virus‑protein taşıma” grubu. HBV‑yüksek ve uzun süreli taşıyıcılarda, virüsle ilişkili ve antijen‑taşıma FDC tipleri hakim oldu ve tümör bölgeleri etrafında iltihaplı ancak immünsuprese edilmiş bir ağ oluşturdular. Mekânsal analizler, MBLM hücreleri ile bu FDC’lerin, hücre göçünü lenf düğümlerine yönlendiren ve NF‑κB gibi büyümeyi destekleyen yolları aktive ettiği bilinen CCL21–CCR7 ekseni ile bağlanan sıkı topluluklar oluşturduğunu gösterdi. Farklı kemoterapi rejimleri bu malign ve FDC alt kümelerini farklı şekillerde değiştirdi; bu da bazı tedavilerin yok edilmesi zor hücre popülasyonlarını geride bırakıp POD24 için zemin hazırlamasını açıklamaya yardımcı oluyor.
Gelecekteki bakım için ne anlama geliyor
Bir uzman olmayan için temel mesaj şu: HBV ilişkili foliküler lenfoma sadece “aynı kanserin üzerine eklenmiş bir virüs” değil. Kronik hepatit B, bellek‑benzeri bir kanser hücresi havuzunu besleyen ve yerel destek hücrelerini yeniden kabloya bağlayan benzersiz bir tümör ekosistemi şekillendiriyor; bunlar birlikte standart tedavi sonrasında erken nüksü tetikliyor. Bu bellek‑benzeri malign hücreleri, onların HBV tarafından şekillendirilen FDC ortaklarını ve bunları birbirine bağlayan sinyal yollarını belirleyerek, çalışma tanı anında yüksek riskli hastaları işaretleyebilecek yeni biyobelirteçleri öne çıkarıyor ve bellek B hücresi kaderini kontrol eden yollar, CCL21–CCR7 sinyalleşmesi ve PTPRCAP ile CD37 gibi belirli yüzey proteinleri gibi hedefleri antiviral tedaviyle birlikte kullanılarak hastalığın erken geri dönüşünü geciktirmeye veya önlemeye yönelik yeni ilaç hedefleri öneriyor.
Atıf: Deng, Y., Zhang, Q., Jia, Z. et al. Spatial profiling uncovers multicellular dynamics in early relapse of hepatitis B virus-associated follicular lymphoma. Commun Biol 9, 551 (2026). https://doi.org/10.1038/s42003-026-09837-y
Anahtar kelimeler: hepatit B, foliküler lenfoma, tümör mikroi̇ncelemesi, mekânsal transkriptomik, erken nüks