Clear Sky Science · pt
Perfilamento espacial revela dinâmicas multicelulares no recidiva precoce do linfoma folicular associado ao vírus da hepatite B
Por que isso importa para pacientes e famílias
Algumas pessoas que vivem com infecção pelo vírus da hepatite B (HBV) ou que se recuperaram dela desenvolvem um tipo comum de câncer hematológico chamado linfoma folicular. Mesmo após quimio‑imunoterapia moderna, muitos desses pacientes têm recidiva rápida da doença dentro de dois anos, um evento de alerta que os médicos chamam de POD24. Este estudo usa ferramentas avançadas de mapeamento gênico “espacial” para observar, in situ, como células tumorais e células imunes interagem dentro dos linfonodos, revelando por que o linfoma folicular associado ao HBV pode recidivar precocemente e onde novos tratamentos poderiam intervir.
Olhando para dentro dos tumores em três dimensões
Os pesquisadores estudaram amostras de linfonodos de 17 pessoas com linfoma folicular recorrente cujos históricos de infecção por HBV e níveis de DNA viral foram monitorados cuidadosamente. Usando uma tecnologia chamada CosMx Spatial Molecular Imaging, mediram a atividade de cerca de 1.000 genes em dezenas de milhares de células individuais mantendo a posição exata de cada célula no tecido. Combinaram isso com dados de sequenciamento de RNA de célula única para rotular os principais grupos celulares: células B cancerosas, células B saudáveis, vários tipos de células T, macrófagos e células dendríticas foliculares (FDCs), e fibroblastos. Essa abordagem produziu “mapas” detalhados que mostram não apenas quais células estão presentes, mas quem está ao lado de quem e quais genes cada uma está ativando.
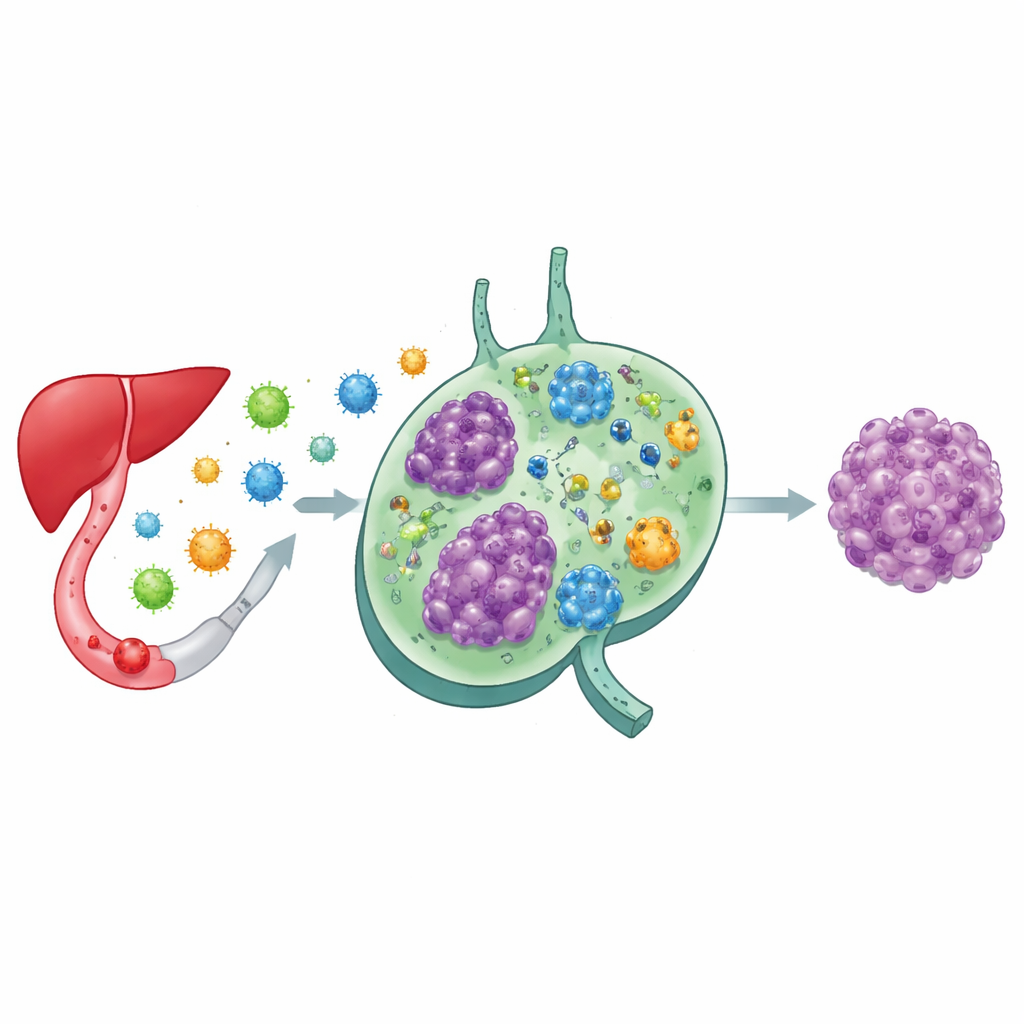
Como a hepatite B crônica remodela o bairro tumoral
Comparando amostras coletadas antes e depois do tratamento, e entre diferentes níveis de DNA do HBV, a equipe observou que a infecção crônica ou de longa duração pelo HBV anda de mãos dadas com um paisagem imune distintiva. Tumores de pacientes com altas cargas virais eram ricos em células B de memória (as células de longa vida que lembram infecções passadas), células T exauridas que perderam grande parte de seu poder de ataque, e redes densas de FDCs. À medida que a terapia antiviral reduzia ou eliminava o DNA do HBV, essas células T exauridas, células T reguladoras e FDCs diminuíam em número, e o equilíbrio entre células malignas e saudáveis mudava. Esse padrão apoia a ideia de que um fluxo constante de antígenos virais empurra o sistema imune para o esgotamento e pode ajudar a proteger as células cancerosas.
Um reservatório oculto de células cancerosas com características de memória
Aprofundando-se nas células B cancerosas, os cientistas encontraram quatro programas malignos principais. Dois se assemelhavam às células clássicas do linfoma folicular, um lembrava mais células plasmáticas, e um, chamado subtipo maligno semelhante a célula B de memória (MBLM), carregava características tanto de células B de memória normais quanto de células tumorais. Análises de "trajetória" genética sugeriram um caminho desde células B de memória comuns, passando por um intermediário atípico, até essas células malignas semelhantes a memória. Células MBLM foram especialmente comuns em tumores com altas cargas de HBV e infecção de longa duração e tendiam a se agrupar espacialmente próximas às células B de memória e a certos subconjuntos de FDCs. Isso aponta para as células B de memória, estimuladas repetidamente por antígenos do HBV e do tumor, como um viveiro-chave para a evolução maligna.
Células de suporte que alimentam o problema
O estudo também dividiu as células dendríticas foliculares em quatro perfis funcionais: células que ativam células T, células que lidam com transporte e apresentação de antígeno, células focadas em adesão, e um grupo de “transporte de proteína viral” enriquecido para genes ligados a vias da hepatite B. Em portadores de HBV com carga alta e de longa duração, os tipos de FDC ligados ao vírus e ao transporte de antígeno dominaram, formando uma rede inflamada porém imunossuprimida ao redor das áreas tumorais. Análises espaciais mostraram que células MBLM e essas FDCs formavam comunidades coesas conectadas por um sinal químico chave, o eixo CCL21–CCR7, conhecido por guiar a migração celular para os linfonodos e ativar vias promotoras de crescimento como NF‑κB. Regimes quimioterápicos diferentes deslocaram esses subconjuntos malignos e de FDCs de maneiras distintas, ajudando a explicar por que alguns tratamentos deixam populações celulares difíceis de erradicar e preparam o terreno para POD24.
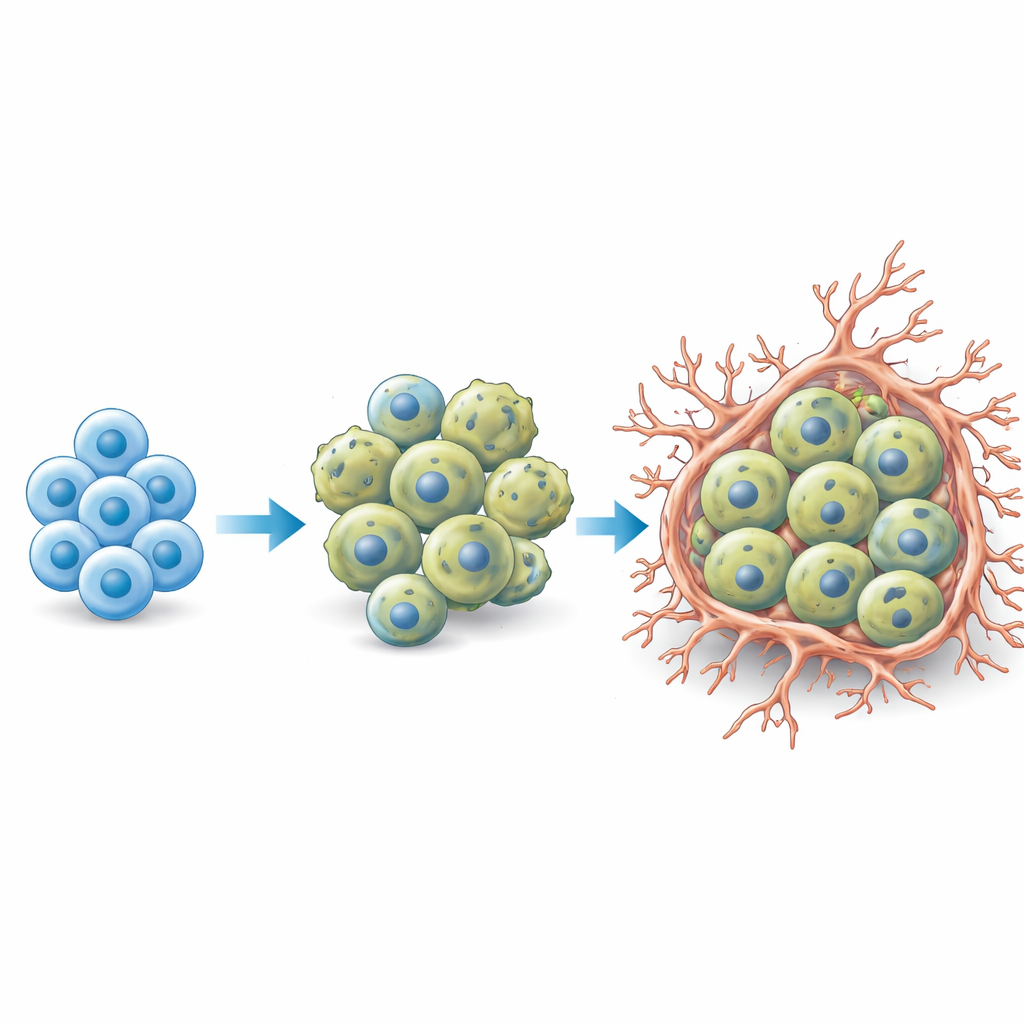
O que isso significa para os cuidados futuros
Para um não especialista, a mensagem central é que o linfoma folicular associado ao HBV não é apenas “o mesmo câncer mais um vírus.” A hepatite B crônica molda um ecossistema tumoral único que nutre um reservatório de células cancerosas com características de memória e reconfigura células de suporte locais, impulsionando em conjunto a recidiva precoce após a terapia padrão. Ao identificar essas células malignas tipo‑memória, suas parceiras FDC moldadas pelo HBV e as vias de sinalização que as conectam, este trabalho destaca novos biomarcadores que podem sinalizar pacientes de alto risco no diagnóstico e sugere alvos farmacológicos — como vias que controlam o destino das células B de memória, sinalização CCL21–CCR7 e proteínas de superfície específicas como PTPRCAP e CD37 — que poderiam ser combinados com terapia antiviral para atrasar ou prevenir o retorno precoce da doença.
Citação: Deng, Y., Zhang, Q., Jia, Z. et al. Spatial profiling uncovers multicellular dynamics in early relapse of hepatitis B virus-associated follicular lymphoma. Commun Biol 9, 551 (2026). https://doi.org/10.1038/s42003-026-09837-y
Palavras-chave: hepatite B, linfoma folicular, microambiente tumoral, transcriptômica espacial, recidiva precoce