Clear Sky Science · tr
Brca1 haploinsufficiency rat modelinde spontan ve radyasyona bağlı meme karsinomlarının mutasyon profilleri
Bu araştırmanın aileler için önemi
BRCA1 geninde bir değişiklik miras alan kişiler, meme kanseri riski açısından çok daha yüksek bir olasılıkla yaşar ve pek çoğu genç yaşta tarama ve koruyucu cerrahi gibi kararlarla karşı karşıya kalır. Yine de bilim insanları, tek kusurlu bir kopyanın kanser için nasıl zemin hazırladığını —özellikle tıbbi radyasyona maruziyetten sonra— tam olarak anlamış değiller. Bu çalışma, tümörlerin DNA düzeyine bakmak için özel olarak tasarlanmış bir sıçan modeli kullanıyor ve görünüşte basit bir soruyu soruyor: BRCA1 taşıyıcılarının kanser hücrelerinde gerçekte neler ters gidiyor?
Durumu kurmak: ince bir gen kusuru ve radyasyon
BRCA1 en çok genomun bekçisi olarak bilinir; hücrelerin DNA’daki tehlikeli kırıkları onarmasına yardımcı olur. On yıllarca araştırmacılar, kanserin bir hücrede her iki BRCA1 kopyası da işlevsiz hale geldikten sonra ortaya çıktığını varsaydılar. Ancak daha yeni çalışmalar, yalnızca bir çalışan kopyaya sahip olmanın —“haploinsufficiency” adı verilen durum— dokuları kanser yönünde eğebileceğini öne sürüyor. Bu erken aşamayı incelemek için yazarlar, bir normal ve bir kırpılmış Brca1 genine sahip sıçanları kullandılar; bu, insan BRCA1 taşıyıcılarını yakın şekilde taklit ediyor. Bu sıçanların bazıları ile karşılaştırma amacıyla normal sıçanlar gençlikte tek doz radyasyona maruz bırakıldı; bu maruziyet, meme dokusundaki DNA’yı zarar verebilen bazı tıbbi maruziyetlere tür olarak benzese de (miktar olarak değil) aynı düzeyde değildi.
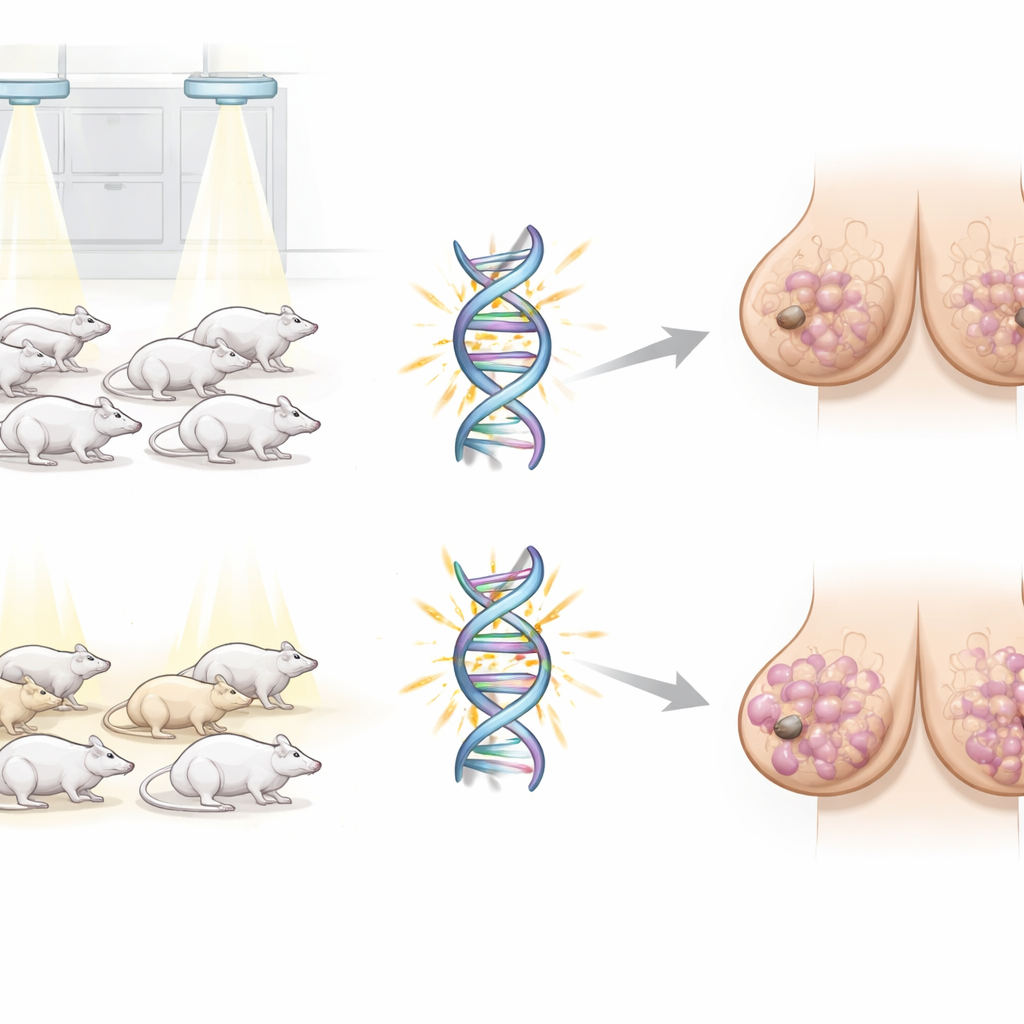
Tümörlerin içini görmek: DNA değişikliklerini saymak
Araştırma ekibi, ya spontan ya da radyasyon sonrası oluşan meme tümörlerini topladı ve ardından genomun neredeyse tüm kodlayan bölgelerini okuyan bir teknik olan tüm-ekzom dizilemesi uyguladı. Tek harf substitüsyonları, küçük ekleme ve silinmeler ile daha büyük DNA segmentlerinin kazanımları ya da kayıpları gibi farklı türde DNA değişikliklerini saydılar. Şaşırtıcı şekilde, taşıyıcı sıçanların ve normal sıçanların tümörleri, hayvanların radyasyona maruz kalıp kalmamasına bakılmaksızın, genel sayı ve desen bakımından benzerdi. İleri evre insan kanserlerinde görülen BRCA1 başarısızlığının klasik izleri —belirli mutasyon “imzalarının” ağır yükü— taşıyıcı sıçanlarda güçlü biçimde zenginleşmemişti; bu da bu işaretlerin genin tamamen kaybedildiği daha sonraki aşamalara ait olduğunu destekliyor.
Ayırt edici bir parmakizi, ama daha fazla kaos değil
Araştırmacılar, DNA hasarının nasıl biriktiğini tanımlayan ayrıntılı “mutasyon imzalarına” daha derinlemesine baktıklarında bir fark buldular. Büyük insan kanseri veri setlerinde bilinen ama henüz iyi anlaşılmamış, eşleşmiş baz değişikliklerini içeren belirli bir desen yalnızca taşıyıcı sıçanların tümörlerinde ortaya çıktı. Bu, BRCA1’in kısmi kaybının hücreleri rastgele hasarın patlamasına sürüklemek yerine genomda belirli, ince bir değişim moduna yönlendirebileceğine işaret ediyor. Aynı zamanda, mutasyonların ve büyük DNA kopya değişikliklerinin genel düzeyi gruplar arasında karşılaştırılabilir kaldı; bu da standart dizileme ile ölçülen yaygın genetik istikrarsızlık evresinin BRCA1 taşıyıcılarında kaçınılmaz olduğu yaygın görüşüne itiraz ediyor.
Taşıyıcı tümörlerde daha az klasik “sürücü” darbe
En beklenmedik sonuç, ekip “sürücü” mutasyonlara —kötücül yönelimi aktif olarak teşvik ettiği düşünülen iyi bilinen kanser genlerindeki DNA değişiklikleri— odaklandığında ortaya çıktı. Normal sıçanların radyasyona bağlı tümörlerinde bu tür sürücü mutasyonlar nispeten yaygındı. Oysa Brca1 taşıyıcı sıçanların radyasyona bağlı tümörlerinde bu tanınmış sürücü darbelerin sayısı anlamlı şekilde daha azdı ve eksomda bariz bir sürücü mutasyon göstermeyen daha fazla tümör vardı. Bu, kısmi BRCA1 kaybı bağlamında radyasyonun, protein kodlayan genlerde güçlü bir ayak izi bırakmayan yollarla meme kanserini teşvik edebileceğini; büyük yapısal yeniden düzenlemeler, DNA üzerindeki kimyasal etiketler (epigenetik değişiklikler) veya etrafındaki destekleyici doku ortamında uzun vadeli değişimler gibi mekanizmalar yoluyla etkili olabileceğini düşündürür.
BRCA1 riskini anlamak için ne anlama geliyor
Bir eğitimli olmayan okuyucu için merkezi mesaj sezgisel olarak çelişkili ama önemli: bu hayvan modelinde BRCA1’in bir bozuk kopyasını taşımak, tümörler içinde nokta nokta daha fazla DNA hatası oluşmasına doğrudan yol açmıyor. Bunun yerine, meme kanserlerinin birçok klasik genetik “motor arızasından” kaçınarak ortaya çıkmasına olanak tanıyor gibi görünür. Yazarlar, BRCA1 haploinsufficiency durumunun, standart gen odaklı testlerin kaçırabileceği büyük ölçekli DNA yeniden düzenlemeleri, epigenetik kaymalar veya tümör çevresindeki destek hücrelerdeki değişiklikler gibi alternatif kanser yollarını açabileceğini öne sürüyor. Bu gizli yolları anlamak, BRCA1 varyantlarını miras alan kişiler için daha iyi erken tespit, daha güvenli radyasyon kullanımı ve hedeflenmiş koruyucu stratejiler tasarlamak adına kritik olacaktır.
Atıf: Nakamura, Y., Daino, K., Ishikawa, A. et al. Mutational profiles of spontaneous and radiation-related mammary carcinomas in a rat model of Brca1 haploinsufficiency. Sci Rep 16, 10291 (2026). https://doi.org/10.1038/s41598-026-41240-9
Anahtar kelimeler: BRCA1, meme kanseri riski, radyasyon maruziyeti, tümör genetiği, DNA onarımı