Clear Sky Science · it
Profili mutazionali dei carcinomi mammari spontanei e correlati a radiazioni in un modello murino di insufficienza di Brca1
Perché questa ricerca conta per le famiglie
Le persone che ereditano una alterazione del gene BRCA1 convivono con un rischio molto aumentato di cancro al seno e molte devono prendere decisioni su screening e interventi preventivi in età precoce. Tuttavia gli scienziati non comprendono ancora del tutto come il possesso di una sola copia difettosa di questo gene predisponi al cancro, in particolare dopo l’esposizione a radiazione medica. Questo studio utilizza un modello di ratto appositamente ingegnerizzato per osservare i tumori a livello del DNA, ponendo una domanda apparentemente semplice: che cosa va effettivamente storto nelle cellule tumorali dei portatori di BRCA1?
Contesto: un difetto genetico sottile e le radiazioni
BRCA1 è noto soprattutto come guardiano del genoma, aiutando le cellule a riparare rotture pericolose del DNA. Per decenni i ricercatori hanno assunto che il cancro insorgesse solo dopo la perdita di entrambe le copie di BRCA1 in una cellula. Tuttavia lavori più recenti suggeriscono che avere una sola copia funzionante — uno stato definito “insufficienza” o haploinsufficienza — possa già inclinare i tessuti verso il cancro. Per sondare questa fase iniziale, gli autori hanno utilizzato ratti che portano una copia normale e una copia troncata del gene Brca1, riproducendo da vicino la situazione dei portatori umani di varianti BRCA1. Alcuni di questi ratti, insieme a ratti normali di controllo, sono stati esposti a una singola dose di radiazione in giovinezza, simile per tipo (sebbene non per entità) ad alcune esposizioni mediche che possono danneggiare il DNA del tessuto mammario.
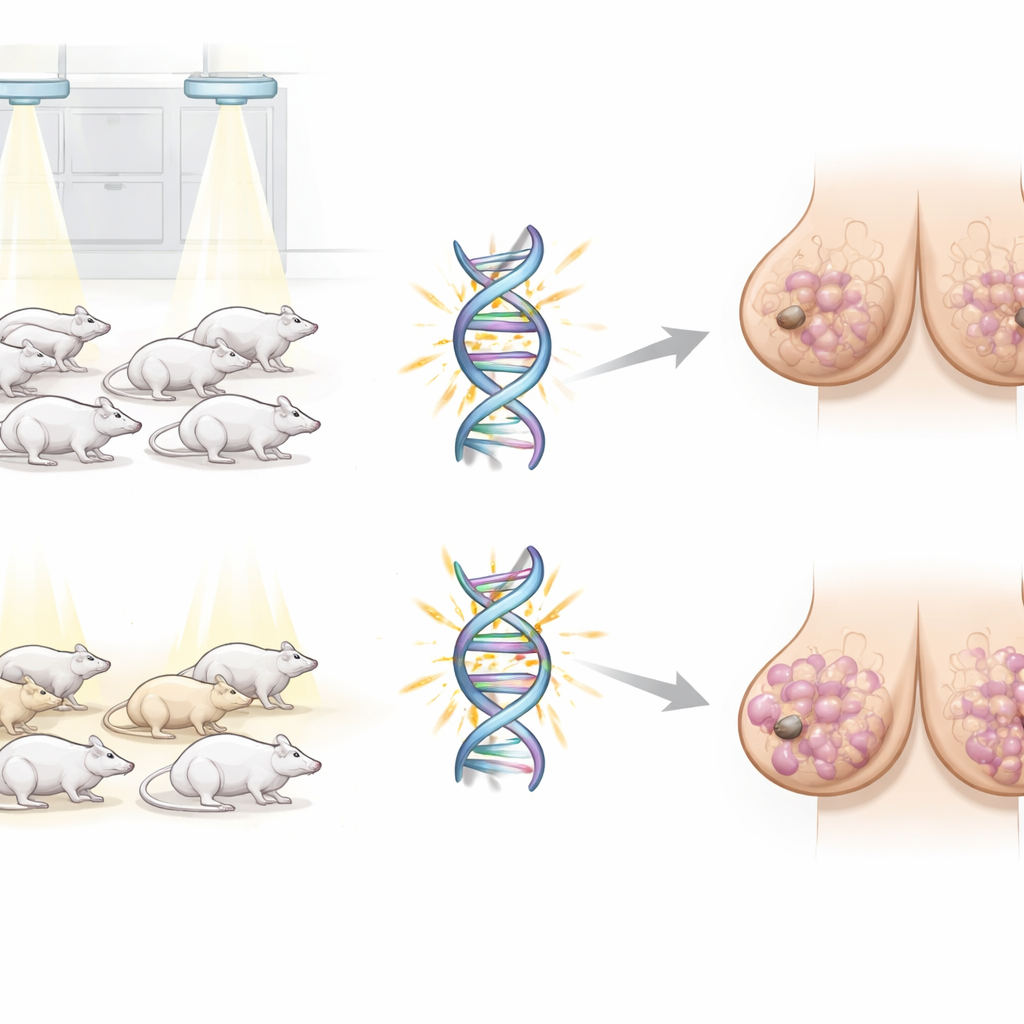
Analizzare i tumori: contare le alterazioni del DNA
Il gruppo ha raccolto tumori mammari insorti spontaneamente o dopo esposizione a radiazioni e ha eseguito il sequenziamento dell’esoma completo, una tecnica che legge quasi tutte le regioni codificanti dei geni. Hanno contato diversi tipi di alterazioni del DNA: sostituzioni di singole basi, piccole inserzioni e delezioni, e guadagni o perdite di segmenti di DNA più grandi. Sorprendentemente, i tumori dei ratti portatori e quelli dei ratti normali presentavano numeri complessivi e schemi di mutazioni simili, indipendentemente dall’esposizione a radiazioni. I segni classici del malfunzionamento di BRCA1 osservati nei tumori umani avanzati — un elevato carico di certe “firme” mutazionali — non risultavano fortemente arricchiti nei ratti portatori, rafforzando l’idea che tali caratteristiche appartengano a fasi successive in cui il gene è completamente perso.
Un’impronta distintiva, ma non più caos
Analizzando più a fondo le “firme mutazionali” che descrivono come si accumula il danno al DNA, i ricercatori hanno trovato una differenza notevole. Un particolare schema che coinvolge cambiamenti di basi accoppiate, noto da grandi dataset di tumori umani ma non ancora ben compreso, è apparso solo nei tumori dei ratti portatori. Questo suggerisce che la perdita parziale di BRCA1 possa indirizzare le cellule verso una modalità specifica e sottile di alterazione del genoma invece di provocare una semplice esplosione di danno casuale. Allo stesso tempo, il livello complessivo di mutazioni e le grandi variazioni del numero di copie di DNA sono rimasti comparabili tra i gruppi, opponendosi all’immagine ricorrente secondo cui i portatori di BRCA1 procederebbero inevitabilmente attraverso una fase di instabilità genetica sfrenata misurabile con il sequenziamento standard.
Meno “driver” classici nei tumori dei portatori
Il risultato più inaspettato è emerso quando il gruppo si è concentrato sulle mutazioni “driver” — alterazioni in geni noti per spingere attivamente le cellule verso la malignità. Nei tumori correlati a radiazioni dei ratti normali, tali mutazioni driver erano relativamente comuni. Al contrario, nei tumori correlati a radiazioni dei ratti portatori di Brca1 si sono riscontrati significativamente meno di questi driver riconosciuti, e un maggior numero di tumori non mostrava alcuna mutazione driver ovvia nell’esoma. Ciò suggerisce che, nel contesto dell’insufficienza parziale di BRCA1, la radiazione possa promuovere il cancro mammario attraverso vie che non lasciano una forte impronta nei geni codificanti proteine, come grandi riorganizzazioni strutturali, marcature chimiche sul DNA che alterano l’attività genica o cambiamenti a lungo termine nell’ambiente tissutale circostante.
Cosa significa per la comprensione del rischio BRCA1
Per un lettore non specialista il messaggio centrale è controintuitivo ma importante: in questo modello animale, portare una copia danneggiata di BRCA1 non provoca semplicemente un maggior numero di errori puntiformi all’interno dei tumori. Piuttosto, sembra permettere l’insorgenza di tumori mammari evitando molte delle classiche “rotture” genetiche che si osservano di solito nei tumori. Gli autori propongono che l’haploinsufficienza di BRCA1 possa aprire percorsi alternativi verso il cancro, che possono coinvolgere riorganizzazioni su larga scala del DNA, spostamenti epigenetici o cambiamenti nelle cellule di supporto intorno al tumore — processi che i test focalizzati sui geni standard possono non rilevare. Comprendere queste vie nascoste sarà cruciale per progettare strategie migliori di diagnosi precoce, un uso più sicuro delle radiazioni e interventi di prevenzione mirati per le persone che ereditano varianti di BRCA1.
Citazione: Nakamura, Y., Daino, K., Ishikawa, A. et al. Mutational profiles of spontaneous and radiation-related mammary carcinomas in a rat model of Brca1 haploinsufficiency. Sci Rep 16, 10291 (2026). https://doi.org/10.1038/s41598-026-41240-9
Parole chiave: BRCA1, rischio di cancro al seno, esposizione a radiazioni, genetica dei tumori, riparazione del DNA