Clear Sky Science · pl
Profile mutacyjne spontanicznych i związanych z promieniowaniem raków sutka w modelu szczura z haploinsuficjencją Brca1
Dlaczego to badanie ma znaczenie dla rodzin
Osoby dziedziczące zmianę w genie BRCA1 żyją z wyraźnie zwiększonym ryzykiem raka piersi, a wiele z nich musi w młodym wieku podejmować decyzje dotyczące badań przesiewowych i zabiegów zapobiegawczych. Naukowcy wciąż jednak nie rozumieją w pełni, jak posiadanie tylko jednej wadliwej kopii tego genu przygotowuje grunt pod rozwój nowotworu, zwłaszcza po ekspozycji na medyczne promieniowanie. W tym badaniu wykorzystano specjalnie zmodyfikowany model szczura, by przyjrzeć się nowotworom na poziomie DNA i odpowiedzieć na pozornie proste pytanie: co tak naprawdę idzie nie tak w komórkach nowotworowych nosicieli BRCA1?
Scenariusz: subtelna wada genu i promieniowanie
BRCA1 jest najlepiej znany jako strażnik genomu, pomagający komórkom naprawiać niebezpieczne pęknięcia DNA. Przez dekady zakładano, że nowotwór pojawia się dopiero wtedy, gdy obie kopie BRCA1 zostaną utracone w komórce. Nowsze badania sugerują jednak, że posiadanie tylko jednej działającej kopii — stan zwany „haploinsuficjencją” — może już przesuwać tkanki w kierunku nowotworzenia. Aby zbadać ten wczesny etap, autorzy użyli szczurów niosących jedną normalną i jedną zredukowaną wersję genu Brca1, co wiernie naśladuje nosicieli BRCA1 u ludzi. Część tych szczurów oraz szczury kontrolne zostały w młodości poddane pojedynczej dawce promieniowania, podobnej pod względem rodzaju (choć niekoniecznie wielkości) do niektórych ekspozycji medycznych, które mogą uszkadzać DNA tkanki piersi.
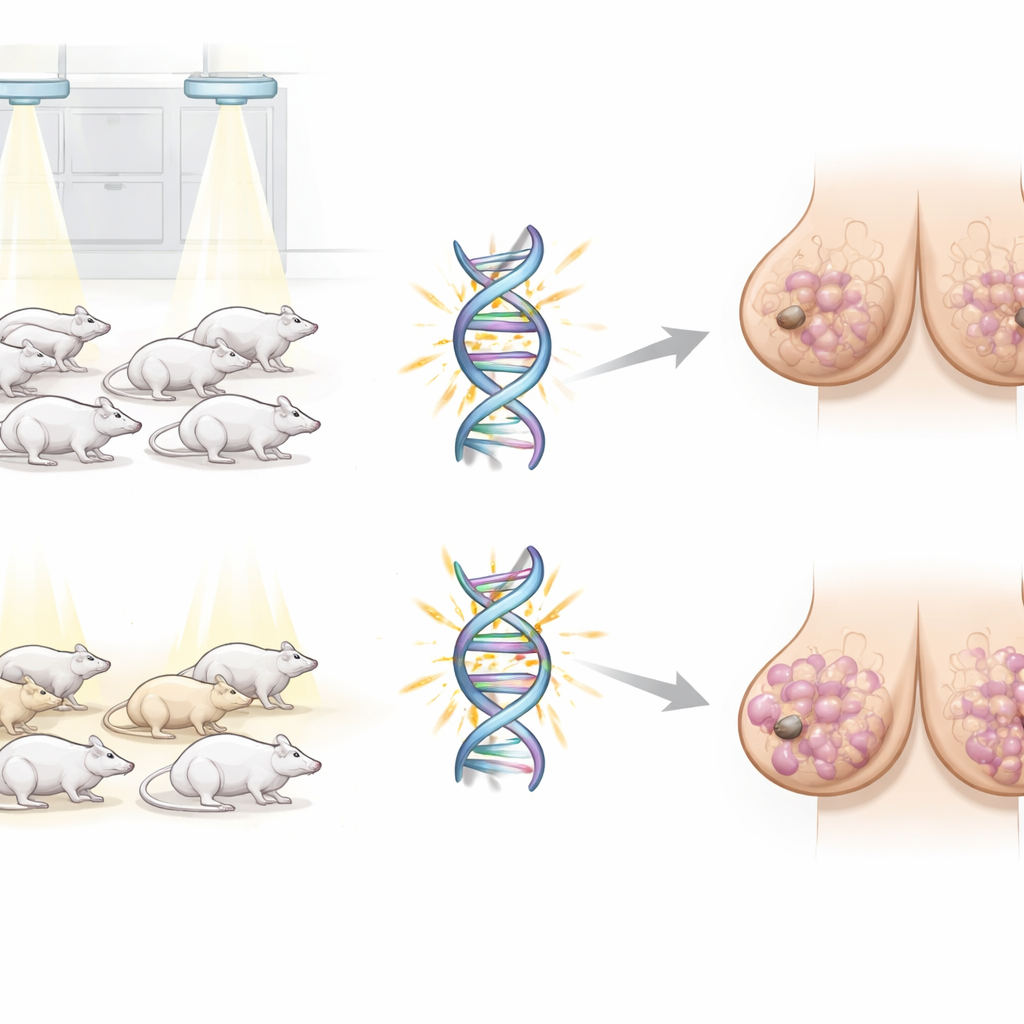
Wgląd w nowotwory: zliczanie zmian w DNA
Zespół zebrał guzy sutka, które powstały spontanicznie lub po ekspozycji na promieniowanie, a następnie przeprowadził sekwencjonowanie eksomowe, technikę odczytującą niemal wszystkie kodujące geny regiony genomu. Zliczono różne rodzaje zmian w DNA: pojedyncze substytucje nukleotydów, małe insercje i delecje oraz zyski lub utraty większych fragmentów DNA. Ku zaskoczeniu, guzy od szczurów-nosicieli i od szczurów normalnych zawierały podobne ogólne liczby i wzorce tych mutacji, niezależnie od tego, czy zwierzęta były napromieniowane. Klasyczne oznaki całkowitej utraty funkcji BRCA1 widoczne w zaawansowanych ludzkich nowotworach — duże obciążenie określonymi „sygnaturami” mutacyjnymi — nie były wyraźnie wzbogacone u szczurów-nosicieli, co wzmacnia ideę, że te cechy pojawiają się później, gdy gen zostaje całkowicie utracony.
Charakterystyczny odcisk, ale nie większy chaos
Gdy badacze wgłębili się w szczegółowe „sygnatury mutacyjne” opisujące, jak kumuluje się uszkodzenie DNA, znaleźli jedną godną uwagi różnicę. Szczególny wzorzec obejmujący sparowane zmiany nukleotydów, znany z dużych zasobów danych nowotworów ludzkich, ale jeszcze słabo poznany, pojawił się wyłącznie w guzach szczurów-nosicieli. Sugeruje to, że częściowa utrata BRCA1 może skierować komórki na specyficzny, subtelny sposób modyfikacji genomu, zamiast powodować prostą lawinę przypadkowych uszkodzeń. Jednocześnie ogólny poziom mutacji i dużych zmian liczby kopii DNA pozostał porównywalny między grupami, co przemawia przeciwko powszechnemu obrazowi, że nosiciele BRCA1 nieuchronnie przechodzą fazę gwałtownej niestabilności genetycznej mierzonej standardowym sekwencjonowaniem.
Mniej klasycznych „kierowców” w guzach nosicieli
Najbardziej nieoczekiwany wynik ujawnił się, gdy zespół skupił się na „mutacjach kierujących” — zmianach DNA w dobrze poznanych genach nowotworowych, uważanych za aktywnie popychające komórki w stronę złośliwości. W guzach związanych z promieniowaniem u szczurów normalnych takie mutacje kierujące występowały stosunkowo często. W przeciwieństwie do tego, guzy związane z promieniowaniem u szczurów-nosicieli Brca1 zawierały istotnie mniej tych rozpoznawanych mutacji kierujących, a w większej liczbie guzów nie znaleziono oczywistej mutacji kierującej w eksomie. Sugeruje to, że w kontekście częściowej utraty BRCA1 promieniowanie może sprzyjać rozwojowi raka piersi drogami, które nie pozostawiają silnego śladu w genach kodujących białka, takimi jak duże restrukturyzacje strukturalne, modyfikacje chemiczne DNA zmieniające aktywność genów lub długotrwałe zmiany w otaczającym środowisku tkankowym.
Co to oznacza dla zrozumienia ryzyka BRCA1
Dla czytelnika niebędącego specjalistą główne przesłanie jest zaskakujące, ale ważne: w tym modelu zwierzęcym posiadanie jednej uszkodzonej kopii BRCA1 nie powoduje po prostu większej liczby punktowych błędów w DNA w obrębie guzów. Zamiast tego wydaje się, że pozwala nowotworom piersi pojawiać się, omijając wiele klasycznych „awarii silnika” genetycznego zwykle widocznych w guzach. Autorzy proponują, że haploinsuficjencja BRCA1 może otwierać alternatywne drogi do nowotworu, prawdopodobnie obejmujące duże restrukturyzacje DNA, zmiany epigenetyczne lub modyfikacje w komórkach wspierających tkankę — procesy, których standardowe testy skoncentrowane na genach mogą nie wykryć. Zrozumienie tych ukrytych ścieżek będzie kluczowe dla projektowania lepszych strategii wczesnego wykrywania, bezpieczniejszego stosowania promieniowania i celowanej prewencji dla osób dziedziczących warianty BRCA1.
Cytowanie: Nakamura, Y., Daino, K., Ishikawa, A. et al. Mutational profiles of spontaneous and radiation-related mammary carcinomas in a rat model of Brca1 haploinsufficiency. Sci Rep 16, 10291 (2026). https://doi.org/10.1038/s41598-026-41240-9
Słowa kluczowe: BRCA1, ryzyko raka piersi, ekspozycja na promieniowanie, genetyka nowotworów, naprawa DNA