Clear Sky Science · tr
Celcomen: tek hücre ve doku perturbasyon modellemesi için uzamsal nedensel çözümleme
Canlı dokuları haritalamanın önemi
Vücudumuzdaki her organ, birbirleriyle sürekli iletişim halinde olan milyarlarca hücreden oluşur. Bu konuşmalar, genlerin açılıp kapanması yoluyla iletilir ve bir dokunun sağlıklı kalıp kalmayacağını, bir enfeksiyonla savaşacağını ya da kanserleşeceğini belirler. Yeni mikroskoplar artık hücrelerin doku içindeki konumlarını koruyarak binlerce genin aktivitesini okuyabiliyor. Ancak bu veri yığınını anlamlandırmak —ve bir geni ya da hücre tipini değiştirdiğimizde ne olacağını tahmin etmek— güçlü ve güvenilir matematiksel araçlar gerektirir. Bu çalışma, hücrelerin kendilerini ve komşularını uzayda nasıl etkilediğini çözmeye ve dokuların hastalık veya tedaviye nasıl yanıt vereceğini öngörmeye yönelik Celcomen adında böyle bir aracı tanıtıyor.
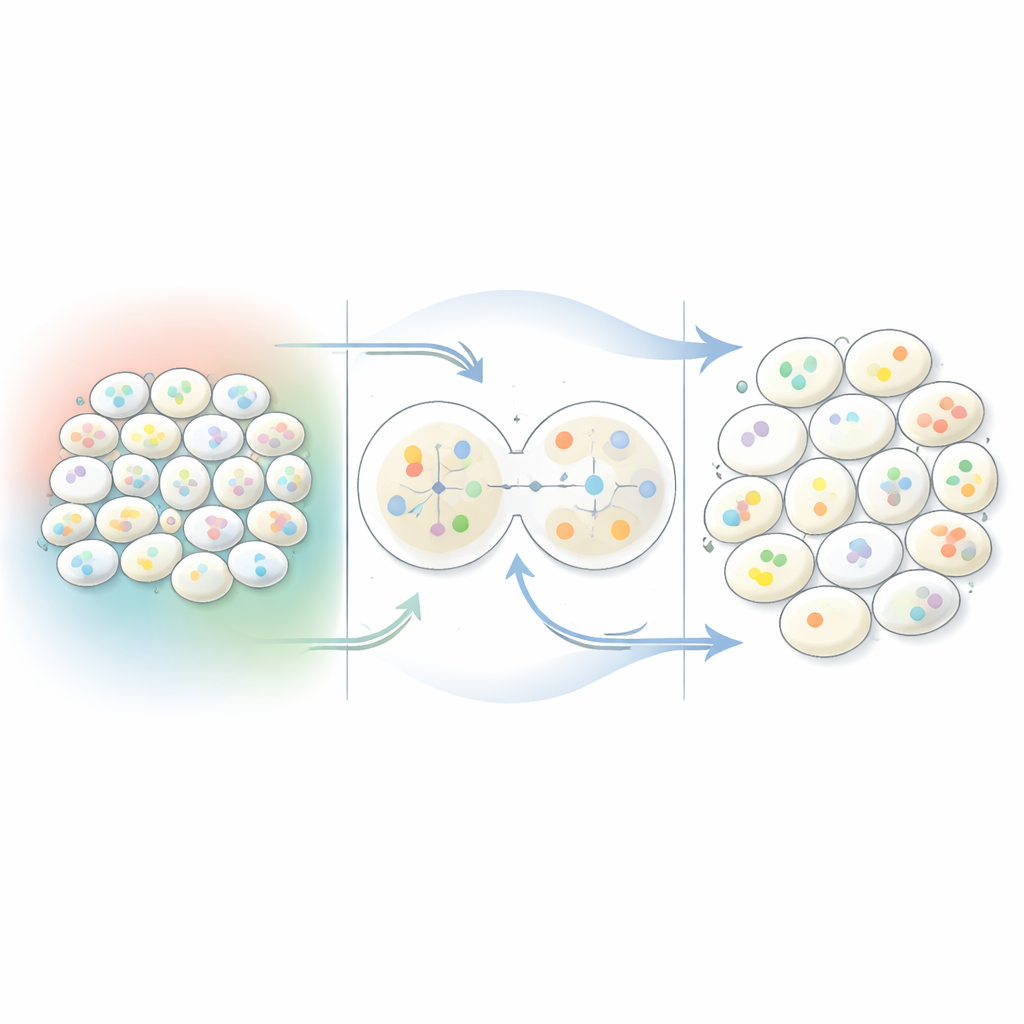
Bir hücreyi çevresinden ayırmak
Her hücrenin gen aktivitesi hem kendi içsel programını hem de çevresindeki hücrelerden aldığı sinyalleri yansıtır. Mevcut yöntemler sıklıkla bu iki etkiyi birbirine karıştırır veya hangi genlerin birbirleriyle konuştuğuna dair eksik ön bilgiyi varsayar. Celcomen farklı bir yol izliyor. Dokuyu, her hücrenin bir düğüm olduğu ve yakın hücrelerin bağlantılarla bağlandığı bir ağ olarak ele alıyor. Bu çerçevede, hücre içinde gerçekleşen etkileşimleri hücre sınırlarını aşan etkileşimlerden matematiksel olarak ayırıyor. Basitçe söylemek gerekirse, hangi gen değişikliklerinin hücrenin kendi iç devreleriyle açıklanabileceğini, hangilerinin komşulardan gelen mesajlara ihtiyaç duyduğunu soruyor.
Motorunun altında nedensellik ilhamlı bir yapı
Celcomen’in merkezinde, nedensel çıkarım ilkeleriyle sıkı sıkıya sınırlandırılmış bir grafik tabanlı sinir ağı bulunuyor. Sadece örüntüleri yakalayan bir “kara kutu” olmak yerine, model tanımlanabilirlik ilkesini karşılayacak şekilde inşa edilmiş: belirli bir veri seti için, onu açıklayan esas etkileşim yapısı pratikte tek bir en iyi yapı olmalı. Yazarlar hem matematiksel argümanlarla hem de bilgisayar simülasyonlarıyla Celcomen’in hücre içinde ve hücreler arasında işleyen gerçek gen–gen ağının temel iskeletini geri kazanabildiğini gösteriyor. Sistem önce veriden bir etkileşim haritası öğreniyor, ardından gerçekçi sentetik doku profilleri üreten ve belirli perturbasyonlar altında gen aktivitesi desenlerinin nasıl değişeceğini tahmin eden ikinci bir modül kullanıyor.
İnsan beyin kanserinde tahminleri test etmek
Celcomen’in gerçek biyolojiyi yakalayıp yakalamadığını görmek için ekip, agresif bir beyin tümörü olan insan glioblastomundan elde edilen yüksek çözünürlüklü uzamsal verilere uyguladı. Modele hangi genlerin salgılanan faktörleri veya içsel sinyal proteinlerini kodladığı söylenmeden, model otomatik olarak salgılanan, hücreden hücreye sinyalleşme genlerini dış etkileşim programlarına atadı ve birçok içsel sinyal genini hücre içi programlarla sınırladı. Ardından sanal bir deney yaptılar: tek bir tümör hücresinde interferon ilişkili genleri kapattılar. Celcomen, yalnızca bu hücre içindeki interferon yanıtının çökmesini değil, aynı zamanda yakın hücrelerde interferon tarafından yönlendirilen bağışıklık programlarının zayıflamasını da öngördü — bu, interferon sinyallerinin dokular aracılığıyla nasıl yayıldığı ve yerel bağışıklığı nasıl etkilediği bilgisini yansıtıyor.
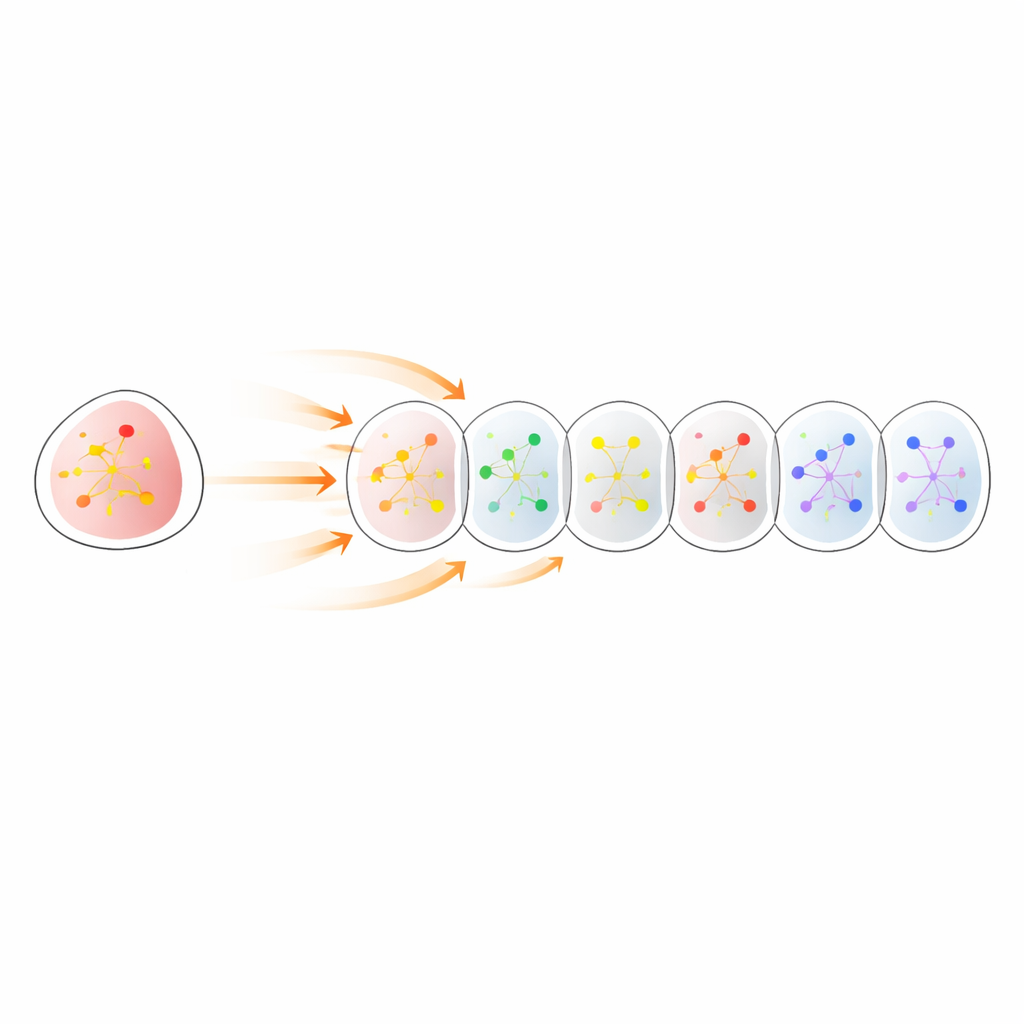
Sanal dokuları gerçek hayvan tümörleriyle karşılaştırmak
Sonraki adımda araştırmacılar, belirli genlerin tanımlı tümör bölgelerinde deneysel olarak ortadan kaldırıldığı bir fare akciğer kanseri modelinden gelen verilerle Celcomen’i zorladılar. Modeli yalnızca bozulmamış veya karışık lezyonlar üzerinde eğittiler, sonra seçilen bir genin belirli tümör noktalarında devre dışı bırakılması durumunda ne olacağını simüle etmesini istediler. Tahmin edilen gen aktivitesi kaymaları, bu genlerin gerçekten in vivo silindiği tümörlerden elde edilen gerçek ölçümlerle karşılaştırıldı. Birden çok lezyon ve gen genelinde, Celcomen’in öngörüleri gerçek değişikliklerle güçlü pozitif korelasyonlar gösterdi ve bu korelasyonlar şans beklentisinin çok üzerindeydi. Bu, modelin sanal deneylerinin biyolojik gerçeklikle yakından uyumlu olduğunu gösteriyor.
Gelecekteki tıp için anlamı
Celcomen, laboratuvar yerine bilgisayarda sorgulanabilen “sanal dokular” oluşturmanın bir yolunu sunuyor. Bir hücrenin davranışının ne kadarının kendi devresinden, ne kadarının çevresinden kaynaklandığını ayırt ederek ve kararlı, yorumlanabilir tahminler sağlayarak, yöntem bilim insanlarının kanser gibi hastalıkların yerel hücre topluluklarını nasıl bozduğunu ve hedefe yönelik tedavilerin bunları nasıl düzeltebileceğini keşfetmelerine yardımcı olabilir. Uzamsal ve tek hücreli teknolojiler daha yaygın ve ayrıntılı hale geldikçe, Celcomen gibi araçlar hangi deneylerin yapılacağını yönlendirebilir, hastalıklı dokulardaki beklenmedik zayıf noktaları vurgulayabilir ve nihayetinde yalnızca tek hücreleri değil, organlarımızı oluşturan karmaşık hücresel toplumları hedef alan tedavilerin tasarımını hızlandırabilir.
Atıf: Megas, S., Chen, D.G., Polanski, K. et al. Celcomen: spatial causal disentanglement for single-cell and tissue perturbation modeling. Nat Commun 17, 4126 (2026). https://doi.org/10.1038/s41467-026-69856-5
Anahtar kelimeler: uzamsal transkriptomik, hücre–hücre iletişimi, nedensel modelleme, kanser mikroçevresi, sanal dokular