Clear Sky Science · de
Celcomen: räumliche kausale Entflechtung für Einzelzell- und Gewebeperturbationsmodellierung
Warum die Kartierung lebender Gewebe wichtig ist
Jedes Organ in unserem Körper besteht aus Milliarden von Zellen, die ständig miteinander kommunizieren. Diese Unterhaltungen, vermittelt durch das Ein‑ und Ausschalten von Genen, entscheiden, ob ein Gewebe gesund bleibt, eine Infektion bekämpft oder krebsartig wird. Neue Mikroskope können inzwischen die Aktivität von Tausenden Genen in einzelnen Zellen erfassen und gleichzeitig ihre Lage im Gewebe bewahren. Aus dieser Datenmenge Sinn zu machen — und vorherzusagen, was passiert, wenn man ein Gen oder einen Zelltyp verändert — erfordert leistungsfähige und verlässliche mathematische Werkzeuge. Diese Studie stellt ein solches Werkzeug vor, genannt Celcomen, das entwickelt wurde, um zu entwirren, wie Zellen sich selbst und ihre Nachbarn im Raum beeinflussen, und um vorherzusagen, wie Gewebe auf Krankheit oder Therapie reagieren werden.
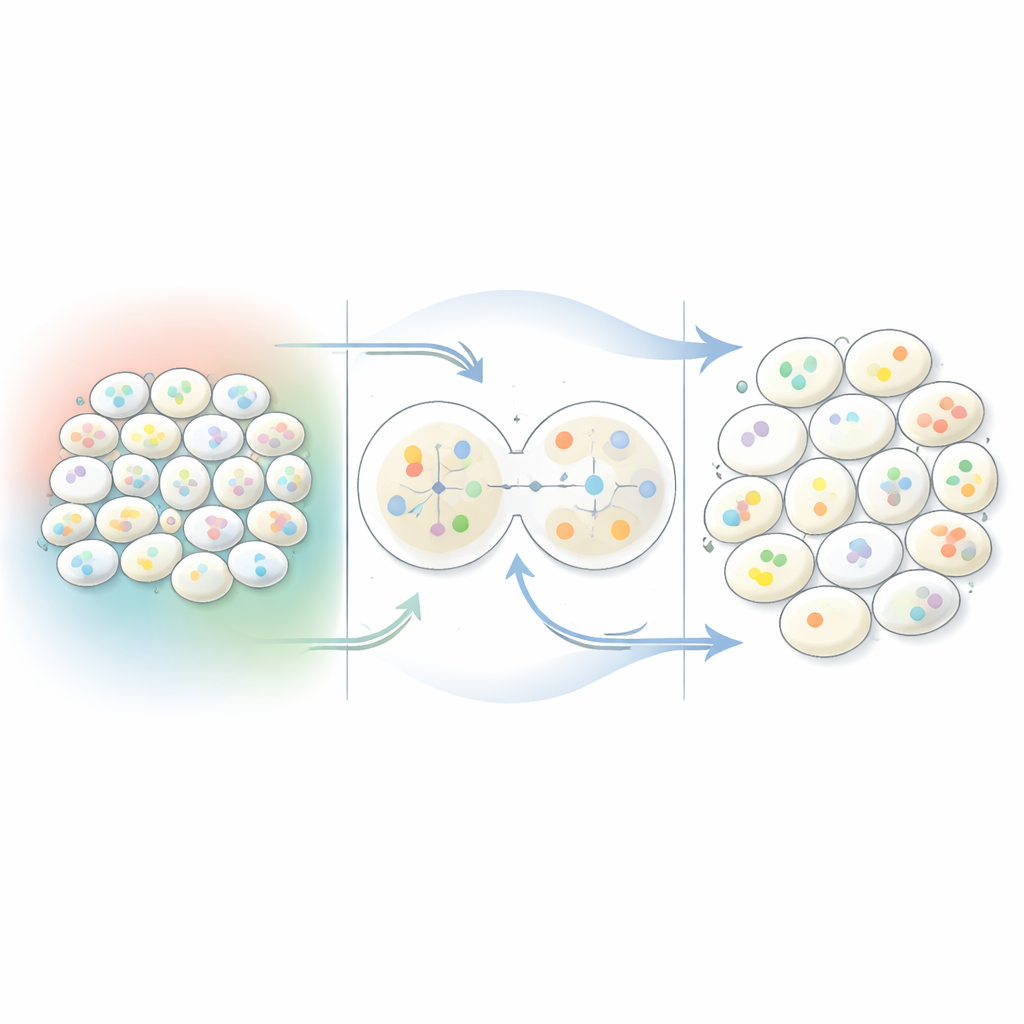
Eine Zelle von ihrer Nachbarschaft trennen
Die Genaktivität jeder Zelle spiegelt sowohl ihr eigenes internes Programm als auch die Signale wider, die sie von umgebenden Zellen erhält. Bestehende Methoden vermischen diese beiden Einflüsse oft oder sind abhängig von unvollständigem Vorwissen darüber, welche Gene miteinander kommunizieren. Celcomen geht einen anderen Weg. Es behandelt das Gewebe als Netzwerk, in dem jede Zelle ein Knoten ist und benachbarte Zellen durch Kanten verbunden sind. Innerhalb dieses Rahmens trennt es mathematisch Interaktionen, die innerhalb einer Zelle stattfinden, von denen, die Zellgrenzen überschreiten. Einfache Frageformuliert: Welche Genveränderungen lassen sich durch die interne Verdrahtung der Zelle erklären und welche erfordern Botschaften von Nachbarzellen?
Ein von Kausalitätsprinzipien geleiteter Motor unter der Haube
Im Kern von Celcomen arbeitet ein graphbasiertes neuronales Netz, das streng durch Prinzipien der kausalen Inferenz eingeschränkt ist. Anstatt eine „Black Box“ zu sein, die lediglich Muster anpasst, ist das Modell so aufgebaut, dass Identifizierbarkeit erfüllt wird: Für einen gegebenen Datensatz sollte es im Wesentlichen eine beste zugrundeliegende Interaktionsstruktur geben, die ihn erklärt. Die Autorinnen und Autoren zeigen sowohl mit mathematischen Argumenten als auch mit Computersimulationen, dass Celcomen das grundlegende Skelett des echten Gen‑Gen‑Netzwerks innerhalb und zwischen Zellen rekonstruieren kann. Das System lernt zuerst eine Interaktionskarte aus den Daten und nutzt dann ein zweites Modul, um realistische synthetische Gewebeprofile zu erzeugen und vorherzusagen, wie sich Genaktivitätsmuster unter spezifischen Perturbationen verändern würden.
Vorhersagen am Menschenhirntumor testen
Um zu prüfen, ob Celcomen reale Biologie erfasst, wendete das Team es auf hochauflösende räumliche Daten von menschlichem Glioblastom an, einem aggressiven Hirntumor. Ohne zu wissen, welche Gene für sekretierte Faktoren oder für interne Signalkomponenten codieren, ordnete das Modell automatisch sekretierte, zell‑zu‑zell Signalisierungsgene externen Interaktionsprogrammen zu und beschränkte viele interne Signalgene auf Programme innerhalb der Zelle. Anschließend führten sie ein virtuelles Experiment durch: das Abschalten interferon‑verwandter Gene in einer einzelnen Tumorzelle. Celcomen sagte nicht nur einen Zusammenbruch der Interferonantwort innerhalb dieser Zelle voraus, sondern auch eine Abschwächung interferongetriebener Immunprogramme in benachbarten Zellen — ein Spiegelbild dessen, wie Interferonsignale bekanntlich durch Gewebe verbreitet werden und die lokale Immunität beeinflussen.
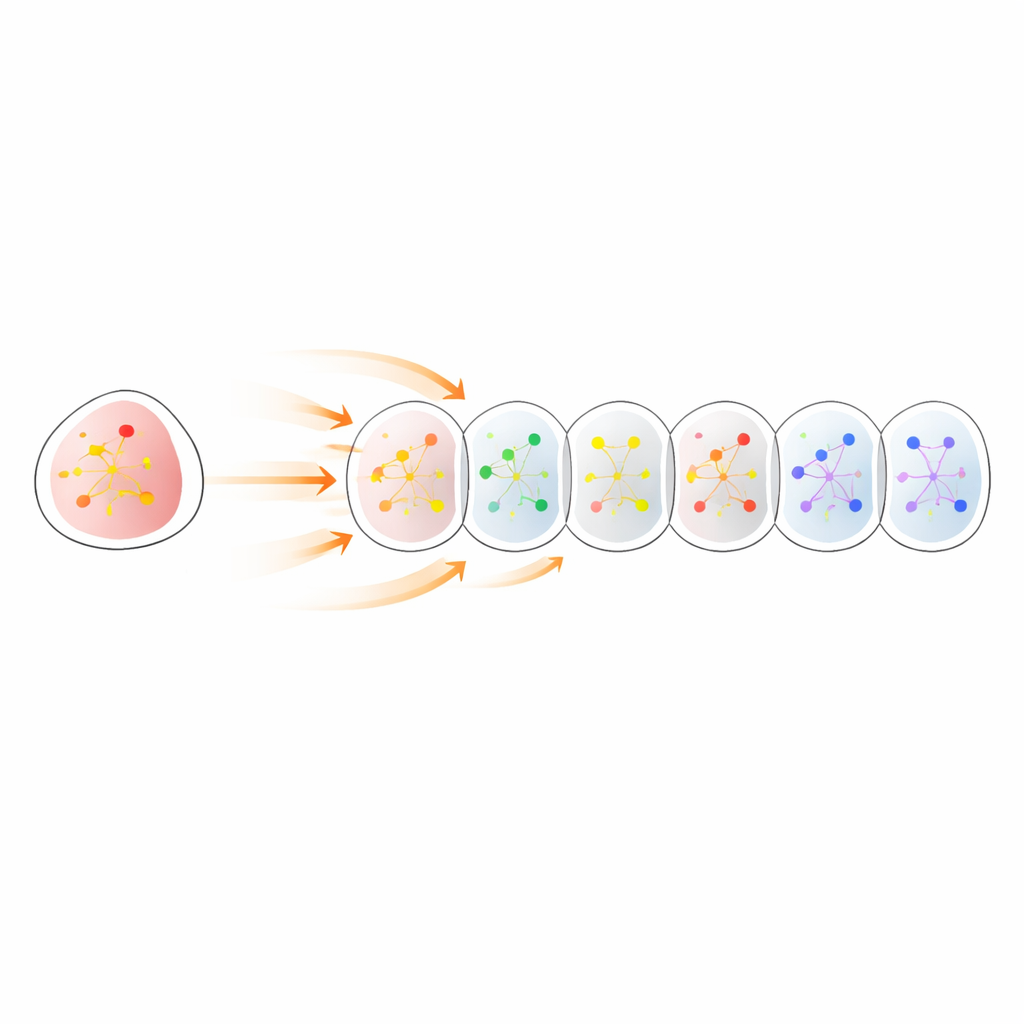
Virtuelle Gewebe mit echten Tier‑Tumoren abgleichen
Als Nächstes stellten die Forschenden Celcomen Daten aus einem Mausmodell von Lungenkrebs gegenüber, in dem spezifische Gene experimentell in definierten Tumorregionen ausgeschaltet worden waren. Sie trainierten das Modell nur an unveränderten oder gemischten Läsionen und baten es dann, zu simulieren, was passieren würde, wenn ein ausgewähltes Gen in bestimmten Tumorbereichen deaktiviert würde. Die vorhergesagten Verschiebungen der Genaktivität wurden mit realen Messungen aus Tumoren verglichen, in denen diese Gene tatsächlich in vivo gelöscht worden waren. Über mehrere Läsionen und Gene hinweg zeigten Celcomens Prognosen starke positive Korrelationen mit den tatsächlichen Veränderungen, und diese Korrelationen waren deutlich stärker, als man zufällig erwarten würde. Das legt nahe, dass die virtuellen Experimente des Modells eng mit biologischer Realität übereinstimmen.
Was das für zukünftige Medizin bedeutet
Celcomen bietet eine Möglichkeit, „virtuelle Gewebe“ zu erstellen, die am Computer statt im Labor untersucht werden können. Indem es unterscheidet, wie viel vom Verhalten einer Zelle aus ihrer eigenen Verdrahtung versus ihrer Nachbarschaft stammt, und indem es stabile, interpretierbare Vorhersagen liefert, kann die Methode Forschenden helfen zu erforschen, wie Krankheiten wie Krebs lokale Zellgemeinschaften stören und wie gezielte Therapien sie wiederherstellen könnten. Mit der zunehmenden Verbreitung und Detaillierung räumlicher und einzelzelliger Technologien könnten Werkzeuge wie Celcomen dabei helfen, zu entscheiden, welche Experimente durchgeführt werden sollten, unerwartete Schwachstellen in kranken Geweben aufzuzeigen und letztlich die Entwicklung von Behandlungen zu beschleunigen, die nicht nur auf einzelne Zellen, sondern auf die komplexen zellulären Gesellschaften unserer Organe abzielen.
Zitation: Megas, S., Chen, D.G., Polanski, K. et al. Celcomen: spatial causal disentanglement for single-cell and tissue perturbation modeling. Nat Commun 17, 4126 (2026). https://doi.org/10.1038/s41467-026-69856-5
Schlüsselwörter: räumliche Transkriptomik, Zell‑zu‑Zell‑Kommunikation, kausales Modellieren, Krebs‑Mikroumgebung, virtuelle Gewebe