Clear Sky Science · fr
Celcomen : démêler les causes spatiales pour modéliser les perturbations au niveau des cellules uniques et des tissus
Pourquoi cartographier les tissus vivants importe
Chaque organe de notre corps est construit à partir de milliards de cellules qui dialoguent en permanence. Ces échanges, portés par l’activation et la désactivation de gènes, déterminent si un tissu reste sain, combat une infection ou devient cancéreux. De nouveaux microscopes peuvent désormais lire l’activité de milliers de gènes dans des cellules individuelles tout en conservant leur position dans le tissu. Mais interpréter cette masse de données — et prévoir ce qui se passerait si l’on modifiait un gène ou un type cellulaire — exige des outils mathématiques puissants et fiables. Cette étude présente un tel outil, nommé Celcomen, conçu pour démêler comment les cellules influencent elles‑mêmes et leurs voisines dans l’espace, et pour anticiper la réponse des tissus aux maladies ou aux traitements.
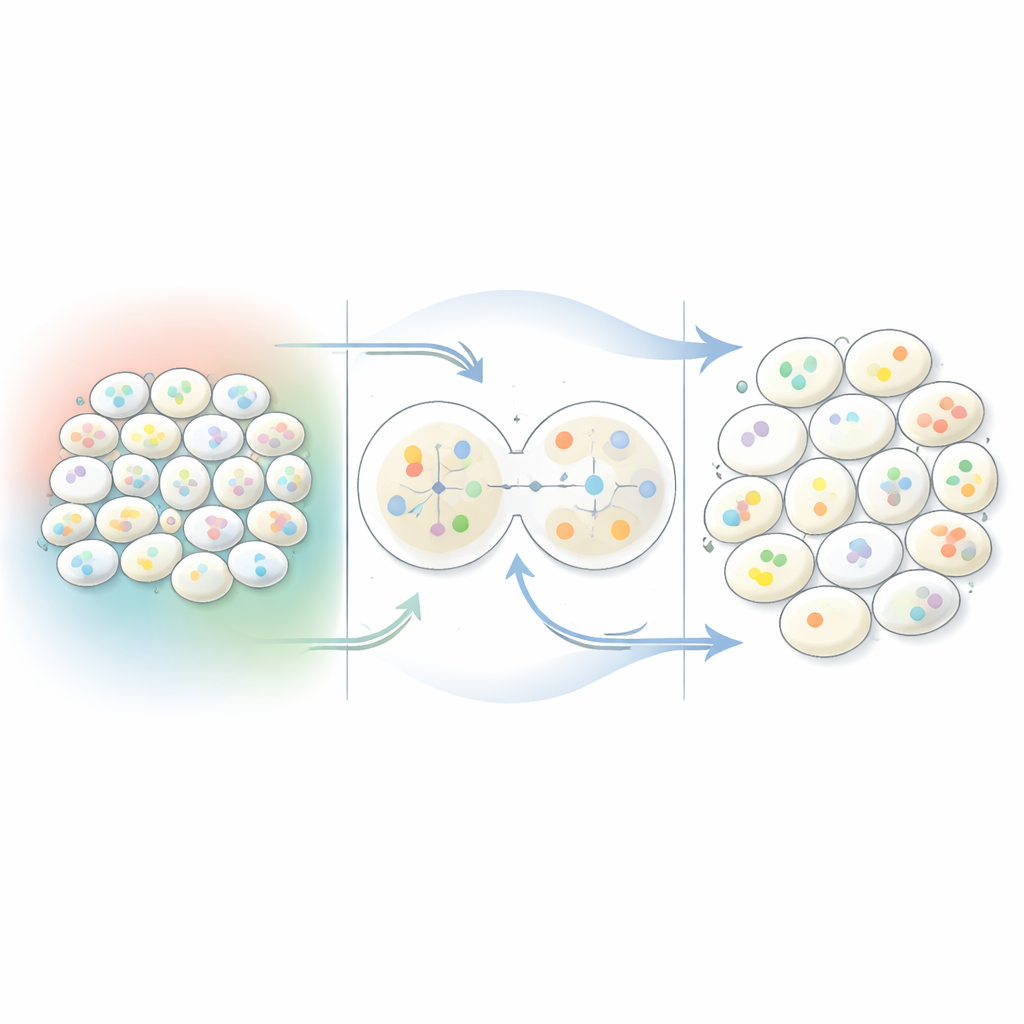
Séparer la cellule de son voisinage
L’activité génique d’une cellule reflète à la fois son programme interne et les signaux qu’elle reçoit des cellules environnantes. Les méthodes existantes mêlent souvent ces deux influences ou reposent sur des connaissances a priori incomplètes sur les interactions géniques. Celcomen emprunte une voie différente. Il considère le tissu comme un réseau où chaque cellule est un nœud et les cellules proches sont reliées par des liens. Dans ce cadre, il sépare mathématiquement les interactions qui se déroulent à l’intérieur d’une cellule de celles qui franchissent les frontières cellulaires. Concrètement, il pose la question : quels changements géniques s’expliquent par le câblage interne de la cellule, et lesquels nécessitent des messages provenant des voisines ?
Un moteur inspiré par la causalité sous le capot
Le cœur de Celcomen est un réseau neuronal basé sur des graphes, fortement contraint par des principes de l’inférence causale. Plutôt que d’être une « boîte noire » qui se contente d’ajuster des motifs, le modèle est construit pour satisfaire l’identifiabilité : pour un jeu de données donné, il doit exister essentiellement une seule structure d’interaction sous‑jacente qui l’explique. Les auteurs montrent, par des arguments mathématiques et des simulations informatiques, que Celcomen peut retrouver le squelette de base du véritable réseau gène–gène opérant intra‑ et inter‑cellulaire. Le système apprend d’abord une carte d’interaction à partir des données puis utilise un second module pour générer des profils de tissus synthétiques réalistes et prédire comment les motifs d’activité génique évolueraient sous des perturbations spécifiques.
Tester les prédictions dans le cancer cérébral humain
Pour vérifier si Celcomen capture la biologie réelle, l’équipe l’a appliqué à des données spatiales haute résolution de glioblastomes humains, des tumeurs cérébrales agressives. Sans indiquer au modèle quels gènes codent des facteurs sécrétés ou des protéines de signalisation internes, celui‑ci a automatiquement assigné les gènes de signalisation sécrétés et intercellulaires aux programmes d’interaction externes et cantonné de nombreux gènes de signalisation internes à des programmes intra‑cellulaires. Ils ont ensuite réalisé une expérience virtuelle : éteindre des gènes liés à l’interféron dans une seule cellule tumorale. Celcomen a prédit non seulement un effondrement de la réponse à l’interféron au sein de cette cellule, mais aussi un affaiblissement des programmes immunitaires pilotés par l’interféron dans les cellules voisines — reflétant la manière dont les signaux d’interféron se propagent dans les tissus et influencent l’immunité locale.
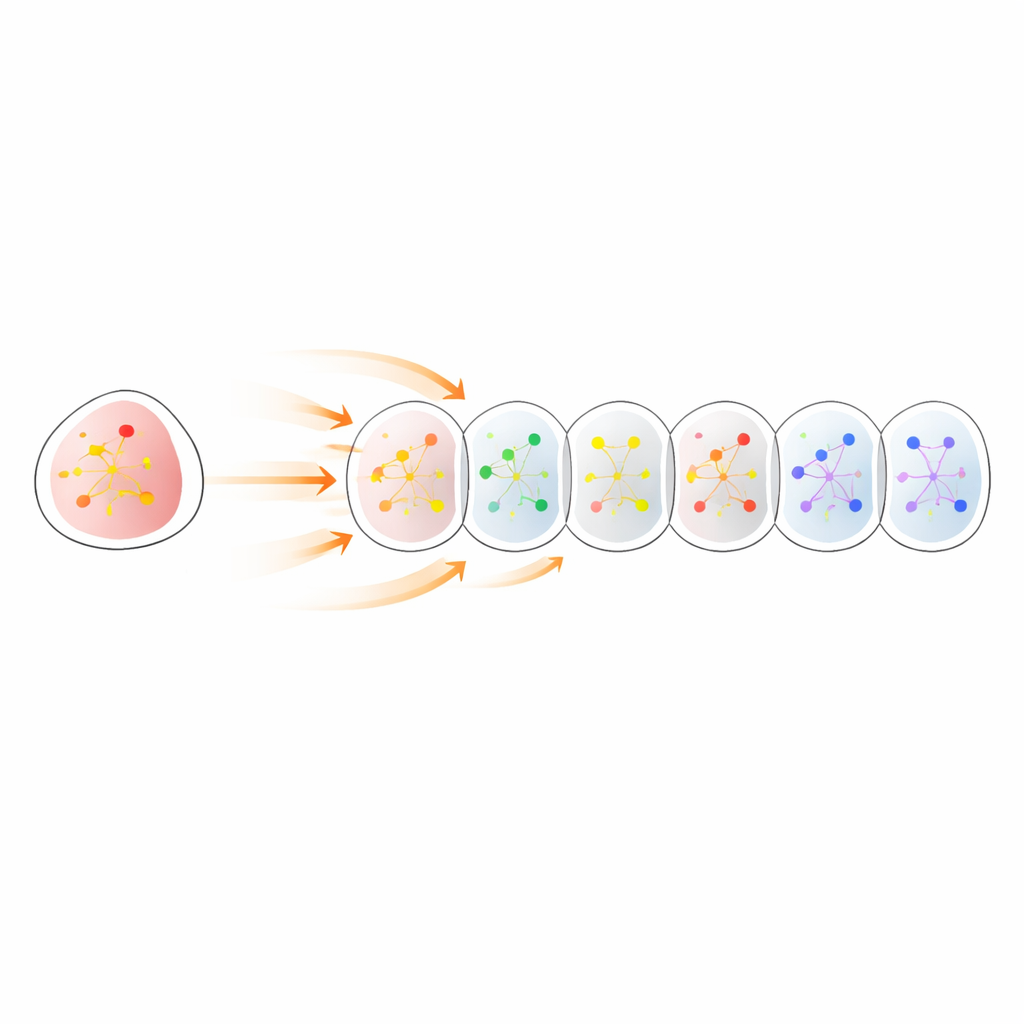
Comparer les tissus virtuels aux tumeurs animales réelles
Ensuite, les chercheurs ont mis Celcomen au défi avec des données d’un modèle murin de cancer du poumon où certains gènes avaient été éliminés expérimentalement dans des régions tumorales définies. Ils ont entraîné le modèle uniquement sur des lésions non perturbées ou mixtes, puis lui ont demandé de simuler ce qui se produirait si un gène choisi était désactivé dans des zones tumorales particulières. Les variations d’activité génique prédites ont été comparées aux mesures réelles provenant de tumeurs où ces gènes avaient effectivement été supprimés in vivo. À travers plusieurs lésions et gènes, les prévisions de Celcomen ont montré de fortes corrélations positives avec les changements observés, et ces corrélations étaient bien plus élevées que ce que l’on attendrait par hasard. Cela suggère que les expériences virtuelles du modèle sont étroitement alignées avec la réalité biologique.
Ce que cela signifie pour la médecine de demain
Celcomen offre un moyen de construire des « tissus virtuels » que l’on peut sonder sur un ordinateur plutôt qu’au laboratoire. En distinguant quelle part du comportement d’une cellule provient de son câblage interne versus son voisinage, et en fournissant des prédictions stables et interprétables, la méthode peut aider les scientifiques à explorer comment des maladies comme le cancer perturbent les communautés cellulaires locales et comment des thérapies ciblées pourraient les restaurer. À mesure que les technologies spatiales et unicellulaires se répandent et gagnent en résolution, des outils comme Celcomen pourraient orienter les expériences à mener, mettre en lumière des points faibles inattendus dans les tissus malades et, ultimement, accélérer la conception de traitements qui agissent non seulement sur des cellules isolées, mais sur les sociétés cellulaires complexes qui forment nos organes.
Citation: Megas, S., Chen, D.G., Polanski, K. et al. Celcomen: spatial causal disentanglement for single-cell and tissue perturbation modeling. Nat Commun 17, 4126 (2026). https://doi.org/10.1038/s41467-026-69856-5
Mots-clés: transcriptomique spatiale, communication cellule–cellule, modélisation causale, microenvironnement tumoral, tissus virtuels