Clear Sky Science · sv
NOX1/4 driver lever lever hepatisk järn- och lipiddysreglering, redoxobalans och inflammation hos etanolmatade möss
Varför denna forskning betyder något för personer som dricker
Tungt drickande är känt för att skada levern, men varför vissa går från enkel fettansamling till allvarlig sjukdom håller fortfarande på att klarläggas. Denna studie granskar ett par enzymatiska ”tändstift” i leverceller som bidrar till bildning av skadliga oxidativa molekyler och visar att blockering av dem med ett experimentellt läkemedel kan dämpa flera skadliga processer samtidigt hos alkoholexponerade möss. Arbetet antyder en möjlig framtida tablett som skulle kunna skydda levern genom att samtidigt lätta på järnöverskott, fettansamling och inflammation, istället för att angripa varje problem separat.
En närmare titt på alkoholens dolda leverskador
Alkoholrelaterad leversjukdom omfattar ett spektrum från fettlever till skrumplever och levercancer. Författarna fokuserar på fyra tätt sammankopplade skadefaktorer: överskott av järn lagrat i levern, ansamling av fettk droplets, kemisk stress orsakad av reaktiva syreföreningar och kronisk inflammation driven av immunceller. Hos personer som dricker mycket försvagar alkohol tarmbarriären och förändrar tarmfloran, vilket gör att bakterieprodukter når levern och eldar på inflammationen. Samtidigt ger alkoholmetabolism i levern upphov till reaktiva molekyler som skadar celler och kan utlösa en form av järn‑driven celldöd kallad ferroptos. Tillsammans skapar dessa processer en ond cirkel som påskyndar leverskadan.
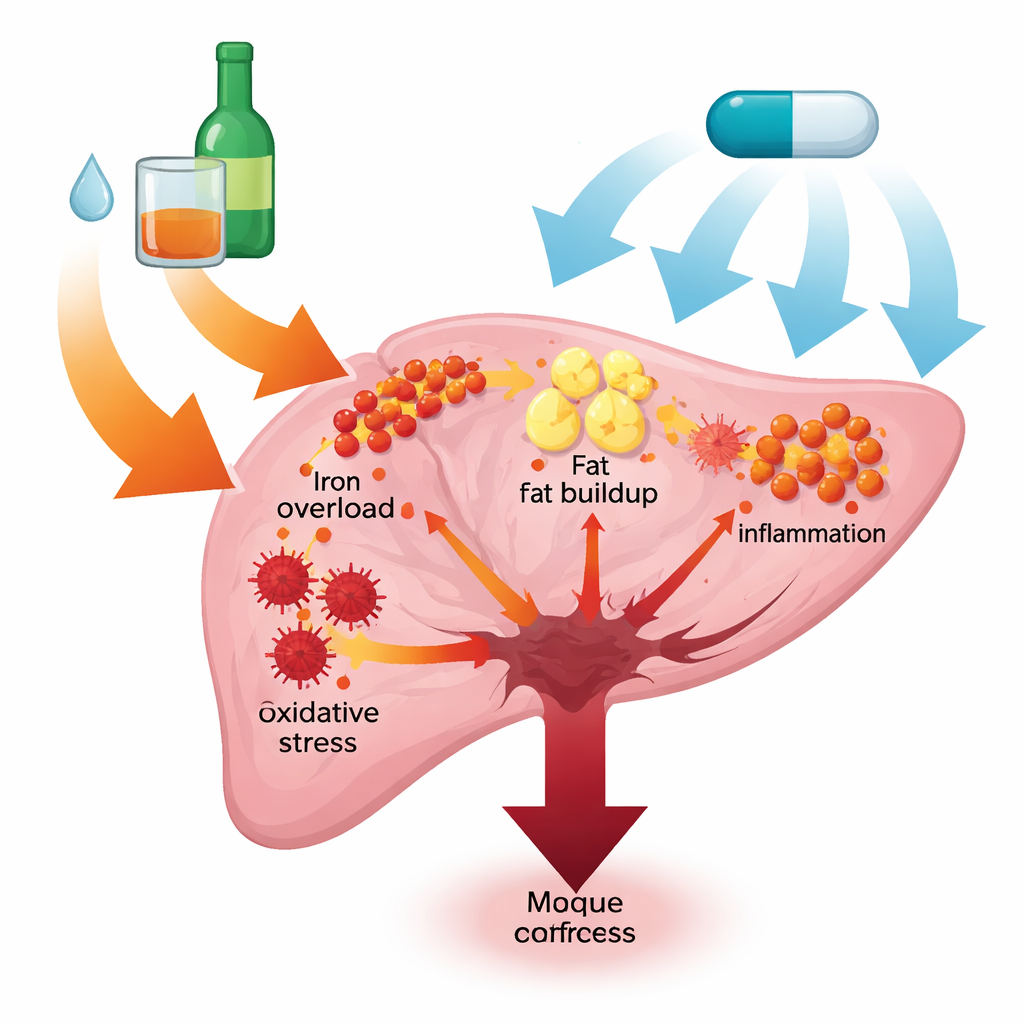
Enzymparet som tänder elden
Studien zoomar in på två närbesläktade enzymer, NOX1 och NOX4, som sitter i cellmembran och producerar reaktiva syreradikaler. Med hjälp av en standardmodell med kronisk plus binge‑alkohol hos möss fann forskarna att alkohol kraftigt ökade både gen‑ och proteinuttrycket av NOX1 och NOX4 i levern. Denna ökning följdes av klassiska tecken på leverskada: förhöjda nivåer av leverenzymer i blodet, svullna och döende leverceller vid mikroskopi samt tydliga tecken på järnansamling och fettavlagringar i levervävnad. Resultaten tyder på att NOX1/4 fungerar som upstream‑antändare som kopplar alkoholexponering till omfattande metaboliska och inflammatoriska skador.
Hur blockering av NOX1/4 kyler ner järn, fett och stress
Forskargruppen testade Setanaxib, ett läkemedel under klinisk utveckling som selektivt hämmar NOX1 och NOX4. Möss som fick Setanaxib tillsammans med alkohol uppvisade mycket mindre leverskada än möss som enbart fick alkohol. Järnmätningar visade att läkemedlet reducerade både järn i tvåvärd och trevärd form i levern och minskade området med järnfärgning, samtidigt som ett nyckelprotein för järnlagring sjönk. På molekylär nivå verkade Setanaxib återställa järntrafiken: det minskade nivåerna av hepcidin, ett hormon som fångar järn i vävnader, återställde järnexportören ferroportin och sänkte nivåerna av transferrinreceptor 1, som tar in järn i celler. Parallellt visade oljefärgade snitt och blodprover att Setanaxib sänkte triglycerider och fria fettsyror i lever och blod, vilket indikerar minskad alkoholinducerad fettbelastning.
Återuppbyggnad av leverns försvar och dämpning av inflammation
Utöver effekter på järn och fett hjälpte Setanaxib till att reparera leverns antioxidativa skydd. Alkohol ensam tömde på glutation, cellens huvudsakliga skyddsmolekyl, ökade dess oxiderade form och höjde markörer för lipidperoxidation. Alkohol hämmande också aktiviteten hos Nrf2, en huvudregulator som slår på antioxidativa gener, vilket ledde till lägre nivåer av skyddande proteiner som HO‑1, SLC7A11 och GPX4, samtidigt som en stressmarkör kallad Prx2 ökade. Setanaxib reverserade dessa förändringar, återställde glutationbalansen och Nrf2‑signalering och sänkte markörer för oxidativ skada. Läkemedlet dämpade också den inflammatoriska responsen: det minskade nivåerna av kemotaktiska MCP‑1, reducerade antalet infiltrerande makrofager i levervävnad och sänkte både lever‑ och blodnivåerna av de proinflammatoriska budbärarna IL‑1β och IL‑6.
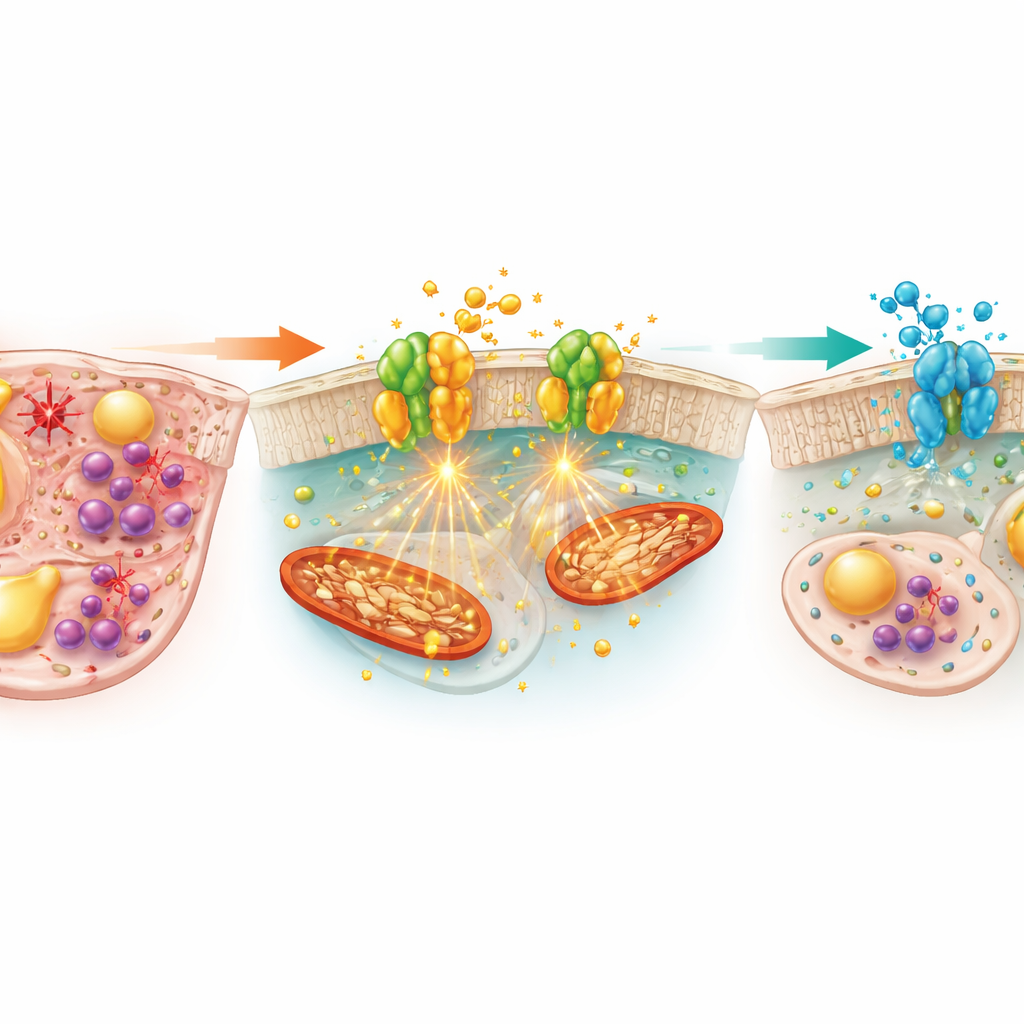
Vad detta kan innebära för framtida behandlingar
Tillsammans tyder fynden på att NOX1 och NOX4 sitter vid en central korsning i alkoholinducerad leverskada, där överskott av järn, fettansamling, oxidativ stress och inflammation kopplas samman. Genom att hämma detta enzympar kunde Setanaxib dämpa alla fyra processer samtidigt hos etanolmatade möss och erbjuda ett bredare skydd än strategier som enbart fyller på antioxidanter eller endast riktar sig mot inflammation. Eftersom arbetet är utfört i djur återstår viktiga frågor om långtidssäkerhet, dosering och effekter hos människor, men studien ger ett starkt skäl för att pröva NOX1/4‑hämmare som multidimensionell behandling för alkoholrelaterad leversjukdom, särskilt hos patienter med tecken på järnöverskott och oxidativ stress.
Citering: Yu, L., He, T., Zhang, P. et al. NOX1/4 drives hepatic iron and lipid dysregulation, redox imbalance, and inflammation in ethanol-fed mice. Sci Rep 16, 12283 (2026). https://doi.org/10.1038/s41598-026-42716-4
Nyckelord: alkoholrelaterad leversjukdom, oxidativ stress, järnöverskott, leverinflammation, Setanaxib