Clear Sky Science · it
NOX1/4 guida la disregolazione del ferro e dei lipidi epatici, lo squilibrio redox e l’infiammazione in topi alimentati con etanolo
Perché questa ricerca è importante per chi consuma alcol
Il consumo eccessivo di alcol è noto per danneggiare il fegato, ma i motivi per cui alcune persone passano da un semplice accumulo di grasso a una malattia grave sono ancora oggetto di studio. Questo lavoro esamina da vicino una coppia di “accenditori” enzimatici nelle cellule epatiche che contribuiscono a generare ossidanti dannosi e mostra che bloccarli con un farmaco sperimentale può attenuare contemporaneamente diversi processi lesivi in topi esposti all’alcol. Lo studio suggerisce la possibilità, in futuro, di una pillola che protegga il fegato riducendo insieme il sovraccarico di ferro, l’accumulo di grasso e l’infiammazione, anziché affrontare ciascun problema separatamente.
Uno sguardo più approfondito ai danni epatici nascosti dell’alcol
La malattia epatica alcolica comprende uno spettro che va dal fegato grasso alla cirrosi e al cancro epatico. Gli autori si concentrano su quattro fattori strettamente correlati: l’eccesso di ferro immagazzinato nel fegato, l’accumulo di goccioline lipidiche, lo stress chimico dovuto alle specie reattive dell’ossigeno e l’infiammazione cronica guidata dalle cellule immunitarie. Nelle persone che bevono molto, l’alcol indebolisce la barriera intestinale e altera il microbiota, consentendo ai prodotti batterici di raggiungere il fegato e alimentare l’infiammazione. Allo stesso tempo, il metabolismo dell’alcol nel fegato produce molecole reattive che danneggiano le cellule e possono innescare una forma di morte cellulare guidata dal ferro chiamata ferroptosi. Questi processi insieme creano un circolo vizioso che accelera il danno epatico.
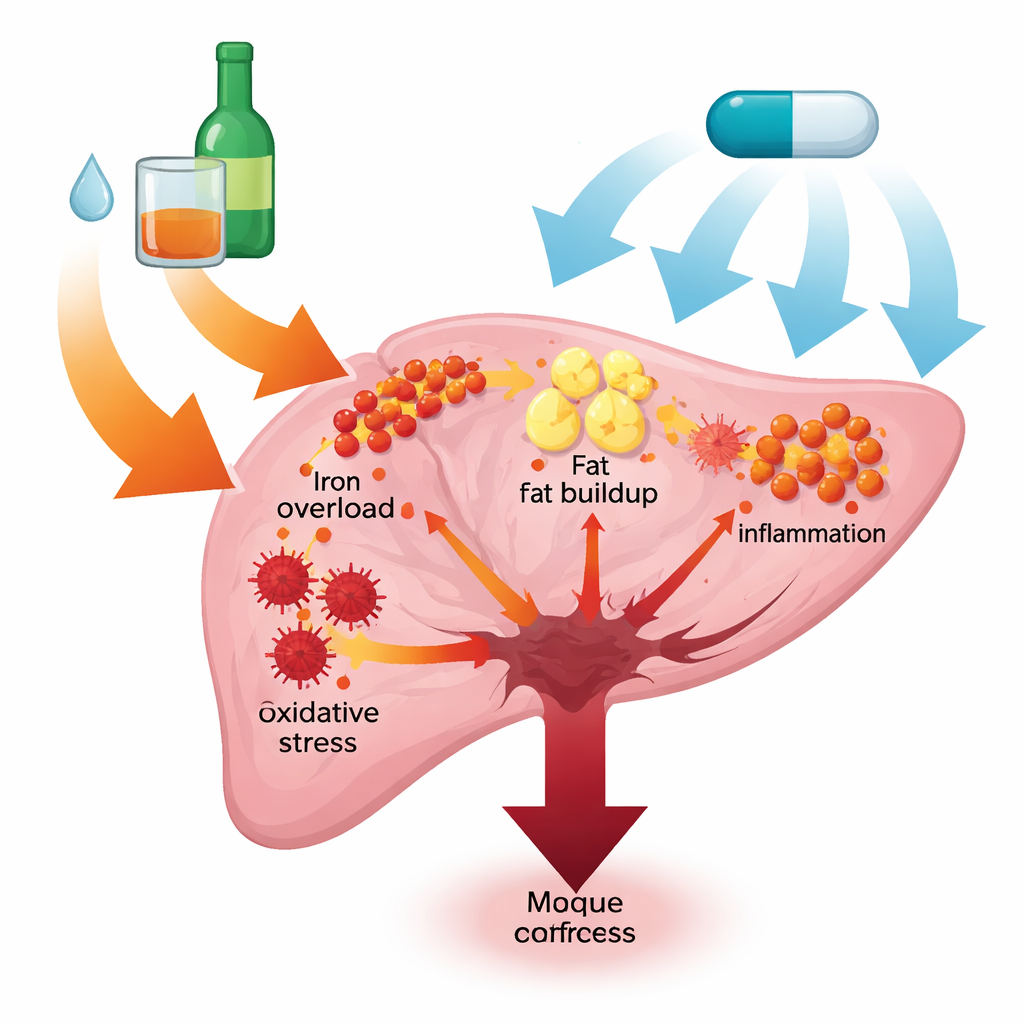
La coppia enzimatica che accende l’incendio
Lo studio si concentra su due enzimi correlati, NOX1 e NOX4, che si trovano nelle membrane cellulari e producono specie reattive dell’ossigeno. Utilizzando un modello murino standard di esposizione cronica più binge di alcol, i ricercatori hanno osservato che l’alcol aumentava marcatamente sia i livelli genici sia quelli proteici di NOX1 e NOX4 nel fegato. Questo incremento era accompagnato da segni classici di danno epatico: livelli ematici più elevati di enzimi epatici, cellule epatiche rigonfie e morenti al microscopio, e chiari indizi di accumulo di ferro e depositi di grasso nel tessuto epatico. Questi risultati suggeriscono che NOX1/4 agiscono come inneschi a monte che collegano l’esposizione all’alcol a diffuse alterazioni metaboliche e infiammatorie.
Come il blocco di NOX1/4 placa ferro, grasso e stress
Il team ha testato Setanaxib, un farmaco in sviluppo clinico che blocca selettivamente NOX1 e NOX4. I topi trattati con Setanaxib insieme all’alcol hanno mostrato un danno epatico molto minore rispetto agli animali esposti solo all’alcol. Le misurazioni del ferro hanno rivelato che il farmaco ha ridotto sia il ferro ferroso sia il ferrico nel fegato e ha diminuito l’area di colorazione del ferro, riducendo al contempo una proteina chiave di stoccaggio del ferro. A livello molecolare, Setanaxib sembra aver riequilibrato il traffico del ferro: ha ridotto i livelli di epcidina, un ormone che intrappola il ferro nei tessuti, ha ripristinato la proteina esportatrice del ferro ferroportina e ha abbassato i livelli del recettore della transferrina 1, che porta il ferro nelle cellule. Parallelamente, sezioni colorate con olio e analisi del sangue hanno mostrato che Setanaxib ha ridotto trigliceridi epatici e plasmatici e acidi grassi liberi, indicando un sollievo dall’accumulo lipidico indotto dall’alcol.
Ripristinare le difese epatiche e calmare l’infiammazione
Oltre al ferro e ai lipidi, Setanaxib ha contribuito a riparare lo scudo antiossidante del fegato. L’alcol da solo esauriva il glutatione, la principale molecola protettiva cellulare, aumentava la sua forma ossidata e innalzava i marcatori della perossidazione lipidica. Inibiva anche l’attività di Nrf2, un interruttore maestro che attiva i geni antiossidanti, portando a livelli ridotti di proteine protettive come HO-1, SLC7A11 e GPX4, mentre aumentava un marcatore di stress chiamato Prx2. Setanaxib ha invertito questi cambiamenti, ripristinando l’equilibrio del glutatione e la segnalazione di Nrf2 e riducendo i marcatori di danno ossidativo. Il farmaco ha inoltre attenuato la risposta infiammatoria: ha ridotto i livelli del chemoattrattante MCP-1, diminuito il numero di macrofagi infiltranti nel tessuto epatico e abbassato sia nel fegato sia nel sangue i livelli dei messaggeri pro‑infiammatori IL‑1β e IL‑6.
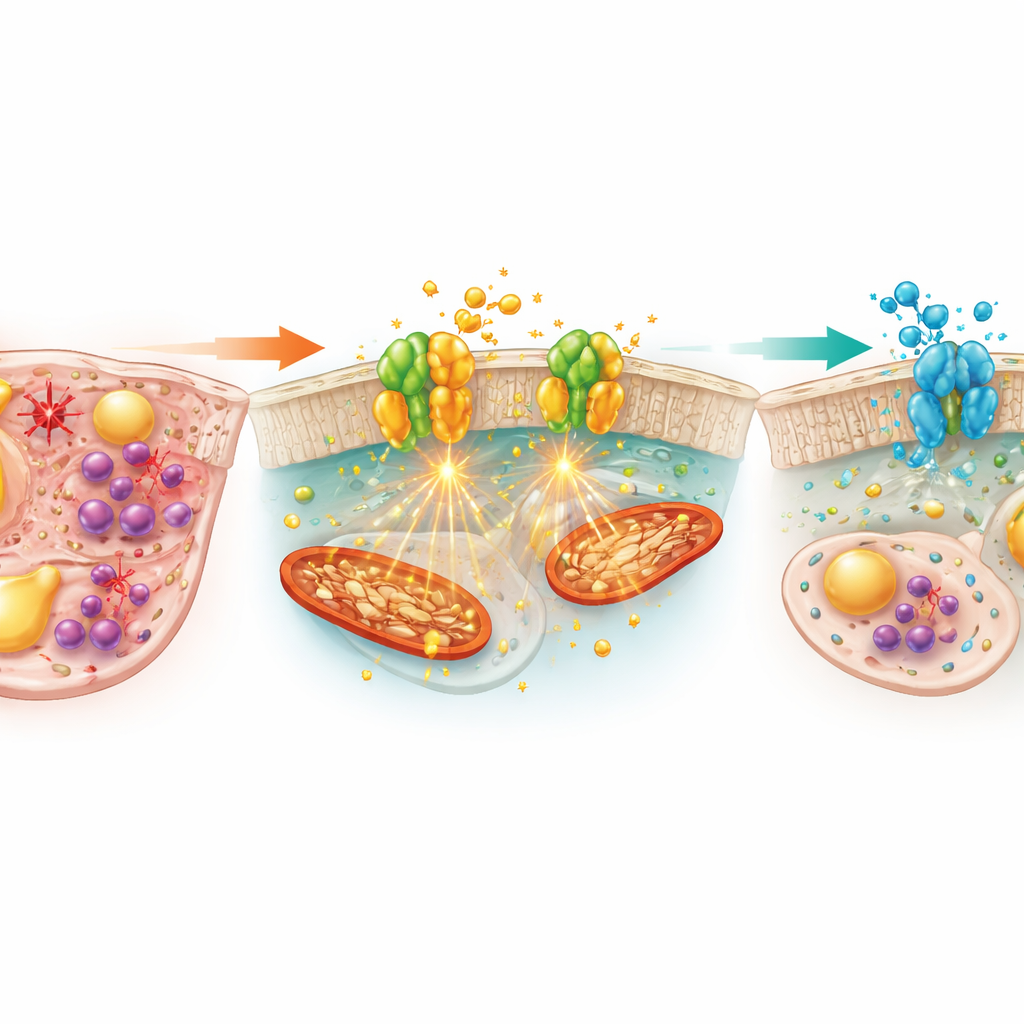
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, i risultati suggeriscono che NOX1 e NOX4 occupano un crocevia centrale del danno epatico indotto dall’alcol, collegando eccesso di ferro, accumulo di grasso, stress ossidativo e infiammazione. Bloccando questa coppia enzimatica, Setanaxib è stato in grado di attenuare simultaneamente tutti e quattro i processi nei topi alimentati con etanolo, offrendo una protezione più ampia rispetto a strategie che si limitano a integrare antiossidanti o a mirare solo all’infiammazione. Pur essendo studi condotti su animali e restando domande importanti sulla sicurezza a lungo termine, il dosaggio e gli effetti nell’uomo, lo studio fornisce una solida motivazione per testare gli inibitori di NOX1/4 come trattamenti multidimensionali per la malattia epatica alcolica, specialmente nei pazienti che mostrano segni di sovraccarico di ferro e stress ossidativo.
Citazione: Yu, L., He, T., Zhang, P. et al. NOX1/4 drives hepatic iron and lipid dysregulation, redox imbalance, and inflammation in ethanol-fed mice. Sci Rep 16, 12283 (2026). https://doi.org/10.1038/s41598-026-42716-4
Parole chiave: malattia epatica alcolica, stress ossidativo, sovraccarico di ferro, infiammazione epatica, Setanaxib