Clear Sky Science · fr
NOX1/4 entraîne une dysrégulation hépatique du fer et des lipides, un déséquilibre redox et une inflammation chez la souris exposée à l’éthanol
Pourquoi cette recherche compte pour les personnes qui boivent
La consommation excessive d’alcool est connue pour endommager le foie, mais les raisons pour lesquelles certaines personnes évoluent d’une simple accumulation de graisses vers une maladie grave restent partiellement élucidées. Cette étude examine de près une paire d’« allumeurs » enzymatiques dans les cellules hépatiques qui contribuent à générer des oxydants nocifs et montre que leur blocage par un médicament expérimental peut apaiser plusieurs processus délétères à la fois chez des souris exposées à l’alcool. Ces travaux laissent entrevoir à terme une pilule capable de protéger le foie en atténuant simultanément la surcharge en fer, l’accumulation lipidique et l’inflammation, plutôt que de traiter chaque problème séparément.
Un regard approfondi sur les dommages hépatiques cachés de l’alcool
La maladie hépatique alcoolique couvre un spectre allant du foie gras à la cirrhose et au cancer du foie. Les auteurs se concentrent sur quatre facteurs étroitement liés : l’excès de fer stocké dans le foie, l’accumulation de gouttelettes graisseuses, le stress chimique causé par les espèces réactives de l’oxygène, et l’inflammation chronique menée par les cellules immunitaires. Chez les gros buveurs, l’alcool fragilise la barrière intestinale et modifie le microbiote, permettant à des produits bactériens d’atteindre le foie et d’attiser l’inflammation. Parallèlement, le métabolisme de l’alcool dans le foie produit des molécules réactives qui blessent les cellules et peuvent déclencher une forme de mort cellulaire dépendante du fer appelée ferroptose. Ensemble, ces processus créent un cercle vicieux qui accélère la lésion hépatique.
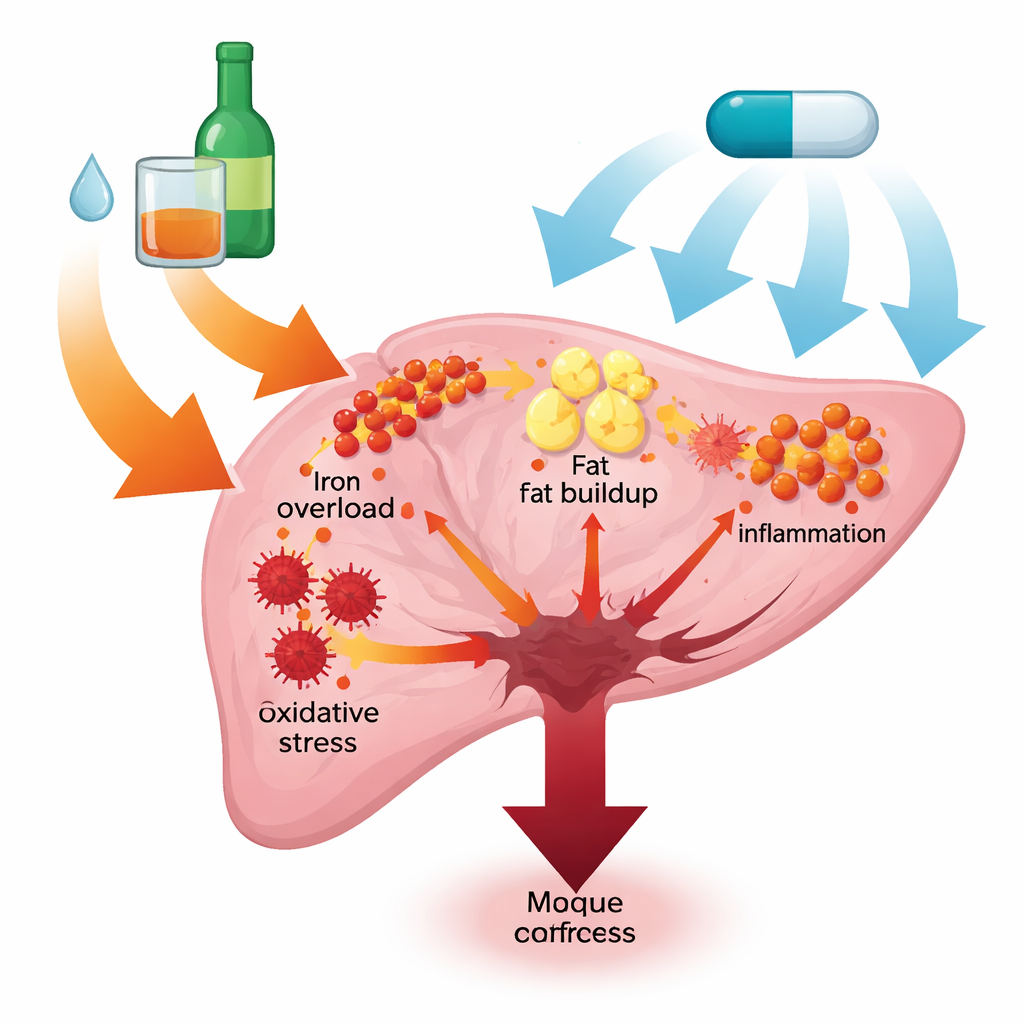
La paire d’enzymes qui met le feu
L’étude met en lumière deux enzymes apparentées, NOX1 et NOX4, qui se situent dans les membranes cellulaires et produisent des espèces réactives de l’oxygène. À l’aide d’un modèle murin standard d’exposition chronique plus binges à l’alcool, les chercheurs ont observé que l’alcool augmentait fortement les niveaux d’ARN et de protéines de NOX1 et NOX4 dans le foie. Cette hausse s’accompagnait de signes classiques de lésion hépatique : élévation des enzymes hépatiques dans le sang, cellules hépatiques ballonisées et en voie de mort à l’examen microscopique, et preuves nettes d’accumulation de fer et de dépôts lipidiques dans le tissu hépatique. Ces résultats suggèrent que NOX1/4 agissent comme des amorceurs en amont, reliant l’exposition à l’alcool à des perturbations métaboliques et inflammatoires étendues.
Comment le blocage de NOX1/4 calme le fer, les graisses et le stress
L’équipe a testé le Setanaxib, un médicament en développement clinique qui bloque sélectivement NOX1 et NOX4. Les souris recevant du Setanaxib en même temps que l’alcool présentaient beaucoup moins de lésions hépatiques que les animaux traités uniquement par l’alcool. Les mesures du fer ont révélé que le médicament réduisait à la fois le fer ferreux et ferrique dans le foie et diminuait la surface de coloration du fer, tout en abaissant une protéine clé de stockage du fer. Au niveau moléculaire, le Setanaxib semblait rééquilibrer le trafic du fer : il réduisait les niveaux d’hepcidine, une hormone qui piège le fer dans les tissus, restaurait la protéine d’export du fer ferroportine, et abaissait les niveaux du récepteur de la transferrine 1, qui permet l’entrée du fer dans les cellules. Parallèlement, des coupes colorées à l’huile et des analyses sanguines ont montré que le Setanaxib réduisait les triglycérides et les acides gras libres du foie et du sang, indiquant un soulagement de la surcharge lipidique induite par l’alcool.
Reconstruire les défenses hépatiques et apaiser l’inflammation
Au-delà du fer et des lipides, le Setanaxib a contribué à réparer le bouclier antioxydant du foie. L’alcool seul appauvrissait le glutathion, la principale molécule protectrice cellulaire, augmentait sa forme oxydée et relevait les marqueurs de peroxydation lipidique. Il supprimait également l’activité de Nrf2, l’interrupteur maître qui active les gènes antioxydants, entraînant des niveaux plus faibles de protéines protectrices telles que HO-1, SLC7A11 et GPX4, tout en augmentant un marqueur de stress appelé Prx2. Le Setanaxib a inversé ces modifications, rétablissant l’équilibre du glutathion et la signalisation Nrf2 et diminuant les marqueurs de dommage oxydatif. Le médicament a aussi atténué la réponse inflammatoire : il a réduit les niveaux du chimiotactant MCP-1, diminué le nombre de macrophages infiltrants dans le tissu hépatique et baissé à la fois les taux hépatiques et sanguins des médiateurs pro-inflammatoires IL‑1β et IL‑6.
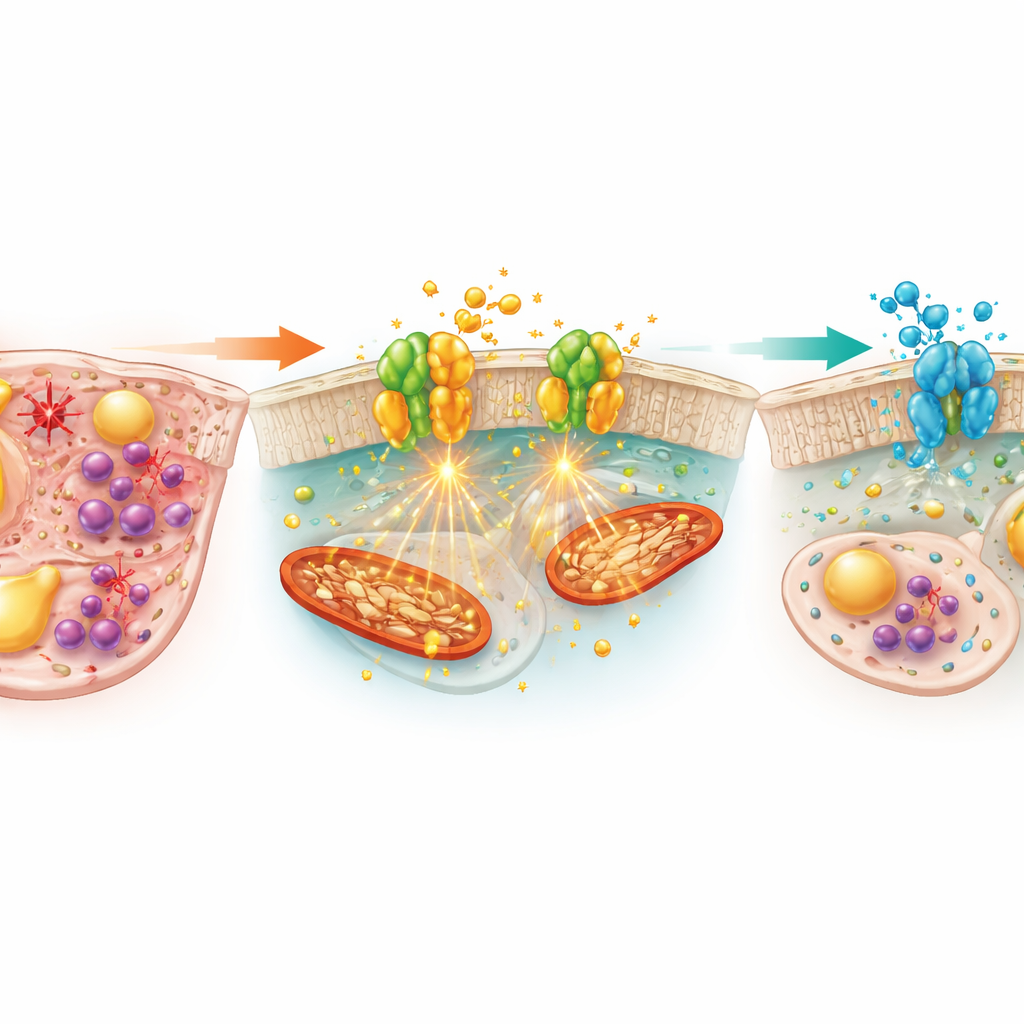
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, ces résultats suggèrent que NOX1 et NOX4 occupent un carrefour central des dommages hépatiques induits par l’alcool, reliant l’excès de fer, l’accumulation lipidique, le stress oxydatif et l’inflammation. En bloquant cette paire d’enzymes, le Setanaxib a pu atténuer simultanément ces quatre processus chez des souris nourries à l’éthanol, offrant une protection plus large que des stratégies ne faisant que reconstituer les antioxydants ou cibler uniquement l’inflammation. Bien que les travaux aient été réalisés sur des animaux et que des questions importantes subsistent sur la sécurité à long terme, le dosage et les effets chez l’humain, l’étude fournit une solide justification pour tester les inhibiteurs de NOX1/4 comme traitements multidimensionnels de la maladie hépatique alcoolique, en particulier chez les patients présentant des signes de surcharge en fer et de stress oxydatif.
Citation: Yu, L., He, T., Zhang, P. et al. NOX1/4 drives hepatic iron and lipid dysregulation, redox imbalance, and inflammation in ethanol-fed mice. Sci Rep 16, 12283 (2026). https://doi.org/10.1038/s41598-026-42716-4
Mots-clés: maladie hépatique alcoolique, stress oxydatif, surcharge en fer, inflammation hépatique, Setanaxib