Clear Sky Science · sv
UTR-DynaPro: en CNN–transformer multimodal språkmodell för avkodning av regleringsmekanismer i 5′UTR
Hur RNA:s främre ände formar liv och medicin
Instruktionerna för att bygga proteiner i våra celler är skrivna i strängar av budbärar-RNA, men inte varje del av den strängen läses av som protein. Ett avsnitt längst i början, kallat 5′ untranslated region, fungerar mer som en kontrollratta än som en ritning. Små förändringar där kan dramatiskt ändra hur mycket protein som produceras, vilket påverkar allt från hur väl ett vaccin fungerar till om en genterapi levererar tillräckligt av ett läkande protein. Denna artikel presenterar en ny artificiell intelligensmodell, UTR-DynaPro, framtagen för att läsa och tolka den kontrollratten mer exakt än tidigare metoder.
Den tysta kontrollzonen före koden
Innan den proteinkodande delen av ett mRNA börjar hjälper 5′ untranslated region (5′UTR) till att avgöra hur effektivt protein kommer att produceras. Dess sekvens och struktur påverkar om cellens proteinproducerande maskineri, ribosomerna, kan fästa, skanna längs och komma igång smidigt. Egenskaper som regionens längd, balansen mellan bokstäverna A, U, G och C, och närvaron av små uppströms startsignaler kan antingen snabba upp eller sakta ner processen. Dessa effekter spelar roll i verkliga tillämpningar: i mRNA-vacciner kan en välanpassad 5′UTR innebära starkare immunitet med mindre doser; i genetiska sjukdomar kan en störande förändring där kraftigt minska proteinproduktionen även när huvudgenkoden är intakt.
Varför äldre prediktionsverktyg brister
Forskare har vänt sig till djupinlärning för att förutsäga hur en given 5′UTR kommer att bete sig, i hopp om att designa sekvenser som ger precis rätt mängd protein. Tidigare modeller tenderar dock att fokusera antingen på mycket korta mönster eller på breda, långdistansrelationer — men inte båda samtidigt. Vissa har svårt att anpassa sig när experimentella förhållanden ändras mellan celltyper eller laboratorieprotokoll, och många ignorerar viktig sidoinformation som RNA:s veckningsenergi eller längden på den proteinkodande regionen. Som en följd har deras noggrannhet nått en platå, vilket begränsar vår förmåga att systematiskt designa 5′UTR:er för vacciner, genterapier och industriell proteinproduktion.
En tvåvägsavläsare för RNA-signaler
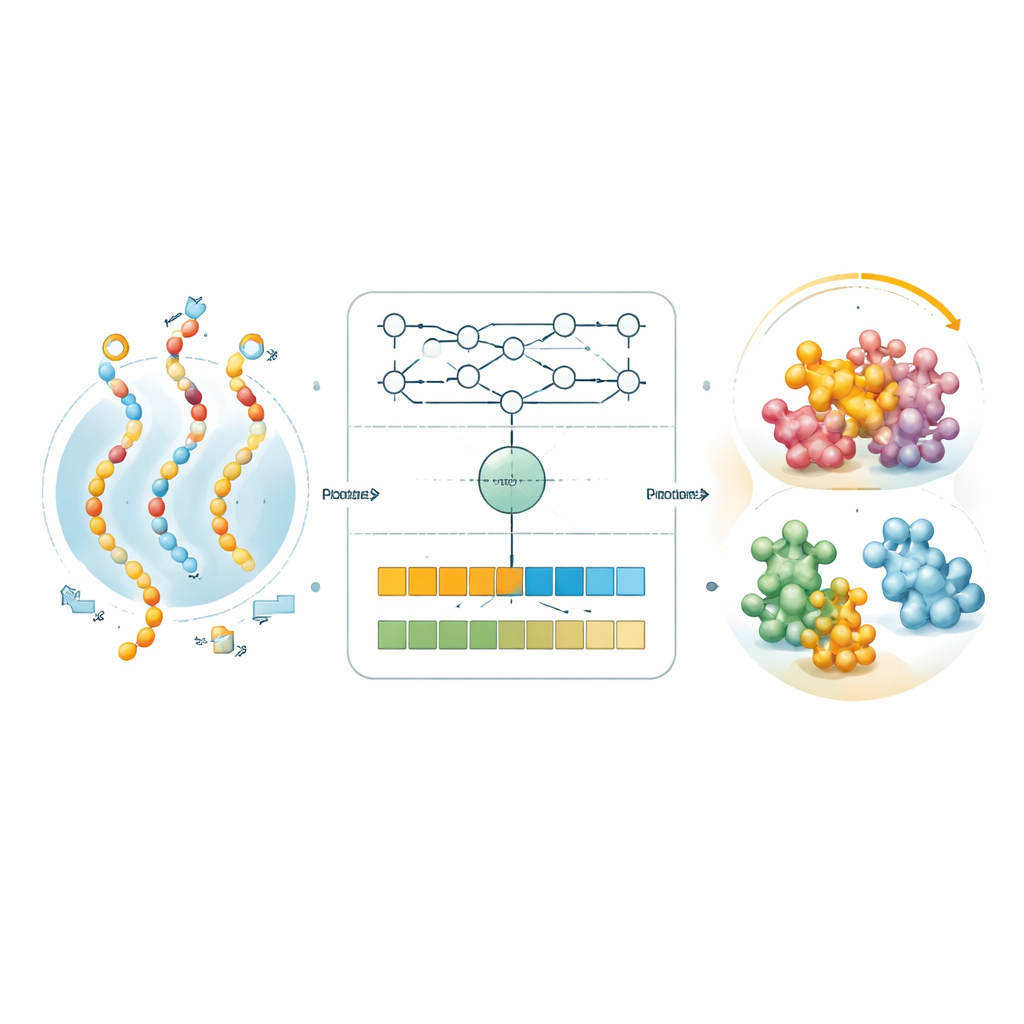
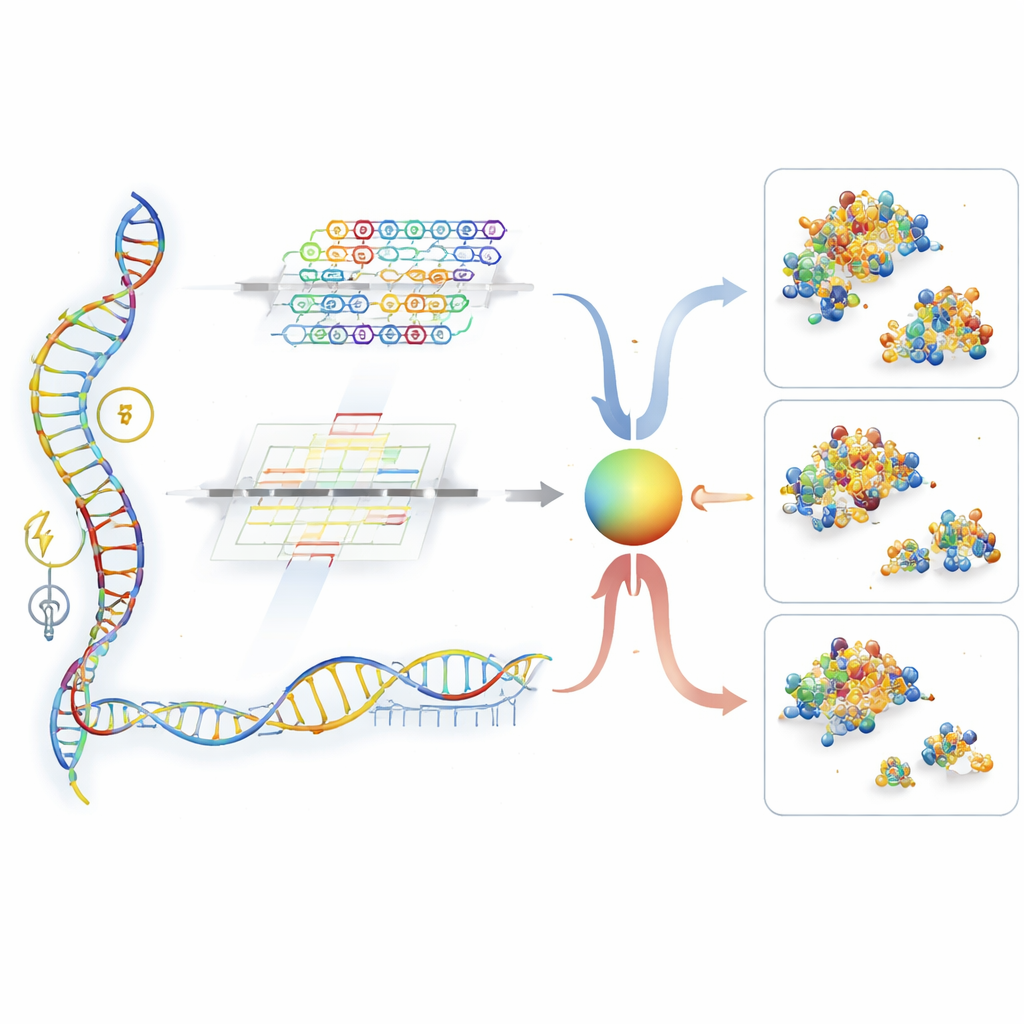
UTR-DynaPro tar sig an dessa brister genom att kombinera två kompletterande sätt att läsa 5′UTR. En väg, baserad på konvolutionsnätverk, är fininställd för att upptäcka korta, lokala mönster — liknande återkommande ”ord” i RNA som fungerar som av/på-strömbrytare. Den andra vägen, byggd av transformerlager, är utmärkt på att fånga långdistansinteraktioner, såsom hur avlägsna delar av strängen veckar sig ihop eller samspelar med den efterföljande kodande regionen. En dynamisk ”grind” avgör sedan, position för position längs RNA:t, hur mycket vikt som ska ges åt lokal respektive global information. Ovanpå detta integrerar modellen extra signaler, inklusive hur tätt RNA:t tenderar att veckas, hur lång den proteinkodande delen är, och om vissa små uppströms läsramar finns närvarande. Tillsammans gör dessa ingredienser det möjligt för UTR-DynaPro att konstruera ett rikt porträtt av hur en 5′UTR sannolikt reglerar proteinproduktion.
Att pröva modellen
Författarna tränade och utvärderade UTR-DynaPro på stora, mångsidiga datasätt: syntetiska och naturliga 5′UTR:er från människor och andra arter, samt mätningar från flera mänskliga celltyper och vävnader. De fokuserade på tre relaterade utfall: genomsnittlig ribosombelastning (hur många ribosomer som i genomsnitt ansamlas på ett mRNA), translationseffektivitet (hur mycket protein som produceras per RNA-molekyl) och den totala uttrycksnivån. I alla dessa uppgifter överträffade den nya modellen konsekvent flera ledande metoder, ibland med nästan tio procent lägre förutsägelsefel. Noggranna ”ablation”-tester — där delar av arkitekturen togs bort eller förenklades — visade att varje huvudkomponent, från tvåvägsdesignen till mixtures-of-experts-submodulerna och ingångar för experimentella förhållanden, mätbart förbättrade prestandan. Visualisering av fusionsgrinden visade vidare att modellen skiftar sitt beroende mellan lokala och globala ledtrådar längs sekvensen och mellan celltyper, vilket speglar den komplexa biologiska logik forskare förväntar sig i detta område.
Från bättre förutsägelser till bättre designer
För icke-specialister är huvudbudskapet att detta arbete erbjuder ett kraftfullare och mer flexibelt sätt att läsa de subtila kontrollinstruktionerna längst fram i ett mRNA. Genom att mer exakt förutsäga hur en förändring i 5′UTR påverkar proteinutsläpp kan UTR-DynaPro vägleda designen av syntetiska sekvenser som ökar eller finjusterar produktionen för specifika behov — starkare vacciner, säkrare genterapier eller bättre industriella enzymer. Samtidigt hjälper dess tolkbara arkitektur forskare att upptäcka både kända och tidigare dolda regleringsmönster. I praktiska termer tar denna modell oss närmare att behandla 5′UTR som en programmerbar kontrollknapp för genuttryck som kan vridas med tillförsikt istället för genom trial-and-error.
Citering: Shen, H., Liu, S., Guo, F. et al. UTR-DynaPro: a CNN–transformer multimodal language model for decoding 5′UTR regulatory mechanisms. Sci Rep 16, 10779 (2026). https://doi.org/10.1038/s41598-026-42175-x
Nyckelord: 5′UTR-reglering, mRNA-translation, djupinlärning för biologi, genuttrycksreglering, design av mRNA-vacciner