Clear Sky Science · sv
ISG-atlasen: en analys av förlust‑av‑funktion som karaktäriserar interferon‑stimulerade geners antivirala egenskaper
Hur våra celler för ett dolt krig mot virus
Människokroppen utsätts ständigt för virus, ändå slår de flesta infektioner aldrig igenom. Denna studie avslöjar hur hundratals beskyddande gener inne i våra celler, som aktiveras av immundämparna interferoner, samarbetar för att bromsa eller i vissa fall underlätta olika virus. Genom att kartlägga detta komplexa nätverk i detalj identifierar forskarna nya svagheter hos virus som SARS‑CoV‑2 och pekar på nya idéer för antivirala behandlingar.
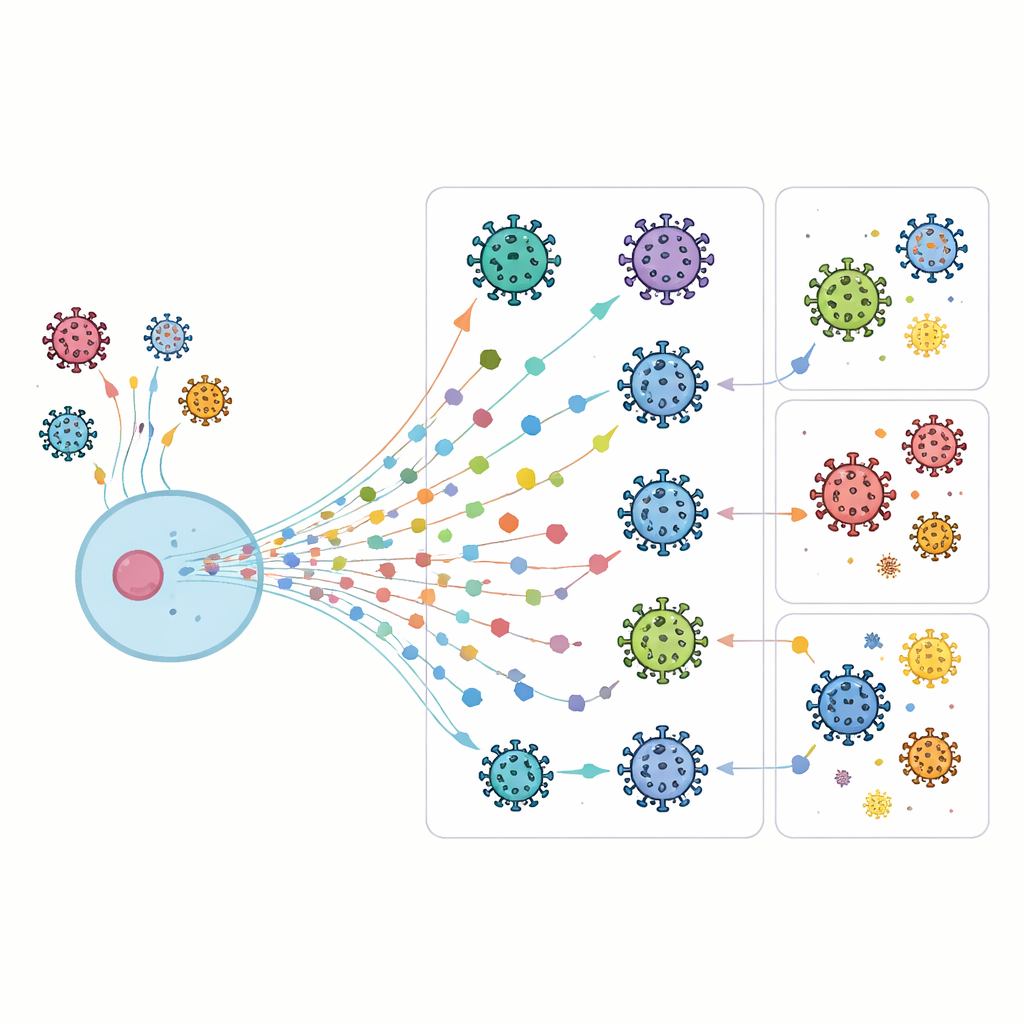
En cellulär larmkedja med många rörliga delar
När celler känner av en viral inkräktare frisätter de interferoner, som i sin tur slår på tusentals interferon‑stimulerade gener (ISG). Dessa gener påverkar nästan alla aspekter av cellbiologin, från hur proteiner tillverkas till hur skadat material avlägsnas. Vissa ISG blockerar ett virus direkt vid specifika steg i dess livscykel, medan andra omformar cellens inre miljö för att göra den mindre gästvänlig för infektion. Eftersom virus utvecklat många knep för att undvika dessa försvar upprätthåller våra celler en stor och överlappande verktygslåda av ISG, vilket skapar ett motståndskraftigt men mycket komplext försvarsnätverk.
En systematisk ”atlas” över antivirala gener
Istället för att konstlat förstärka enstaka gener en i taget valde teamet motsatt strategi: de stängde selektivt av 285 olika ISG i lungliknande celler och följde sedan hur åtta skilda virus betedde sig. Med hjälp av mikroskopi på levande celler under flera dagar mätte de hur snabbt varje virus spred sig och hur starkt det tog över cellpopulationen. Genom att passa in dessa infektionsmönster i tillväxtkurvor kunde de uppskatta både styrkan och hastigheten i viral expansion för varje gen‑virus‑kombination och bygga en tidsupplöst atlas över hur varje ISG formar infektionen.
Gemensamma försvarare, dolda medhjälpare och virus‑specifika effekter
Atlasen bekräftade att välkända aktörer i interferonsignalering, såsom STAT1, STAT2, IRF9 och sensorn DDX58, brett hämmar många virus. Den lyfte också fram oväntade försvarare som tidigare inte kopplats till antiviral aktivitet, inklusive proteiner som är inblandade i proteinnedbrytning, RNA‑behandling och grundläggande cellulär underhåll. Överraskande nog hjälpte en betydande andel ISG i detta system faktiskt virus att replikera. Vissa gener främjade tillväxten av nästan alla testade virus, medan andra visade ”delade personligheter”, blockerade ett virus men gynnade ett annat. Dessa blandade roller tyder på att många ISG finjusterar väsentliga cellprocesser som virus antingen kan exploatera eller störas av, beroende på deras strategi.
Fokusering på SARS‑CoV‑2 och en ny grindvakt
På grund av dess globala påverkan ägnade forskarna särskild uppmärksamhet åt SARS‑CoV‑2. Genom att kombinera sin förlust‑av‑funktion‑atlas med proteininteraktionskartor och proteomiska analyser identifierade de en uppsättning ISG med särskilt stark inverkan på koronavirusets tillväxt. Som väntat framträdde gener som kontrollerar interferonsignalering och kända inträdesspärrar som LY6E som viktiga försvarare. Bland flera nya kandidater utmärkte sig en: BORCS8, en lite studerad komponent i ett komplex som styr rörelse och funktion hos inre vesiklar och lysosomer. När BORCS8 togs bort tog SARS‑CoV‑2 sig in i cellerna mer effektivt, producerade fler infektiösa partiklar och visade liknande fördelar över flera virusvarianter.
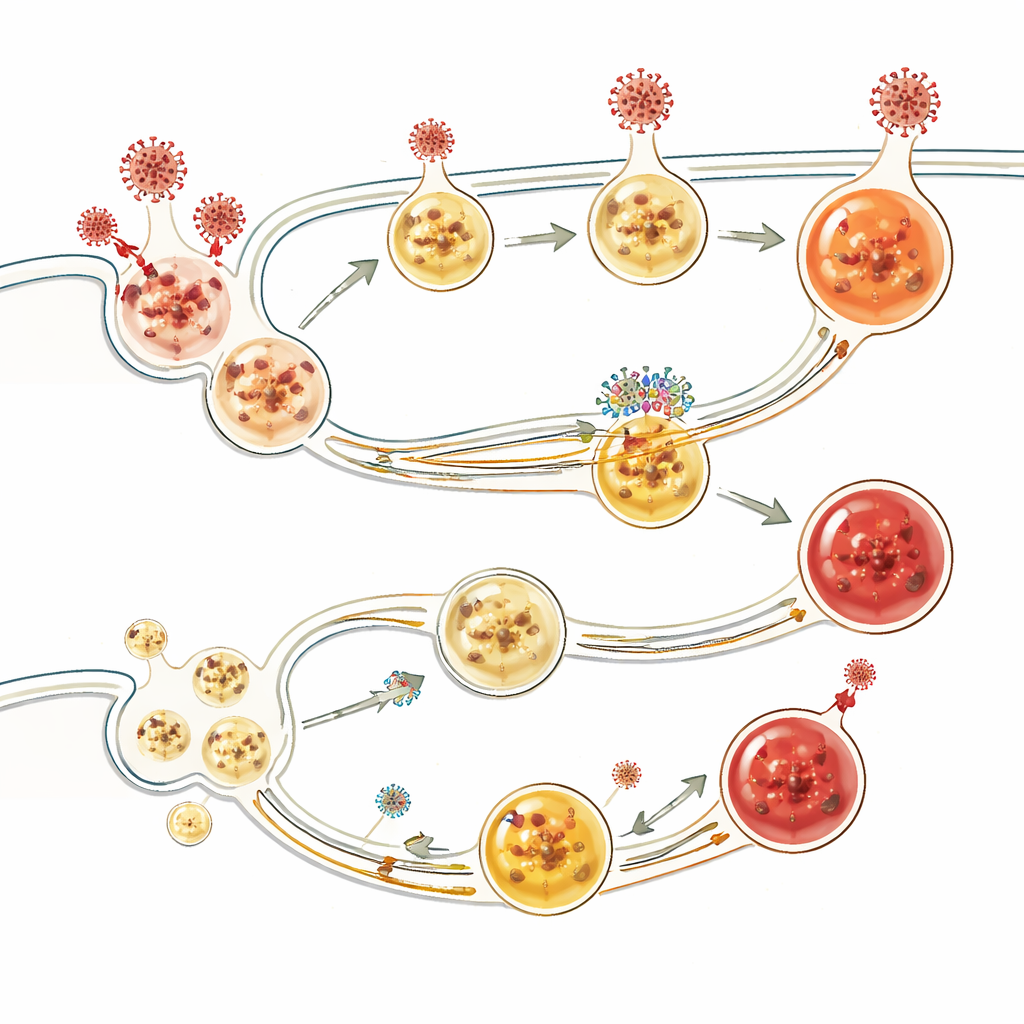
Hur BORCS8 formar virusets inträdesvägar
Ytterligare experiment visade att BORCS8 hjälper till att samordna transport och försurning av endosomer och lysosomer — de små kompartiment som tar emot inkommande material och kan förgöra det. I celler utan BORCS8 klumpade lysosomerna onormalt nära cellkärnan, endocytiska vesiklar blev överdrivet sura men mognade inte korrekt, och viralt material dirigerades inte effektivt mot nedbrytning. Virus som är starkt beroende av endosomal inträde, inklusive SARS‑CoV‑2 i vissa celltyper, kunde därför ta sig igenom lättare. Studien fann också att BORCS8 samarbetar med andra vesikel‑sorteringskomplex och att det påverkar lokaliseringen av SARS‑CoV‑2:s ORF3a‑protein, vilket är involverat i virusets frisättning från celler.
Samarbete för ett starkare antiviralt försvar
Där interferon aktiverar många ISG samtidigt testade författarna hur par av gener beter sig när de inaktiveras tillsammans. Genom att jämföra observerade utfall med matematiska förväntningar upptäckte de synergistiska kombinationer där dubbel förlust gav en mycket större ökning av viral tillväxt än någon av generna ensam. Särskilt förstorade borttagning av både inträdesspärrar (som LY6E eller BORCS8) och komponenter i interferonsignalering (som STAT2 eller IRF9) SARS‑CoV‑2‑replikationen, vilket understryker hur inträdeskontroll och immunsignalering förstärker varandra. Dessa fynd speglar kliniska framgångar där läkemedel som blockerar viralt inträde kombineras med interferon‑baserade terapier.
Vad detta innebär för framtida antivirala strategier
Detta arbete levererar en rik, kvantitativ karta över hur hundratals interferon‑utlösta gener formar ödet för olika virus. För icke‑specialister är huvudbudskapet att vårt antivirala försvar inte drivs av ett fåtal »magiska kulor» utan av ett koordinerat samhälle av gener, varav några oavsiktligt hjälper fienden. Genom att avslöja breda försvarare, virus‑specifika svagheter och kraftfulla genkombinationer erbjuder ISG‑atlasen en ritning för att utforma smartare antivirala strategier — särskilt sådana som parar ihop inträdesspärrar relaterade till BORCS8‑vägar med förstärkare av interferonsignalering för att hålla framtida virushot i schack.
Citering: Krey, K., Risso-Ballester, J., Hamad, S. et al. The ISG Atlas: a loss-of-function analysis characterizes antiviral properties of interferon stimulated genes. Nat Commun 17, 4206 (2026). https://doi.org/10.1038/s41467-026-72732-x
Nyckelord: medfödd immunitet, interferon‑stimulerade gener, antiviral försvar, SARS‑CoV‑2‑inträde, lysosomtrafik