Clear Sky Science · fr
L’atlas des ISG : une analyse par perte de fonction caractérise les propriétés antivirales des gènes stimulés par l’interféron
Comment nos cellules mènent une guerre cachée contre les virus
Le corps humain est constamment bombardé par des virus, et pourtant la plupart des infections ne prennent jamais racine. Cet article révèle comment des centaines de gènes protecteurs à l’intérieur de nos cellules, activés par des molécules immunitaires appelées interférons, agissent de concert pour ralentir ou parfois favoriser différents virus. En cartographiant en détail ce réseau complexe, les chercheurs mettent au jour de nouvelles faiblesses chez des virus comme le SARS-CoV-2 et ouvrent des pistes pour des thérapies antivirales.
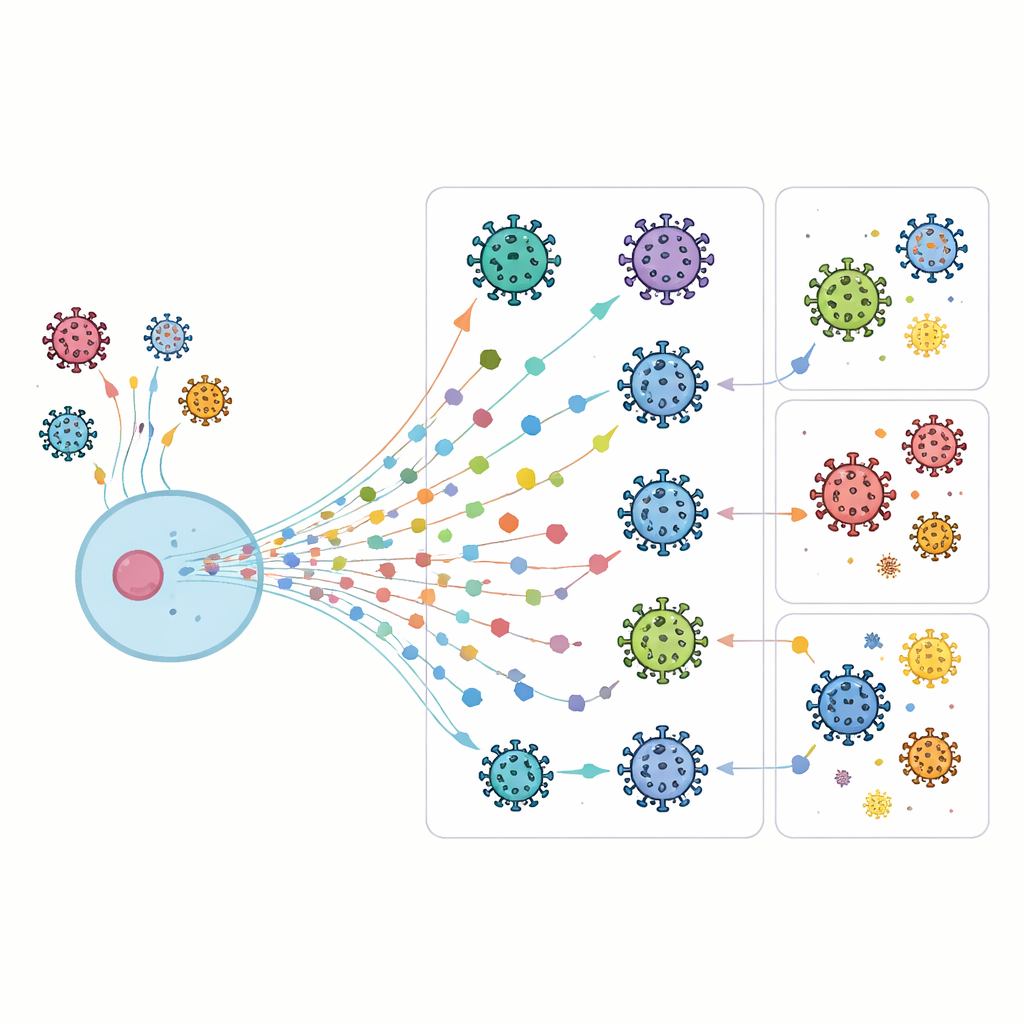
Un système d’alarme cellulaire aux nombreux rouages
Quand les cellules détectent un intrus viral, elles libèrent des interférons, qui à leur tour activent des milliers de gènes stimulés par l’interféron (ISG). Ces gènes influencent presque tous les aspects de la biologie cellulaire, depuis la synthèse des protéines jusqu’à l’élimination du matériel endommagé. Certains ISG bloquent directement un virus à des étapes spécifiques de son cycle de vie, tandis que d’autres modifient l’environnement interne de la cellule pour le rendre moins propice à l’infection. Parce que les virus ont développé de nombreux stratagèmes pour contourner ces défenses, nos cellules maintiennent une boîte à outils étendue et redondante d’ISG, créant un réseau de défense résilient mais extrêmement complexe.
Un « atlas » systématique des gènes antiviraux
Plutôt que de stimuler artificiellement des gènes un par un, l’équipe a adopté l’approche inverse : elle a désactivé sélectivement 285 ISG différents dans des cellules de type pulmonaire, puis observé le comportement de huit virus distincts. À l’aide de microscopie en cellules vivantes sur plusieurs jours, ils ont mesuré la vitesse de propagation de chaque virus et l’ampleur de sa prise en charge de la population cellulaire. En ajustant ces motifs d’infection à des courbes de croissance, ils ont pu estimer à la fois l’intensité et la vitesse d’expansion virale pour chaque combinaison gène–virus, construisant ainsi un atlas résolu dans le temps de l’impact de chaque ISG sur l’infection.
Défenseurs communs, aides dissimulées et effets spécifiques aux virus
L’atlas confirme que des acteurs bien connus de la signalisation par l’interféron, tels que STAT1, STAT2, IRF9 et le senseur DDX58, restreignent largement de nombreux virus. Il met aussi en lumière des défenseurs inattendus, non auparavant reliés à l’action antivirale, incluant des protéines impliquées dans la dégradation des protéines, le traitement de l’ARN et l’entretien cellulaire de base. Fait surprenant, une fraction substantielle d’ISG favorisait en réalité la réplication virale dans ce système. Certains gènes ont soutenu la croissance de presque tous les virus testés, tandis que d’autres ont montré des « personnalités divisées », bloquant un virus mais en aidant un autre. Ces rôles mixtes suggèrent que de nombreux ISG ajustent des processus cellulaires essentiels que les virus peuvent exploiter ou qui peuvent les gêner, selon leur stratégie.
Zoom sur le SARS-CoV-2 et un nouveau gardien
En raison de son impact mondial, les chercheurs ont porté une attention particulière au SARS-CoV-2. En combinant leur atlas par perte de fonction avec des cartes d’interaction protéique et des analyses protéomiques, ils ont identifié un ensemble d’ISG ayant une influence particulièrement forte sur la croissance des coronavirus. Comme prévu, les gènes contrôlant la signalisation par l’interféron et les bloqueurs d’entrée connus comme LY6E se sont imposés comme des défenseurs clés. Parmi plusieurs nouveaux candidats, un a émergé : BORCS8, un composant peu étudié d’un complexe qui régule le mouvement et la fonction des vésicules internes et des lysosomes. Lorsque BORCS8 était supprimé, le SARS-CoV-2 entrait dans les cellules plus efficacement, produisait davantage de particules infectieuses et montrait des avantages similaires à travers plusieurs variantes virales.
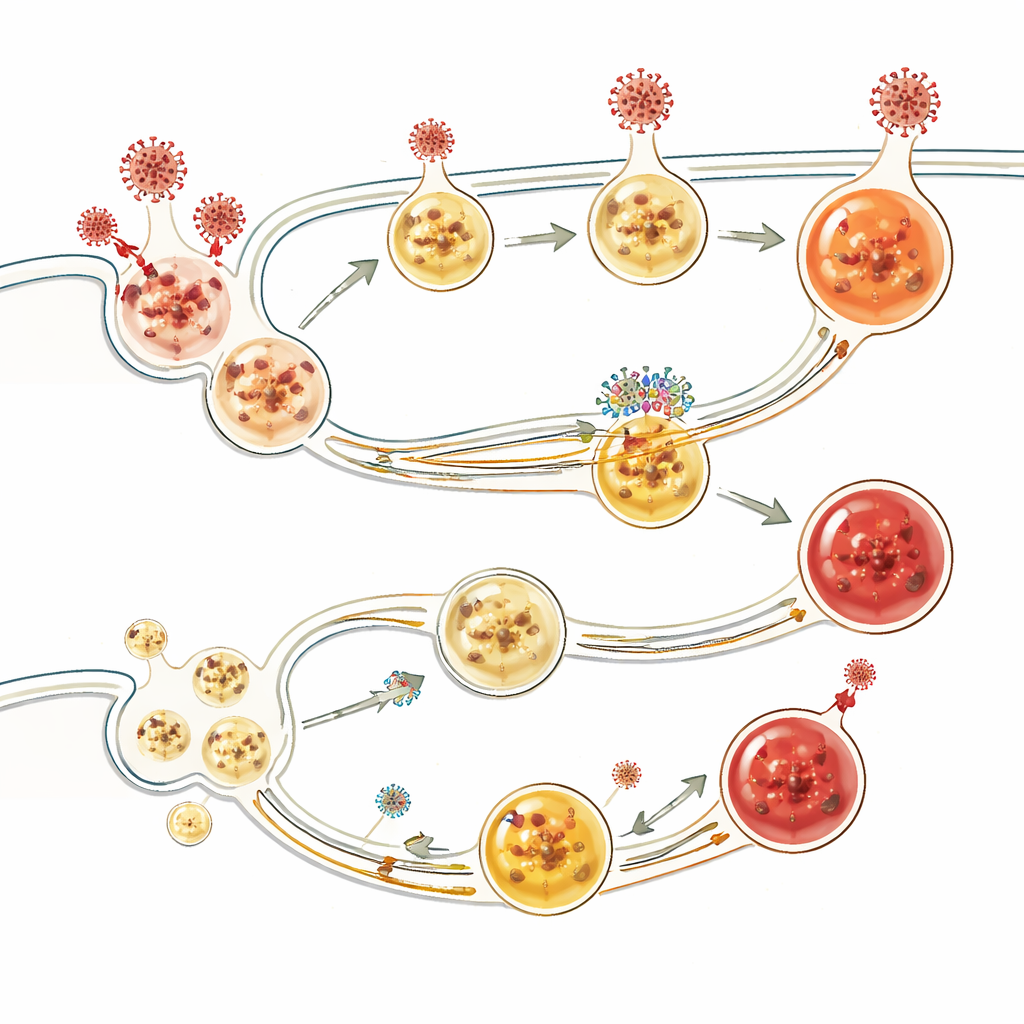
Comment BORCS8 façonne les voies d’entrée virale
D’autres expériences ont révélé que BORCS8 aide à coordonner le transport et l’acidification des endosomes et des lysosomes — ces petits compartiments qui reçoivent le matériel entrant et peuvent le détruire. Dans les cellules dépourvues de BORCS8, les lysosomes se regroupaient anormalement près du noyau, les vésicules endocytées devenaient excessivement acides mais ne maturaient pas correctement, et le matériel viral n’était pas efficacement orienté vers la dégradation. Les virus qui dépendent fortement de l’entrée endosomale, y compris le SARS-CoV-2 dans certains types cellulaires, pouvaient donc passer plus facilement. L’étude a aussi montré que BORCS8 fonctionne en concert avec d’autres complexes de tri des vésicules, et qu’il influence la localisation de la protéine ORF3a du SARS-CoV-2, impliquée dans la libération virale des cellules.
Travailler ensemble pour une défense antivirale renforcée
Parce que l’interféron active simultanément de nombreux ISG, les auteurs ont testé le comportement de paires de gènes quand elles sont inactivées ensemble. En comparant les résultats observés aux attentes mathématiques, ils ont découvert des combinaisons synergiques où la double perte produisait une augmentation bien plus importante de la croissance virale que la perte de chaque gène séparément. Notamment, la suppression conjointe des bloqueurs d’entrée (comme LY6E ou BORCS8) et des composants de la signalisation par l’interféron (comme STAT2 ou IRF9) amplifiait fortement la réplication du SARS-CoV-2, soulignant comment le contrôle de l’entrée et la signalisation immunitaire se renforcent mutuellement. Ces résultats font écho à des succès cliniques où des médicaments bloquant l’entrée virale sont associés à des thérapies à base d’interféron.
Ce que cela implique pour les stratégies antivirales futures
Ce travail fournit une carte riche et quantitative de la façon dont des centaines de gènes déclenchés par l’interféron déterminent le destin de virus divers. Pour les non-spécialistes, le message clé est que notre défense antivirale n’est pas portée par quelques « balles magiques », mais par une communauté coordonnée de gènes, dont certains aident involontairement l’ennemi. En révélant des défenseurs larges, des points faibles spécifiques aux virus et des combinaisons de gènes puissantes, l’atlas des ISG offre une feuille de route pour concevoir des stratégies antivirales plus intelligentes — en particulier celles qui associent des bloqueurs d’entrée, par exemple via des voies liées à BORCS8, à des renforçateurs de la signalisation par l’interféron pour contenir les menaces virales futures.
Citation: Krey, K., Risso-Ballester, J., Hamad, S. et al. The ISG Atlas: a loss-of-function analysis characterizes antiviral properties of interferon stimulated genes. Nat Commun 17, 4206 (2026). https://doi.org/10.1038/s41467-026-72732-x
Mots-clés: immunité innée, gènes stimulés par l’interféron, défense antivirale, entrée du SARS-CoV-2, trafic lysosomal