Clear Sky Science · de
Der ISG-Atlas: Eine Loss-of-Function-Analyse charakterisiert antivirale Eigenschaften interferon‑aktivierter Gene
Wie unsere Zellen einen verborgenen Krieg gegen Viren führen
Der menschliche Körper wird ständig von Viren angegriffen, dennoch schlagen sich die meisten Infektionen nicht durch. Diese Studie zeigt, wie Hunderte schützender Gene in unseren Zellen, die durch Immunbotenstoffe namens Interferone aktiviert werden, gemeinsam wirken, um verschiedene Viren zu verlangsamen oder in manchen Fällen sogar zu fördern. Durch die detaillierte Kartierung dieses komplexen Netzwerks identifizieren die Forschenden neue Verwundbarkeiten von Viren wie SARS‑CoV‑2 und liefern Anhaltspunkte für neuartige antivirale Therapien.
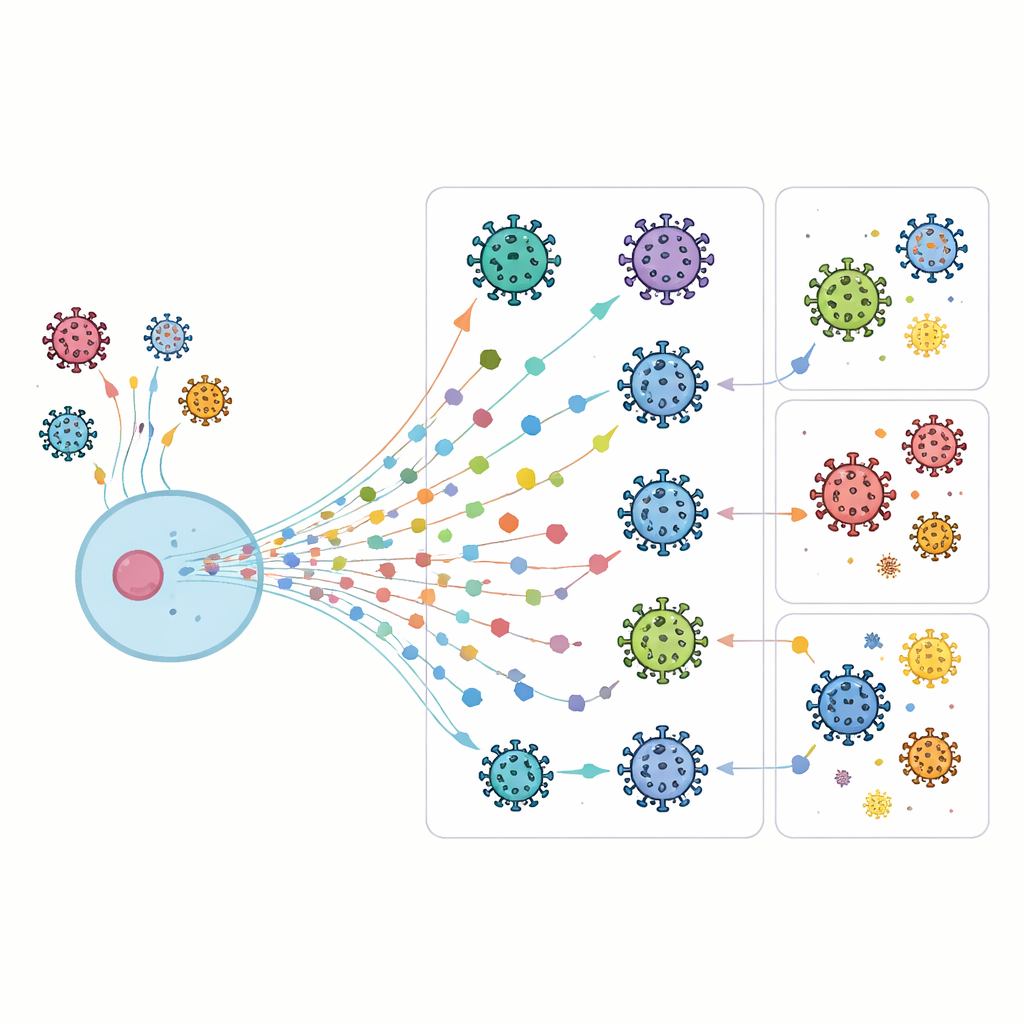
Ein zelluläres Alarmsystem mit vielen Bausteinen
Wenn Zellen einen viralen Eindringling erkennen, schütten sie Interferone aus, die wiederum Tausende von interferonaktivierten Genen (ISGs) einschalten. Diese Gene beeinflussen nahezu jeden Bereich der Zellbiologie, von der Proteinsynthese bis zur Beseitigung beschädigter Bestandteile. Einige ISGs blockieren ein Virus direkt an bestimmten Stadien seines Lebenszyklus, andere verändern das innere Milieu der Zelle, sodass es für eine Infektion weniger geeignet ist. Da Viren zahlreiche Tricks entwickelt haben, um diesen Abwehrmechanismen zu entgehen, unterhalten unsere Zellen ein großes und überlappendes Repertoire an ISGs – ein robustes, aber hochkomplexes Abwehrnetzwerk.
Ein systematischer „Atlas" antiviraler Gene
Statt einzelne Gene jeweils künstlich zu überaktivieren, verfolgte das Team den entgegengesetzten Ansatz: Sie schalteten gezielt 285 verschiedene ISGs in lungenähnlichen Zellen aus und beobachteten dann das Verhalten von acht unterschiedlichen Viren. Mithilfe von Live‑Zellmikroskopie über mehrere Tage maßen sie, wie schnell sich jedes Virus ausbreitete und wie stark es die Zellpopulation dominierte. Durch Anpassung dieser Infektionsmuster an Wachstumskurven konnten sie sowohl Stärke als auch Geschwindigkeit der viralen Expansion für jede Gen‑Virus‑Kombination abschätzen und so einen zeitaufgelösten Atlas erstellen, der zeigt, wie jedes ISG die Infektion beeinflusst.
Geteilte Verteidiger, verborgene Helfer und virus‑spezifische Effekte
Der Atlas bestätigte, dass bekannte Akteure der Interferon‑Signalgebung wie STAT1, STAT2, IRF9 und der Sensor DDX58 viele Viren breit hemmen. Gleichzeitig hob er unerwartete Verteidiger hervor, die zuvor nicht mit antiviraler Wirkung in Verbindung gebracht worden waren, darunter Proteine, die am Proteinabbau, an der RNA‑Verarbeitung und an grundlegender Zellwartung beteiligt sind. Überraschenderweise half ein erheblicher Anteil der ISGs in diesem System tatsächlich den Viren bei der Replikation. Manche Gene förderten das Wachstum nahezu aller getesteten Viren, andere zeigten „geteilte Persönlichkeiten“: Sie blockierten ein Virus, unterstützten aber ein anderes. Diese gemischten Rollen deuten darauf hin, dass viele ISGs essenzielle zelluläre Prozesse feinjustieren, die Viren je nach ihrer Strategie entweder ausnutzen oder durch die sie behindert werden können.
Fokus auf SARS‑CoV‑2 und ein neuer Türsteher
Wegen seiner globalen Bedeutung widmeten die Forschenden SARS‑CoV‑2 besondere Aufmerksamkeit. Durch die Kombination ihres Loss‑of‑Function‑Atlas mit Protein‑Interaktionskarten und Proteomanalysen identifizierten sie eine Gruppe von ISGs mit besonders starker Wirkung auf das Wachstum von Coronaviren. Wie erwartet traten Gene, die die Interferon‑Signalgebung kontrollieren, und bereits bekannte Eintrittsblocker wie LY6E als zentrale Verteidiger hervor. Unter mehreren neuen Kandidaten stach eines hervor: BORCS8, ein wenig untersuchter Bestandteil eines Komplexes, der die Bewegung und Funktion interner Vesikel und Lysosomen steuert. Wurde BORCS8 entfernt, gelang SARS‑CoV‑2 der Eintritt in Zellen effizienter, es entstanden mehr infektiöse Partikel, und ähnliche Vorteile zeigten sich über mehrere Virusvarianten hinweg.
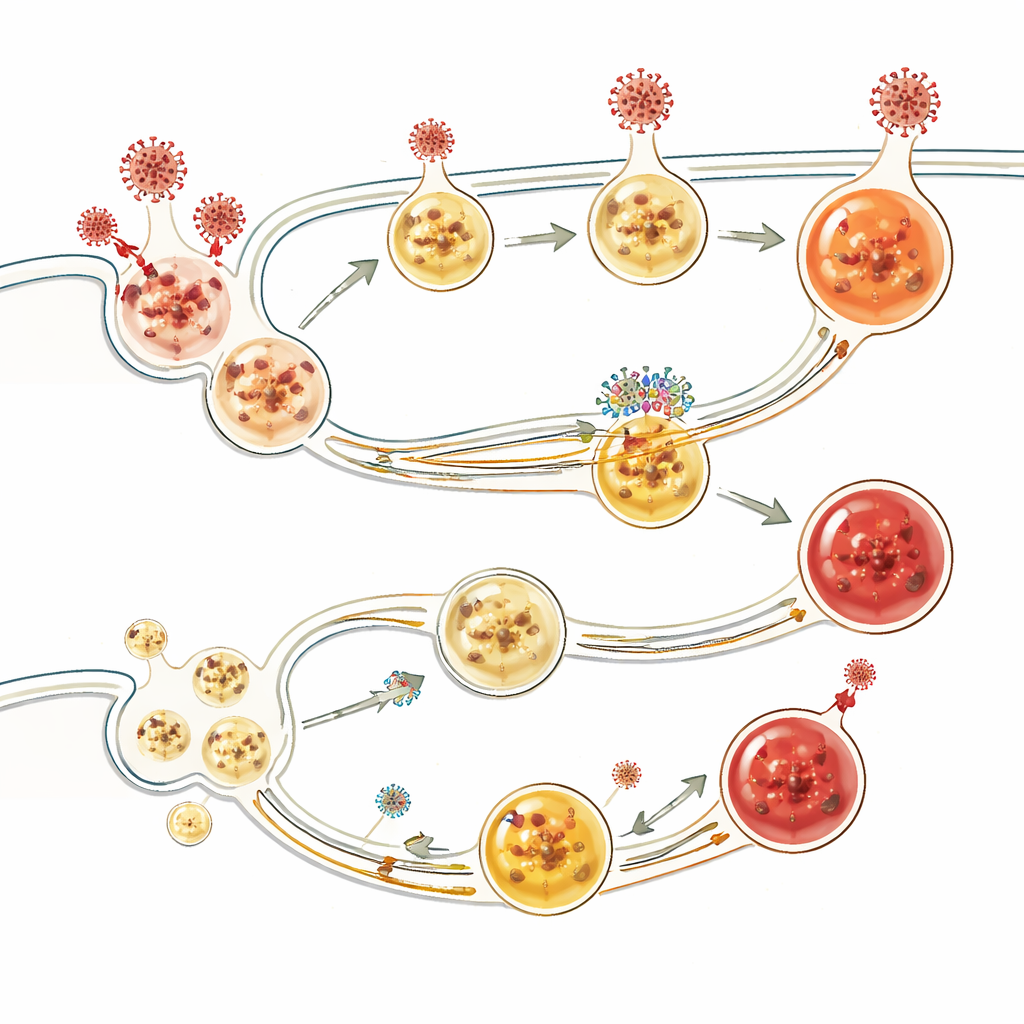
Wie BORCS8 Eintrittswege von Viren formt
Weitere Experimente zeigten, dass BORCS8 dabei hilft, den Transport und die Ansäuerung von Endosomen und Lysosomen zu koordinieren – die kleinen Kompartimente, die eingehende Fracht aufnehmen und zerstören können. In Zellen ohne BORCS8 sammelten sich Lysosomen untypisch nahe dem Zellkern, endozytotische Vesikel wurden übermäßig sauer, reiften aber nicht richtig, und virale Fracht wurde nicht effizient zur Degradation geleitet. Viren, die stark auf endosomalen Eintritt angewiesen sind, einschließlich SARS‑CoV‑2 in bestimmten Zelltypen, konnten daher leichter hindurchschlüpfen. Die Studie fand außerdem, dass BORCS8 mit anderen Vesikel‑Sortierkomplexen zusammenarbeitet und die Lokalisierung des SARS‑CoV‑2‑Proteins ORF3a beeinflusst, das an der Freisetzung von Viren aus Zellen beteiligt ist.
Gemeinsam stärker: Synergien in der antiviralen Abwehr
Da Interferon viele ISGs gleichzeitig aktiviert, testeten die Autoren, wie Genpaare wirken, wenn sie zusammen ausgeschaltet werden. Durch den Vergleich beobachteter Ergebnisse mit mathematischen Erwartungen entdeckten sie synergetische Kombinationen, bei denen ein doppelter Verlust eine deutlich größere Zunahme des viralen Wachstums erzeugte als der Verlust eines einzelnen Gens. Bemerkenswerterweise verstärkte die Entfernung sowohl von Eintrittsblockern (wie LY6E oder BORCS8) als auch von Interferon‑Signalgebern (wie STAT2 oder IRF9) die SARS‑CoV‑2‑Replikation erheblich und unterstrich, wie Eintrittskontrolle und Immun‑Signalgebung sich gegenseitig stärken. Diese Befunde spiegeln klinische Erfolge wider, in denen Wirkstoffe, die den Viruseintritt blockieren, mit interferonbasierten Therapien kombiniert werden.
Was das für künftige antivirale Strategien bedeutet
Diese Arbeit liefert eine reichhaltige, quantitative Karte darüber, wie Hunderte interferonaktivierter Gene das Schicksal unterschiedlicher Viren bestimmen. Für Nicht‑Spezialisten lautet die Kernbotschaft: Unsere antivirale Abwehr beruht nicht auf einigen wenigen „Wunderwaffen“, sondern auf einer koordinierten Gemeinschaft von Genen, von denen einige unbeabsichtigt dem Gegner helfen. Indem der ISG‑Atlas breite Verteidiger, virus‑spezifische Schwachstellen und potente Genkombinationen offenlegt, bietet er einen Bauplan für die Entwicklung klügerer antiviraler Strategien – insbesondere solche, die Eintrittsblocker über BORCS8‑ähnliche Wege mit Verstärkern der Interferon‑Signalgebung kombinieren, um künftige virale Bedrohungen in Schach zu halten.
Zitation: Krey, K., Risso-Ballester, J., Hamad, S. et al. The ISG Atlas: a loss-of-function analysis characterizes antiviral properties of interferon stimulated genes. Nat Commun 17, 4206 (2026). https://doi.org/10.1038/s41467-026-72732-x
Schlüsselwörter: angeborene Immunität, interferonaktivierte Gene, antivirale Abwehr, SARS-CoV-2 Eintritt, Lysosom-Transport