Clear Sky Science · sv
Komplementreceptor 3 (CR3)-beroende mikroglial synapsborttagning driver Parkinsons sjukdomspatogenes vid systemisk inflammation
Varför denna studie är viktig för hälsa i vardagen
Parkinsons sjukdom är mest känd för att orsaka skakningar och stelhet, men långt innan dessa symptom uppträder pågår subtil skada i hjärnan. Denna studie visar hur en kraftig immunreaktion i kroppen – till exempel vid infektion eller kronisk inflammation – tyst kan radera de små förbindelserna mellan hjärnceller som styr rörelse och därigenom bana väg för Parkinson-liknande degeneration. Att förstå denna tidiga ”tysta” fas kan öppna ett fönster för behandlingar som förhindrar eller bromsar sjukdomen innan större skador uppstår.
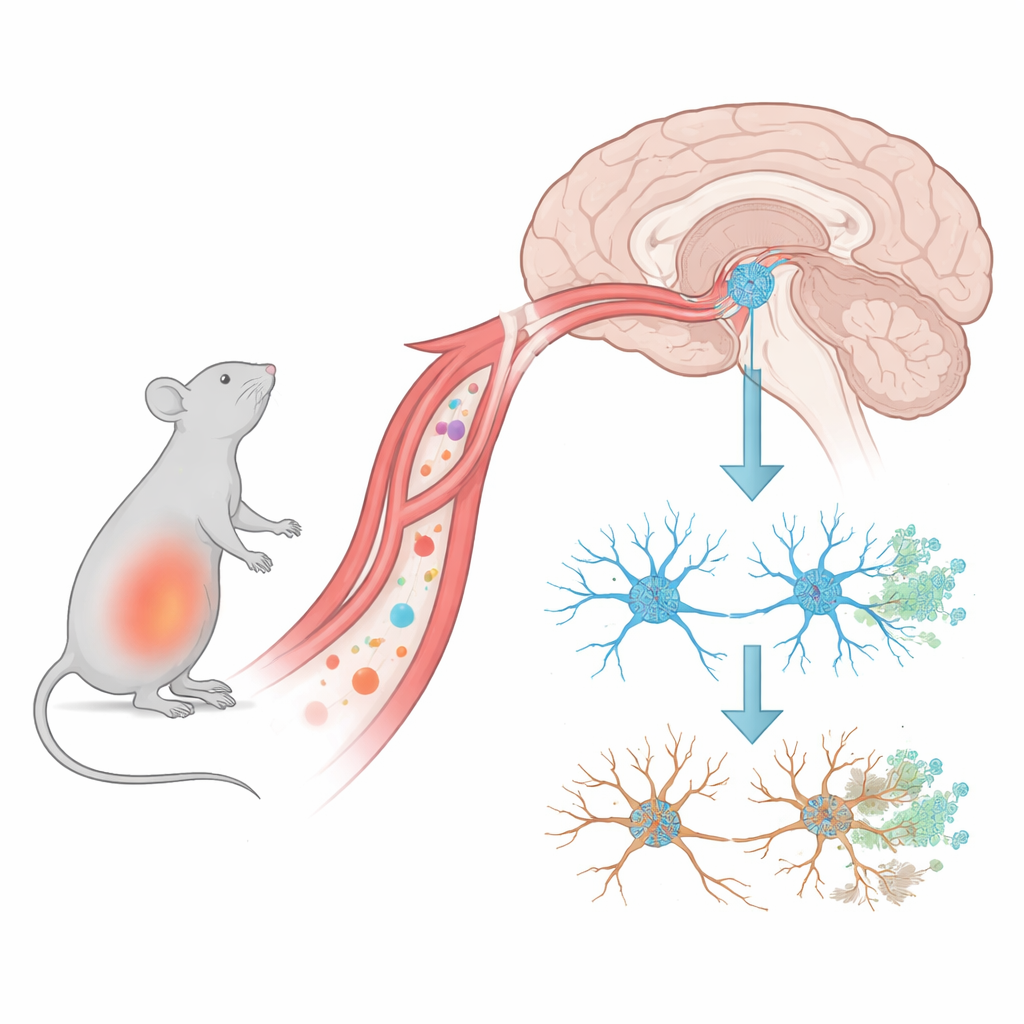
Tidig problematik vid hjärnans kommunikationspunkter
Forskarna använde möss som utsattes för en bakteriekomponent kallad LPS för att efterlikna en kroppsomfattande inflammationsattack. De följde sedan förändringar i en mellanhjärnsregion som hyser dopaminproducerande nervceller, vilka är avgörande för mjuka rörelser och hårt påverkade vid Parkinsons sjukdom. De fann att redan en dag efter den sista inflammationsinsatsen hade antalet synapser – de mikroskopiska kontaktpunkterna där nervceller kommunicerar – minskat. Däremot dog de dopaminproducerande nervcellerna inte i någon märkbar utsträckning förrän först omkring två veckor senare. Denna tidsmässiga förlopp tyder på att det tidigaste skadetillståndet i denna Parkinson-liknande modell inte är neuronernas död, utan den tysta förlusten av deras förbindelser.
Hjärnans immunceller som överivriga städare
Hjärnans egna immunceller, kallade mikroglia, fungerar som väktare och städare: de övervakar omgivningen och avlägsnar skräp, inklusive svaga eller onödiga synapser. I de inflammerade mössen såg teamet att mikroglia i mellanhjärnan blev kraftigt aktiverade samtidigt som synapsförlusten började. Cellerna svällde, ändrade form och uppvisade ökade nivåer av interna ”nedbrytande” strukturer, tecken på att de gick in i ett aggressivt städläge. Tredimensionell bildgivning visade att mikroglia faktiskt slukade både den sändande och den mottagande sidan av synapserna. Denna intensiva beskärning var som starkast en dag efter inflammationen och avtog därefter gradvis, även om den tidiga vågen av synapsförlust banade väg för senare neuronsdöd.
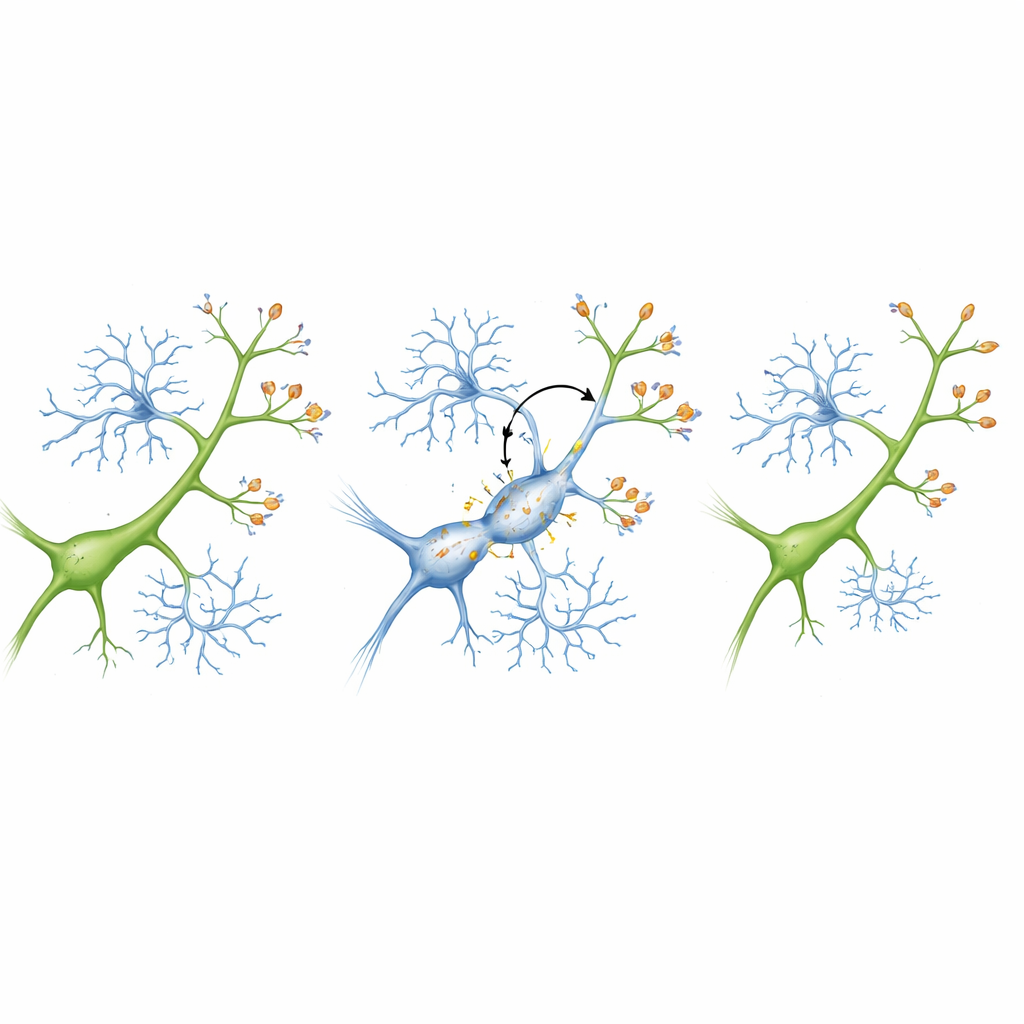
Ett märkssystem som flaggar synapser för borttagning
För att förstå varför mikroglia plötsligt vände sig mot synapser som såg friska ut fokuserade forskarna på ett molekylärt ”märknings”-system känt som komplementvägen. I detta system täcker små proteiner mål som ska avlägsnas, och mikroglia bär receptorer som känner igen dessa märken. Teamet fann att ett komplementprotein, C3, blev mer förekommande på synapser i de inflammerade mössen, medan en matchande receptor, CR3, ökade på mikroglia. Detta par flaggade effektivt synapser för borttagning. När författarna återskapade systemet i odlingsskålar med neuroner och mikroglia skadade inflammation ensamt inte isolerade neuroner. Men när mikroglia fanns närvarande minskade synapsantalet kraftigt vid inflammation – och att blockera C3 eller minska CR3 på mikroglia skyddade dessa synapser och höll neuronerna friskare.
Att stänga av den skadliga vägen i levande hjärnor
Forskarna testade sedan om man genom att stänga av CR3 specifikt i mikroglia kunde skydda hjärnorna hos levande möss. De använde ett viralt verktyg för att reducera CR3 endast i mikroglia innan de inducerade systemisk inflammation. Hos dessa djur dämpades komplementaktiviteten, mikroglia var mindre aktiverade och de åt upp betydligt färre synapser. Som en följd bevarades synapstätheten i mellanhjärnan bättre kort efter inflammationen, och veckor senare var de dopaminproducerande neuronerna mycket mindre benägna att dö. Mikroglia visade också en mer normal, förgrenad form istället för den kompakt, attackberedda formen som sågs vid okontrollerad inflammation, vilket tyder på att blockad av CR3 hindrade dem från att hamna i ett skadligt överdriftsläge.
Vad detta innebär för framtida Parkinsonvård
Detta arbete omformulerar tidig Parkinson-liknande skada som ett problem med felaktig städning snarare än omedelbar celldöd. Systemisk inflammation tycks aktivera ett synaps-märkningssystem som får mikroglia att ta bort viktiga förbindelser via C3–CR3-vägen; först senare faller de dopaminproducerande neuronerna ihop. För en lekman är slutsatsen att hjärnhälsa inte bara beror på nervcellernas överlevnad utan också på bevarandet av deras kommunikationslinjer, särskilt vid kraftig immunsvar i kroppen. Genom att rikta in sig på de specifika molekyler som talar om för mikroglia vilka synapser de ska ta bort, kan framtida terapier potentiellt skydda dessa förbindelser och bromsa eller förhindra progressionen av Parkinsons sjukdom.
Citering: Cai, L., Zhang, Y., Li, J. et al. Complement receptor 3 (CR3)-dependent microglial synapse elimination drives Parkinson’s disease pathogenesis in systemic inflammation. Cell Death Dis 17, 319 (2026). https://doi.org/10.1038/s41419-026-08557-9
Nyckelord: Parkinsons sjukdom, mikroglia, förlust av synapser, neuroinflammation, komplementsystemet