Clear Sky Science · de
Komplementrezeptor 3 (CR3)-abhängige Mikroglia-Synapsenelimination treibt die Pathogenese der Parkinson-Krankheit bei systemischer Entzündung voran
Warum diese Studie für die Gesundheit im Alltag wichtig ist
Die Parkinson-Krankheit ist vor allem für das Auftreten von Tremor und Steifheit bekannt, doch lange bevor diese Symptome sichtbar werden, laufen im Gehirn bereits subtile Schäden ab. Diese Studie zeigt, wie eine starke Immunreaktion im Körper – etwa durch eine Infektion oder chronische Entzündung – die winzigen Verbindungsstellen zwischen Nervenzellen, die die Bewegung steuern, unbemerkt abbauen kann und so den Boden für eine Parkinson-ähnliche Degeneration bereitet. Das Verständnis dieser frühen „stummen“ Phase könnte ein Zeitfenster für Therapien eröffnen, die die Erkrankung verhindern oder verlangsamen, bevor erheblicher Schaden entsteht.
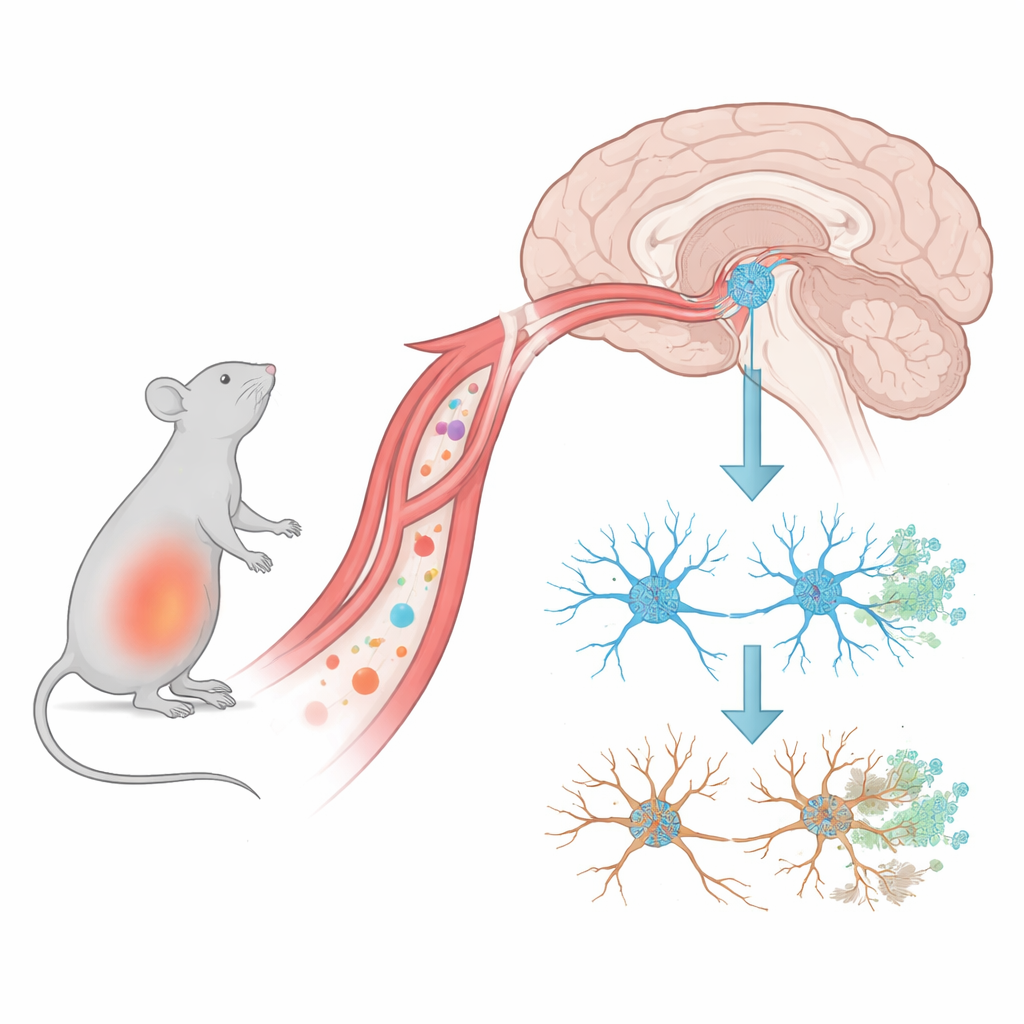
Frühe Probleme an den Kommunikationspunkten des Gehirns
Die Autoren verwendeten Mäuse, die einem bakteriellen Bestandteil namens LPS ausgesetzt wurden, um einen Schub systemischer Entzündung nachzuahmen. Sie verfolgten dann Veränderungen in einer Mittelhirnregion, die dopaminproduzierende Nervenzellen beherbergt – diese sind wichtig für flüssige Bewegungen und bei Parkinson stark betroffen. Sie fanden heraus, dass bereits einen Tag nach dem letzten entzündlichen Reiz die Anzahl der Synapsen – der mikroskopischen Kontaktstellen, an denen Nervenzellen miteinander kommunizieren – zurückgegangen war. Im Gegensatz dazu starben die dopaminproduzierenden Nervenzellen selbst erst etwa zwei Wochen später in nennenswertem Umfang. Dieses Timing deutet darauf hin, dass der früheste Schaden in diesem Parkinson-ähnlichen Zustand nicht der Zelltod der Neurone ist, sondern der leise Verlust ihrer Verbindungen.
Gehirn-Immunkompetente Zellen als übertriebene Reinigungskräfte
Die residenten Immunzellen des Gehirns, die Mikroglia, fungieren als Wächter und Haushälter: Sie überwachen die Umgebung und entfernen Trümmer, einschließlich schwacher oder überflüssiger Synapsen. Bei den entzündeten Mäusen beobachtete das Team, dass Mikroglia im Mittelhirn hochaktiv wurden, sobald der Synapsenverlust begann. Diese Zellen schwollen an, änderten ihre Form und zeigten erhöhte Mengen innerer "Verdauungs"-Strukturen – Anzeichen dafür, dass sie in einen aggressiven Reinigungsmodus geschaltet hatten. Dreidimensionale Bildgebung zeigte, dass Mikroglia tatsächlich sowohl die sendenden als auch die empfangenden Seiten von Synapsen verschlangen. Dieses intensive Beschneiden war am stärksten einen Tag nach der Entzündung und nahm dann allmählich ab, obwohl die frühe Welle des Synapsenverlusts den Boden für den späteren Neuronenverlust bereitete.
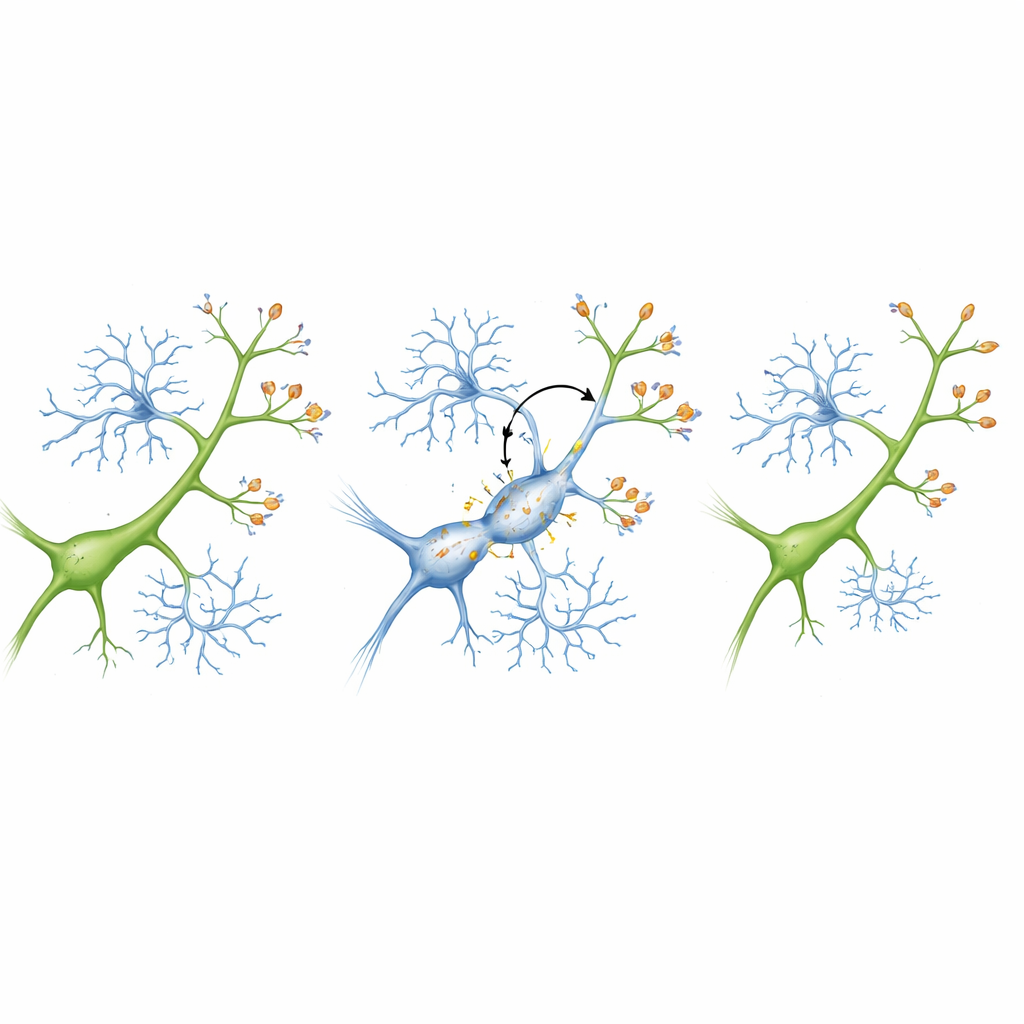
Ein Markiersystem, das Synapsen zur Entfernung kennzeichnet
Um zu verstehen, warum Mikroglia plötzlich gesunde aussehende Synapsen angriffen, konzentrierten sich die Forschenden auf ein molekulares "Markiersystem", bekannt als Komplementweg. In diesem System überziehen kleine Proteine Ziele, die entfernt werden sollen, und Mikroglia tragen Rezeptoren, die diese Markierungen erkennen. Das Team fand, dass ein Komplementprotein, C3, an Synapsen in den entzündeten Mäusen vermehrt auftrat, während ein passender Rezeptor, CR3, an den Mikroglia zunahm. Dieses Paar markierte Synapsen effektiv zur Entfernung. Als die Autoren das System in Zellkulturen mit Neuronen und Mikroglia nachstellten, schadete Entzündung allein isolierten Neuronen nicht. Sobald jedoch Mikroglia vorhanden waren, reduzierte Entzündung die Synapsenzahl stark – und das Blockieren von C3 oder das Reduzieren von CR3 auf Mikroglia schützte diese Synapsen und erhielt die Gesundheit der Neurone.
Den schädigenden Weg im lebenden Gehirn abschalten
Die Forschenden testeten anschließend, ob das gezielte Abschalten von CR3 in Mikroglia die Gehirne lebender Mäuse schützen könnte. Sie verwendeten ein virales Werkzeug, um CR3 nur in Mikroglia vor der Induktion systemischer Entzündung zu reduzieren. In diesen Tieren war die Komplementaktivität gedämpft, Mikroglia waren weniger aktiviert und sie verschlangen deutlich weniger Synapsen. Infolgedessen blieb die Synapsendichte im Mittelhirn kurz nach der Entzündung besser erhalten, und Wochen später waren die dopaminproduzierenden Neurone deutlich weniger dem Tod ausgesetzt. Mikroglia zeigten außerdem eine normalere, verzweigte Gestalt statt der kompakten, angreifbereiten Form, die bei unkontrollierter Entzündung beobachtet wurde, was darauf hindeutet, dass das Blockieren von CR3 sie davon abhielt, in einen schädlichen Übersteuerungszustand zu geraten.
Was das für die zukünftige Parkinson-Versorgung bedeutet
Diese Arbeit rahmt frühzeitige Parkinson-ähnliche Schäden als Problem fehlgeleiteter Reinigung statt unmittelbaren Zelltods. Systemische Entzündung scheint ein Synapsen-Markiersystem zu aktivieren, das Mikroglia dazu veranlasst, über den C3–CR3-Weg wichtige Verbindungen abzutragen; erst später fallen die dopaminproduzierenden Neurone. Für Laien lautet die Schlussfolgerung, dass die Gesundheit des Gehirns nicht nur vom Überleben der Nervenzellen abhängt, sondern auch vom Erhalt ihrer Kommunikationswege, besonders während Phasen starker Immunaktivierung im Körper. Durch das Anvisieren der spezifischen Moleküle, die Mikroglia sagen, welche Synapsen sie "fressen" sollen, könnten künftige Therapien diese Verbindungen schützen und das Fortschreiten der Parkinson-Krankheit verlangsamen oder verhindern.
Zitation: Cai, L., Zhang, Y., Li, J. et al. Complement receptor 3 (CR3)-dependent microglial synapse elimination drives Parkinson’s disease pathogenesis in systemic inflammation. Cell Death Dis 17, 319 (2026). https://doi.org/10.1038/s41419-026-08557-9
Schlüsselwörter: Morbus Parkinson, Mikroglia, Synapsenverlust, Neuroinflammation, Komplementsystem