Clear Sky Science · es
El receptor del complemento 3 (CR3)-dependiente eliminación de sinapsis por microglía impulsa la patogenia de la enfermedad de Parkinson en la inflamación sistémica
Por qué este estudio importa para la salud diaria
La enfermedad de Parkinson es más conocida por provocar temblores y rigidez, pero mucho antes de que aparezcan esos síntomas, ya se están produciendo daños sutiles en el cerebro. Este estudio muestra cómo una reacción inmune intensa en el cuerpo —por ejemplo, a causa de una infección o inflamación crónica— puede despojar silenciosamente las pequeñas conexiones entre las células cerebrales que controlan el movimiento, preparando el terreno para una degeneración similar a la del Parkinson. Comprender esta fase temprana “silenciosa” puede abrir una ventana para tratamientos que prevengan o ralenticen la enfermedad antes de que ocurra un daño importante.
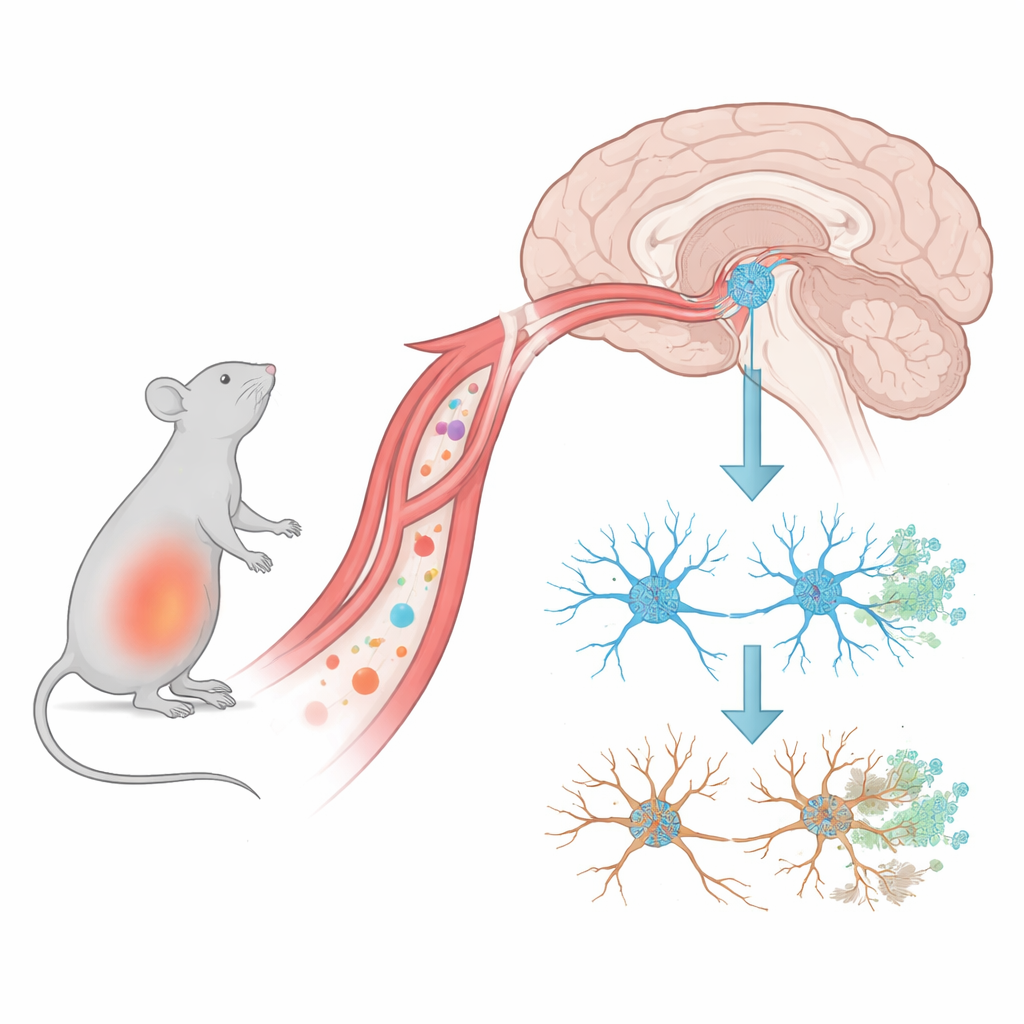
Problemas tempranos en los puntos de comunicación del cerebro
Los autores emplearon ratones expuestos a un componente bacteriano llamado LPS para imitar un estallido de inflamación sistémica. Luego siguieron los cambios en una región del mesencéfalo que alberga neuronas productoras de dopamina, cruciales para el movimiento suave y muy afectadas en la enfermedad de Parkinson. Encontraron que, en solo un día tras el último golpe inflamatorio, el número de sinapsis —los puntos microscópicos de contacto donde las neuronas se comunican— ya había disminuido. En cambio, las propias neuronas productoras de dopamina no mostraron una pérdida apreciable hasta aproximadamente dos semanas después. Esta cronología sugiere que el daño más temprano en este estado similar al Parkinson no es la muerte neuronal, sino la pérdida silenciosa de sus conexiones.
Las células inmunitarias del cerebro como limpiadoras excesivas
Las células inmunitarias residentes del cerebro, llamadas microglías, actúan como centinelas y encargadas de la limpieza: vigilan el entorno y eliminan desechos, incluidas sinapsis débiles o innecesarias. En los ratones inflamados, el equipo observó que las microglías en el mesencéfalo se activaron intensamente en cuanto comenzó la pérdida de sinapsis. Estas células aumentaron de tamaño, cambiaron de forma y mostraron niveles elevados de estructuras internas “digestivas”, señales de que estaban en un modo agresivo de limpieza. La imagen tridimensional reveló que las microglías estaban realmente engullendo tanto el lado emisor como el receptor de las sinapsis. Esta intensa poda fue más fuerte un día después de la inflamación y luego fue disminuyendo gradualmente, aunque la primera ola de pérdida sináptica sentó las bases para la muerte neuronal posterior.
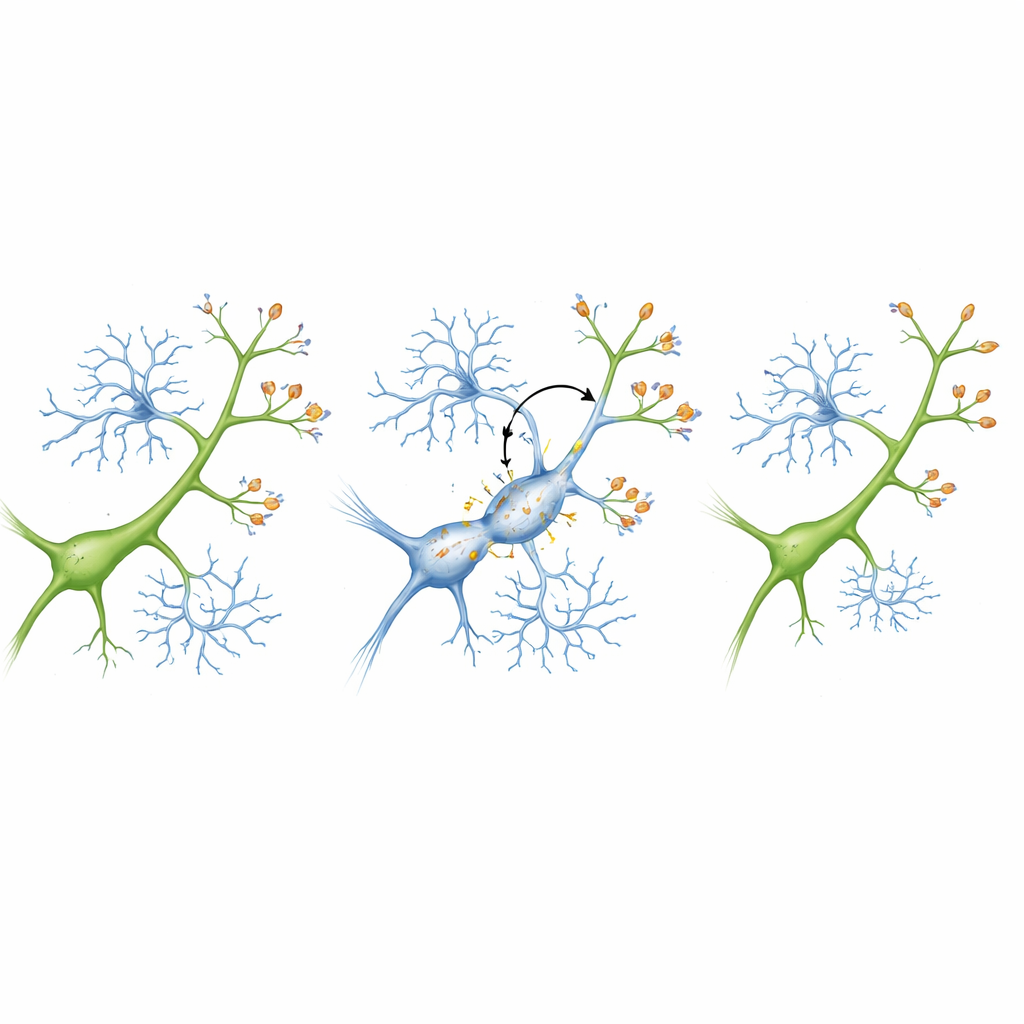
Un sistema de etiquetado que marca sinapsis para su eliminación
Para entender por qué las microglías de repente atacaron sinapsis que parecían sanas, los investigadores se centraron en un sistema molecular de “etiquetado” conocido como la vía del complemento. En este sistema, pequeñas proteínas cubren objetivos que deben ser eliminados, y las microglías llevan receptores que reconocen esas etiquetas. El equipo halló que una proteína del complemento, C3, se volvió más abundante en las sinapsis de los ratones inflamados, mientras que un receptor correspondiente, CR3, aumentó en las microglías. Este emparejamiento marcó efectivamente las sinapsis para su eliminación. Cuando los autores recrearon el sistema en placas de laboratorio con neuronas y microglías, la inflamación por sí sola no dañó a las neuronas aisladas. Pero cuando las microglías estaban presentes, la inflamación redujo drásticamente el número de sinapsis; bloquear C3 o reducir CR3 en las microglías protegió esas sinapsis y mantuvo a las neuronas más saludables.
Apagar la vía dañina en cerebros vivos
Los investigadores probaron luego si inhibir CR3 específicamente en microglías podía proteger los cerebros de ratones vivos. Utilizaron una herramienta viral para reducir CR3 solo en microglías antes de inducir inflamación sistémica. En estos animales, la actividad del complemento se atenuó, las microglías se activaron menos y fagocitaron muchas menos sinapsis. Como resultado, la densidad sináptica en el mesencéfalo se conservó mejor poco después de la inflamación y, semanas más tarde, las neuronas productoras de dopamina tuvieron mucha menos probabilidad de morir. Las microglías también mostraron una morfología más normal y ramificada en lugar de la forma compacta y lista para atacar observada bajo la inflamación descontrolada, lo que sugiere que bloquear CR3 impidió que entraran en un estado de sobreactivación perjudicial.
Qué significa esto para el cuidado futuro del Parkinson
Este trabajo replantea el daño temprano similar al Parkinson como un problema de limpieza errónea más que de muerte celular inmediata. La inflamación sistémica parece activar un sistema de etiquetado sináptico que hace que las microglías retiren conexiones cruciales a través de la vía C3–CR3; solo después sucumben las neuronas productoras de dopamina. Para el público general, la conclusión es que la salud cerebral depende no solo de la supervivencia de las neuronas, sino también de la preservación de sus líneas de comunicación, especialmente durante episodios de fuerte activación inmune en el cuerpo. Al dirigir las moléculas específicas que indican a las microglías qué sinapsis deben “comer”, las terapias futuras podrían proteger estas conexiones y ralentizar o prevenir la progresión de la enfermedad de Parkinson.
Cita: Cai, L., Zhang, Y., Li, J. et al. Complement receptor 3 (CR3)-dependent microglial synapse elimination drives Parkinson’s disease pathogenesis in systemic inflammation. Cell Death Dis 17, 319 (2026). https://doi.org/10.1038/s41419-026-08557-9
Palabras clave: Enfermedad de Parkinson, microglía, pérdida de sinapsis, neuroinflamación, sistema del complemento