Clear Sky Science · ru
Разработка и валидация активируемого ПЭТ‑радиотракера для выявления внеклеточной активности миелопероксидазы при детекции нестабильной атеросклеротической бляшки
Почему это важно для здоровья сердца
Большинство инфарктов и инсультов вызываются не самыми большими закупорками артерий, а небольшими, хрупкими участками жирового отложения, которые внезапно рвутся или разрушаются. Врачам сейчас трудно предсказать, какие бляшки готовы вызвать осложнение. В этом исследовании предложен новый контрастный агент для ПЭТ‑сканирования, который разработан так, чтобы «загораться» только в тех «опасных» бляшках, где действует определённый провоспалительный фермент, что потенциально поможет находить зоны высокого риска в артериях до наступления экстренной ситуации.
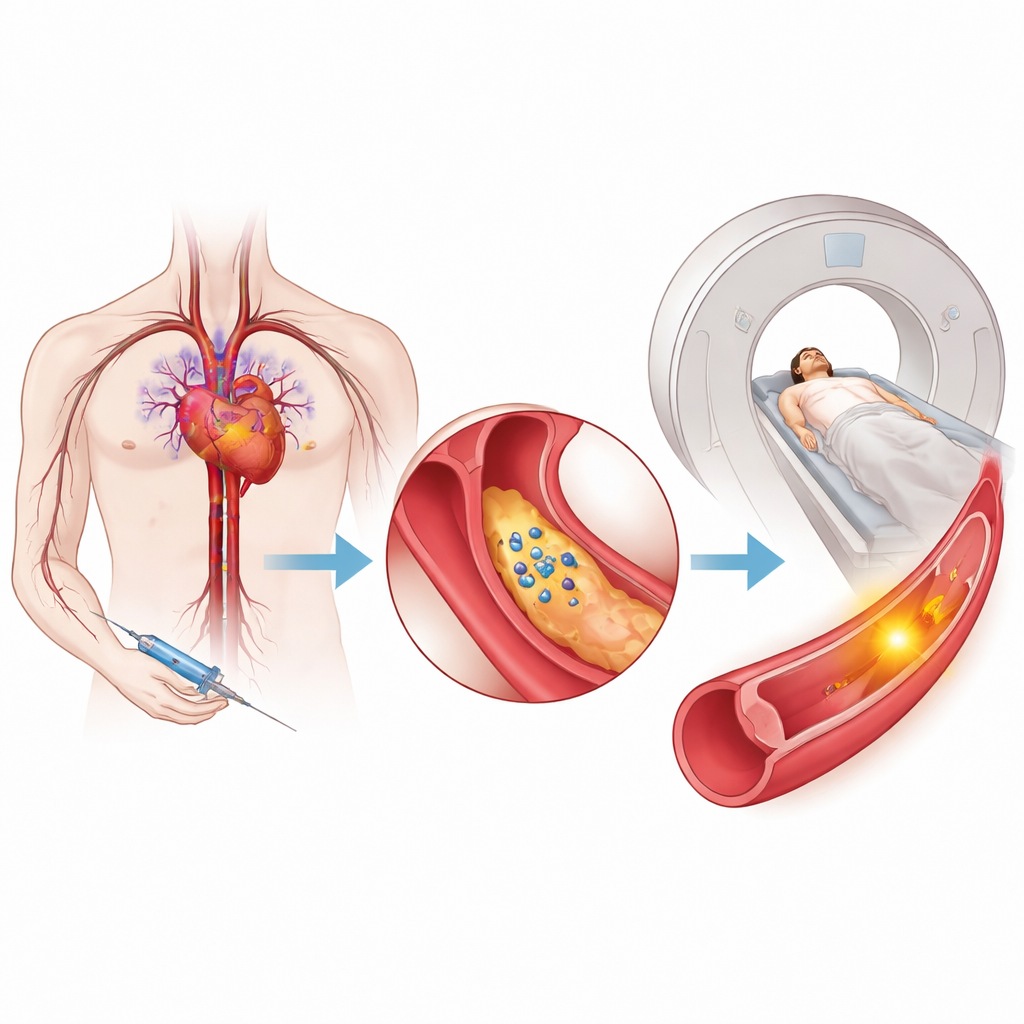
Скрытая опасность внутри артериальной бляшки
Атеросклероз — накопление жировых отложений в сосудах — является одной из ведущих причин инвалидности и преждевременной смерти в мире. Не все бляшки одинаково опасны: некоторые накопления относительно стабильны, тогда как другие приобретают тонкую «шляпку», воспаляются и склонны к разрыву, что провоцирует тромбы, способные перекрыть кровоток к сердцу или мозгу. Обычные исследования обычно показывают, насколько сужена артерия или сколько бляшек присутствует, но они не всегда надёжно указывают, активно ли эта бляшка разрушается и нестабильна. Существующие ПЭТ‑тракеры в основном подсвечивают общую иммунную активность и не могут чётко отличить вредное воспаление от воспаления, связанного с восстановлением.
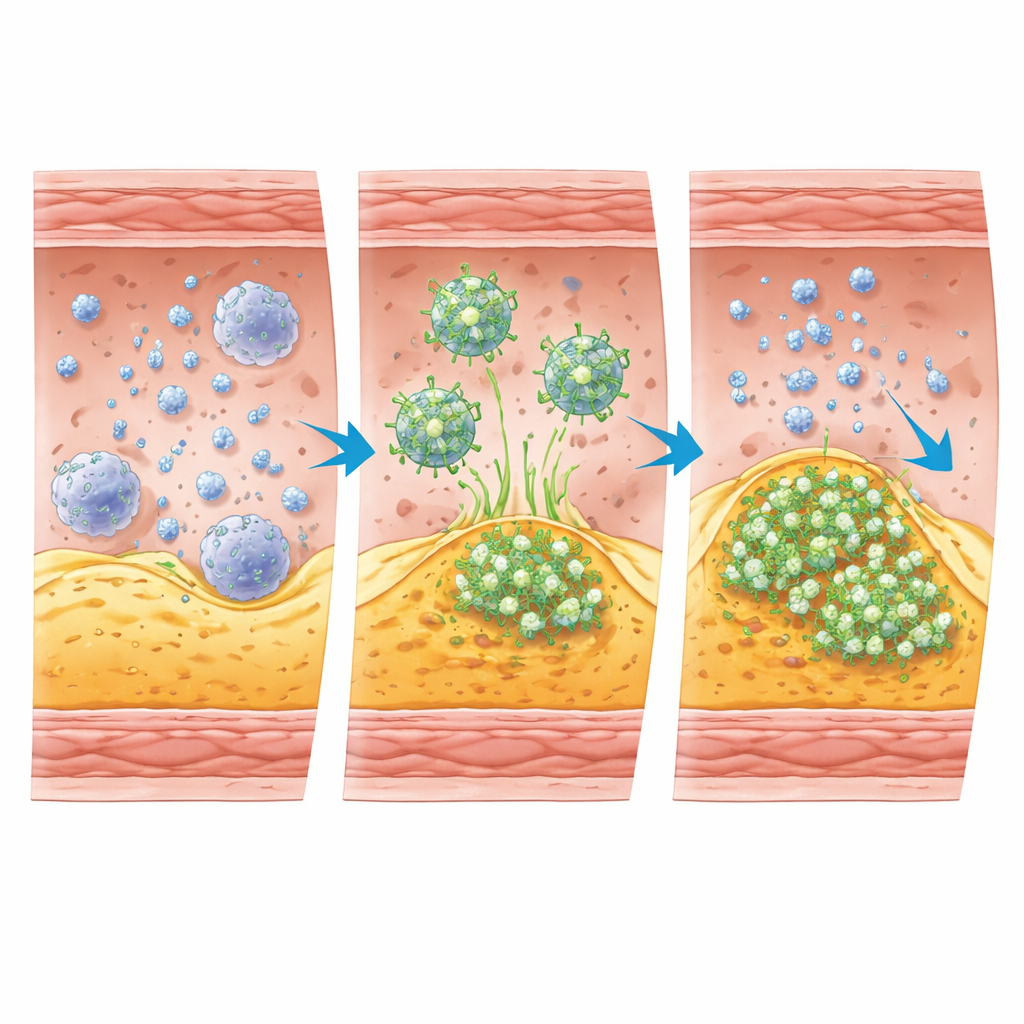
Фермент, отмечающий по‑настоящему опасное воспаление
Исследователи сосредоточились на миелопероксидазе (MPO) — ферменте, выделяемом некоторыми лейкоцитами при агрессивной, повреждающей ткани реакции. MPO помогает уничтожать микробы, но при выделении в пространство вокруг бляшки он может истончать защитную шляпку, разъедать поверхность и повышать вероятность образования тромбов. На животных и в клинических исследованиях показано, что бляшки с высокой активностью MPO чаще бывают нестабильными, а ингибирование MPO может стабилизировать бляшку без существенного изменения числа иммунных клеток. Это делает внеклеточную активность MPO перспективным маркером действительно опасного поведения бляшки, а не просто наличия воспаления.
Проектирование «умного» тракера, который прилипает там, где проблема
Чтобы зафиксировать этот сигнал, команда создала новый ПЭТ‑тракер под названием [68Ga]Ga‑IEMA. Химически он спроектирован так, чтобы обычно оставаться растворённым в крови и не проникать в клетки. В лабораторных тестах тракер был стабилен в сыворотке человека и обладал свойствами, предотвращающими прохождение через клеточные мембраны, то есть он в основном отражает события внеклеточного пространства. При встрече с активной MPO в присутствии её обычных окислителей молекулы тракера соединяются между собой и с близлежащими белками, образуя более крупные комплексы, которые задерживаются в ткани. Такое поведение «активация‑и‑приклеивание» превращает активность MPO в яркий ПЭТ‑сигнал в местах нестабильной бляшки.
Что показали исследования на животных
Учёные сначала подтвердили, что [68Ga]Ga‑IEMA можно быстро и чисто синтезировать с высокой радиохимической чистотой и что у мышей он выводится из крови главным образом через почки. Затем они использовали хорошо зарекомендовавшую себя модель мыши, в которой в разных сегментах артерий формируются как стабильные, так и нестабильные бляшки. ПЭТ/КТ‑сканирование показало, что тракер значительно сильнее накапливается в участках артерии, известных наличием нестабильной бляшки, чем в зонах со стабильными бляшками или без бляшек. У кроликов с продвинутым атеросклерозом невозобновлённая (нерадиоактивная) версия тракера была обнаружена в более высоких концентрациях в бляшках, которые разорвались или эродировали и образовали тромбы, по сравнению с более стабильными бляшками, что снова соответствовало ожиданиям для высокой активности MPO.
Перспективы применения у пациентов
В совокупности результаты указывают на то, что [68Ga]Ga‑IEMA функционирует как визуализатор внеклеточной активности MPO, выделяя бляшки, которые с большей вероятностью представляют опасность, а не просто большие по размеру. Поскольку он использует галлий‑68 и хелаторную химию, уже знакомую клинической нуклеарной медицине, перевод этого тракера в клинические исследования у людей может встретить относительно умеренные регуляторные препятствия и иметь дозы облучения, сопоставимые с обычно используемыми ПЭТ‑агентами. Если будущие испытания подтвердят его безопасность и эффективность у людей, этот тракер может помочь кардиологам локализовать уязвимые бляшки и оценить, действительно ли противовоспалительная терапия подавляет вредное артериальное воспаление, приближая уход к точному, основанному на риске подходу.
Цитирование: Keeling, G.P., Wang, X., Chen, W. et al. Development and validation of an activatable PET radiotracer reporting extracellular myeloperoxidase activity for the detection of unstable atherosclerotic plaque. npj Imaging 4, 23 (2026). https://doi.org/10.1038/s44303-026-00156-9
Ключевые слова: атеросклероз, ПЭТ‑визуализация, миелопероксидаза, уязвимая бляшка, радиотрактор