Clear Sky Science · pl
Opracowanie i walidacja aktywowanego radioterapeutyka PET raportującego pozakomórkową aktywność mieloperoksydazy do wykrywania niestabilnych blaszek miażdżycowych
Dlaczego to ma znaczenie dla zdrowia serca
Większość zawałów serca i udarów nie jest wywoływana przez największe zwężenia tętnic, lecz przez małe, kruche ogniska nagromadzenia tłuszczu, które nagle pękają lub ulegają erozji. Lekarze mają obecnie trudności z rozpoznaniem, które blaszek wkrótce spowodują powikłania. W tym badaniu przedstawiono nowy środek do obrazowania PET, zaprojektowany tak, aby uwidaczniać wyłącznie te „niebezpieczne” blaszki napędzane przez konkretny enzym zapalny, co potencjalnie może pomóc lekarzom zlokalizować obszary o wysokim ryzyku w tętnicach, zanim doprowadzą do stanu zagrożenia życia.
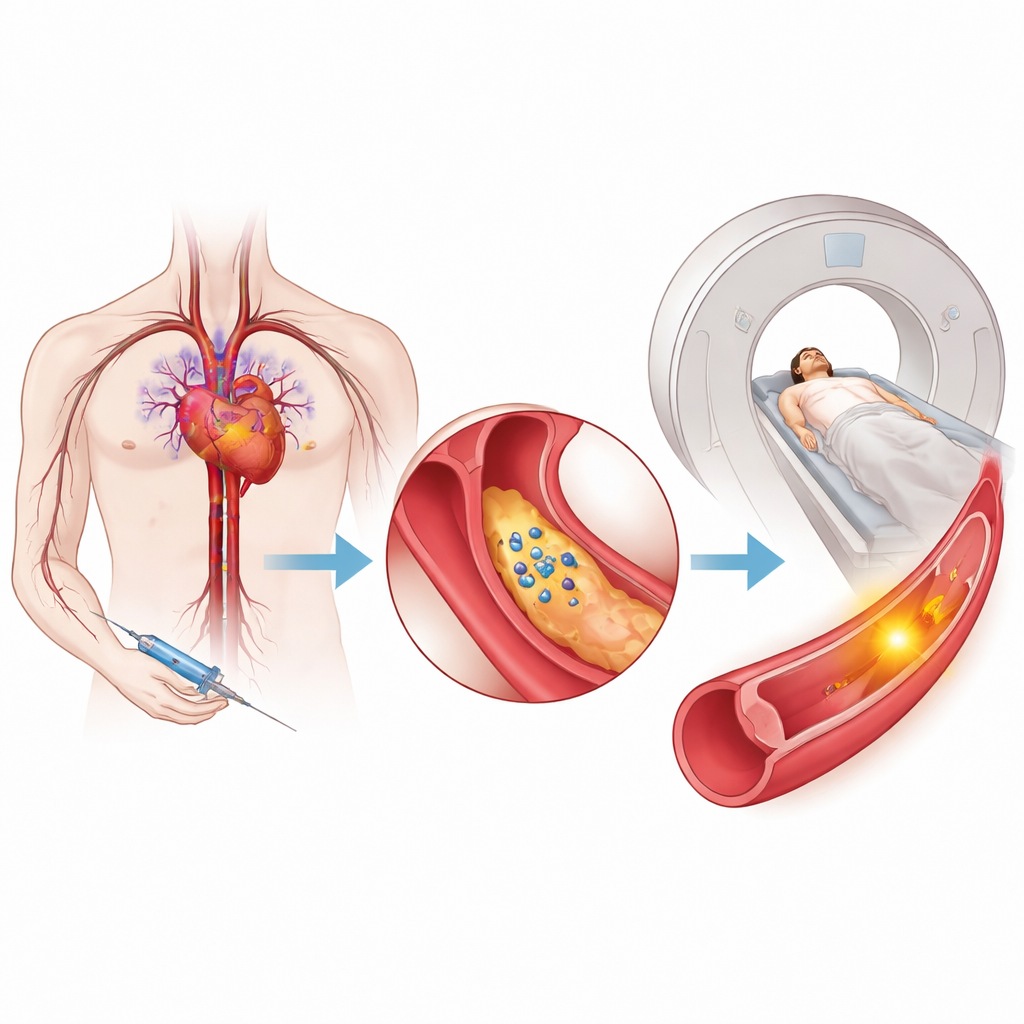
Ukryte niebezpieczeństwo wewnątrz blaszki tętniczej
Miażdżyca — nagromadzenie tłuszczu wewnątrz tętnic — jest wiodącą przyczyną niepełnosprawności i przedwczesnych zgonów na całym świecie. Nie wszystkie blaszki są jednakowo niebezpieczne: niektóre złogi są stosunkowo stabilne, podczas gdy inne mają cienką czapeczkę, są zapalone i podatne na pęknięcie, co uruchamia powstawanie skrzepów blokujących przepływ krwi do serca lub mózgu. Standardowe badania zazwyczaj pokazują, jak bardzo tętnica jest zwężona lub ile blaszki jest obecnych, ale nie ujawniają wiarygodnie, czy dana blaszka jest aktywnie uszkadzana i niestabilna. Istniejące znaczniki PET głównie uwidaczniają ogólną aktywność układu odpornościowego i nie potrafią jasno odróżnić zapalenia szkodliwego od zapalenia będącego częścią zdrowej reakcji naprawczej.
Enzym oznaczający naprawdę niebezpieczne zapalenie
Naukowcy skupili się na mieloperoksydazie (MPO), enzymie uwalnianym przez niektóre białe krwinki podczas agresywnej, tkankowo‑uszkadzającej odpowiedzi. MPO pomaga zabijać drobnoustroje, ale gdy przedostanie się do przestrzeni wokół blaszki, może przerzedzać ochronną czapeczkę, erodować powierzchnię i zwiększać prawdopodobieństwo powstawania skrzepów. Badania na zwierzętach i ludziach wykazały, że blaszki o wysokiej aktywności MPO częściej są niestabilne, a blokowanie MPO może stabilizować blaszki bez konieczności zmiany liczby obecnych komórek odpornościowych. To sprawia, że pozakomórkowa aktywność MPO jest obiecującym markerem naprawdę niebezpiecznego zachowania blaszki, a nie tylko obecności zapalenia.
Projektowanie inteligentnego znacznika, który zatrzymuje się tam, gdzie jest problem
Aby wykorzystać ten sygnał, zespół opracował nowy znacznik PET nazwany [68Ga]Ga‑IEMA. Chemicznie jest zbudowany tak, by normalnie pozostawać rozpuszczony we krwi i nie wnikać do komórek. W testach laboratoryjnych znacznik był stabilny w surowicy ludzkiej i miał właściwości uniemożliwiające przekraczanie błon komórkowych, co oznacza, że głównie raportuje zdarzenia pozakomórkowe. Gdy napotyka aktywną MPO w obecności jej typowych utleniaczy, cząsteczki znacznika łączą się ze sobą i wiążą z pobliskimi białkami, tworząc większe kompleksy, które zostają uwięzione w miejscowej tkance. To zachowanie „aktywuj i przyklej” przekształca aktywność MPO w wyraźny sygnał PET w miejscach niestabilnej blaszki.
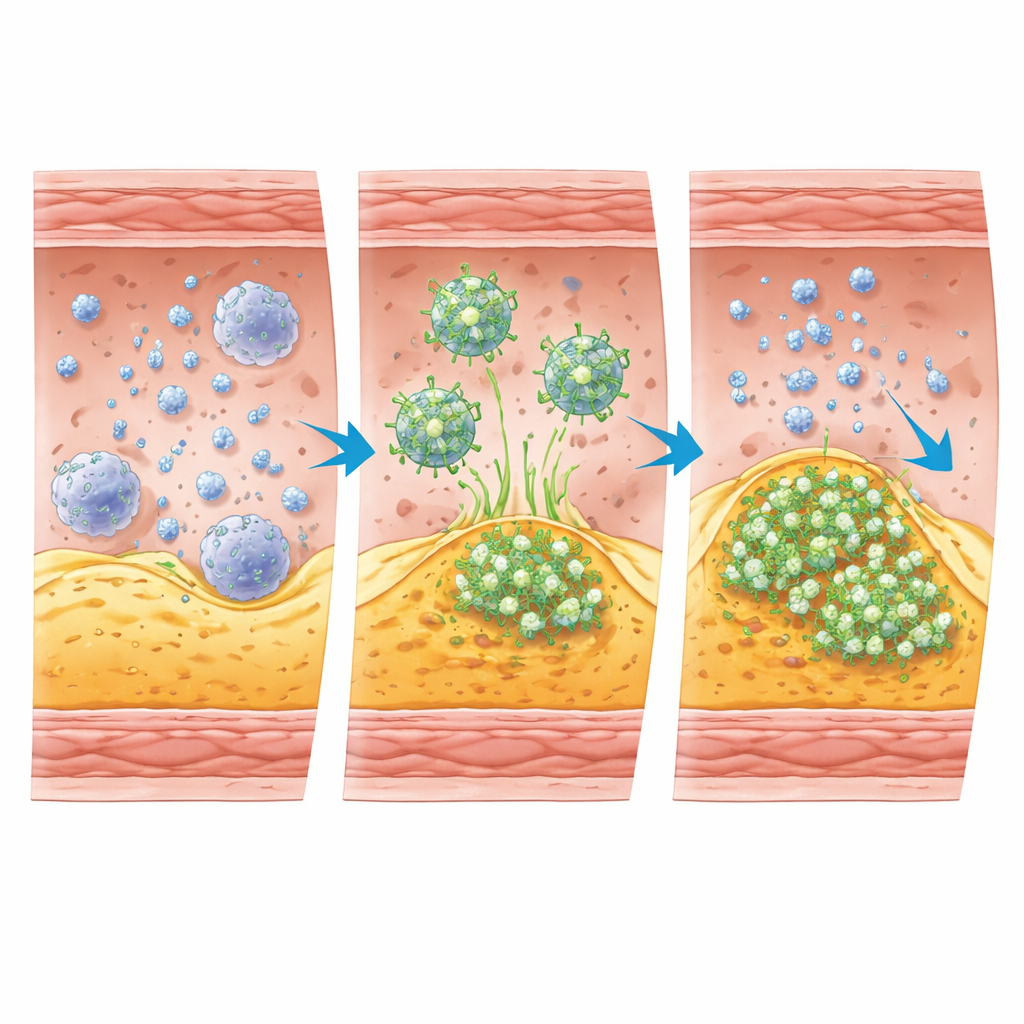
Co ujawniły badania na zwierzętach
Naukowcy najpierw potwierdzili, że [68Ga]Ga‑IEMA można wytworzyć szybko i czysto, z wysoką czystością radiochemiczną, oraz że u myszy jest wydalany z krwi głównie przez nerki. Następnie wykorzystali dobrze ugruntowany model myszy, który rozwija zarówno stabilne, jak i niestabilne blaszki w różnych odcinkach tętnic. Badania PET/CT wykazały, że znacznik gromadził się znacznie silniej w obszarze tętnicy znanym z obecności niestabilnej blaszki niż w regionach ze stabilną blaszką lub bez blaszki w ogóle. U królików z zaawansowaną miażdżycą, nieradiacyjna wersja znacznika wykazywała wyższe stężenia w blasz- kach, które pękły lub uległy erozji i utworzyły skrzepy, w porównaniu z bardziej stabilnymi blaszkami, ponownie odpowiadając oczekiwanemu wzorcowi wysokiej aktywności MPO.
Perspektywy zastosowania u pacjentów
Podsumowując, wyniki wskazują, że [68Ga]Ga‑IEMA działa jako reporter obrazowy pozakomórkowej aktywności MPO, uwidaczniając blaszki bardziej prawdopodobne do bycia niebezpiecznymi, a nie jedynie duże. Ponieważ wykorzystuje gal i um‑68 (gallium‑68) i chelatorową chemię już znaną w klinicznej medycynie nuklearnej, znacznik mógłby zostać przetłumaczony na badania u ludzi przy relatywnie umiarkowanych przeszkodach regulacyjnych oraz dawkach promieniowania podobnych do powszechnie stosowanych środków PET. Jeśli przyszłe badania potwierdzą jego bezpieczeństwo i skuteczność u ludzi, znacznik mógłby pomóc kardiologom zlokalizować wrażliwe blaszki i ocenić, czy terapie przeciwzapalne rzeczywiście łagodzą szkodliwe zapalenie tętnic, przybliżając opiekę do precyzyjnego podejścia opartego na ryzyku.
Cytowanie: Keeling, G.P., Wang, X., Chen, W. et al. Development and validation of an activatable PET radiotracer reporting extracellular myeloperoxidase activity for the detection of unstable atherosclerotic plaque. npj Imaging 4, 23 (2026). https://doi.org/10.1038/s44303-026-00156-9
Słowa kluczowe: miażdżyca, obrazowanie PET, mieloperoksydaza, niestabilna blaszka, znacznik radiologiczny